Clear Sky Science · ru
Интегрированное электрическое моделирование циркулирующих опухолевых клеток для улучшенного диэлектрофоретического захвата и электропорации
Почему крошечные электрические разряды важны для клеток крови
Рак может рассылать в кровоток несколько побочных клеток задолго до того, как опухоль станет заметна на сканировании. Эти циркулирующие опухолевые клетки представляют собой ценные подсказки для ранней диагностики и индивидуального подбора лечения, но они редки и с ними трудно обращаться, не повредив остальную часть крови. В этой работе изучается, как специально сформированные электрические поля внутри компактного устройства «лаборатория-на-чипе» могут аккуратно улавливать эти блуждающие раковые клетки, временно открывать микропоры в их мембранах, а затем позволять им восстановиться — при этом здоровые клетки крови в значительной степени остаются невредимыми.
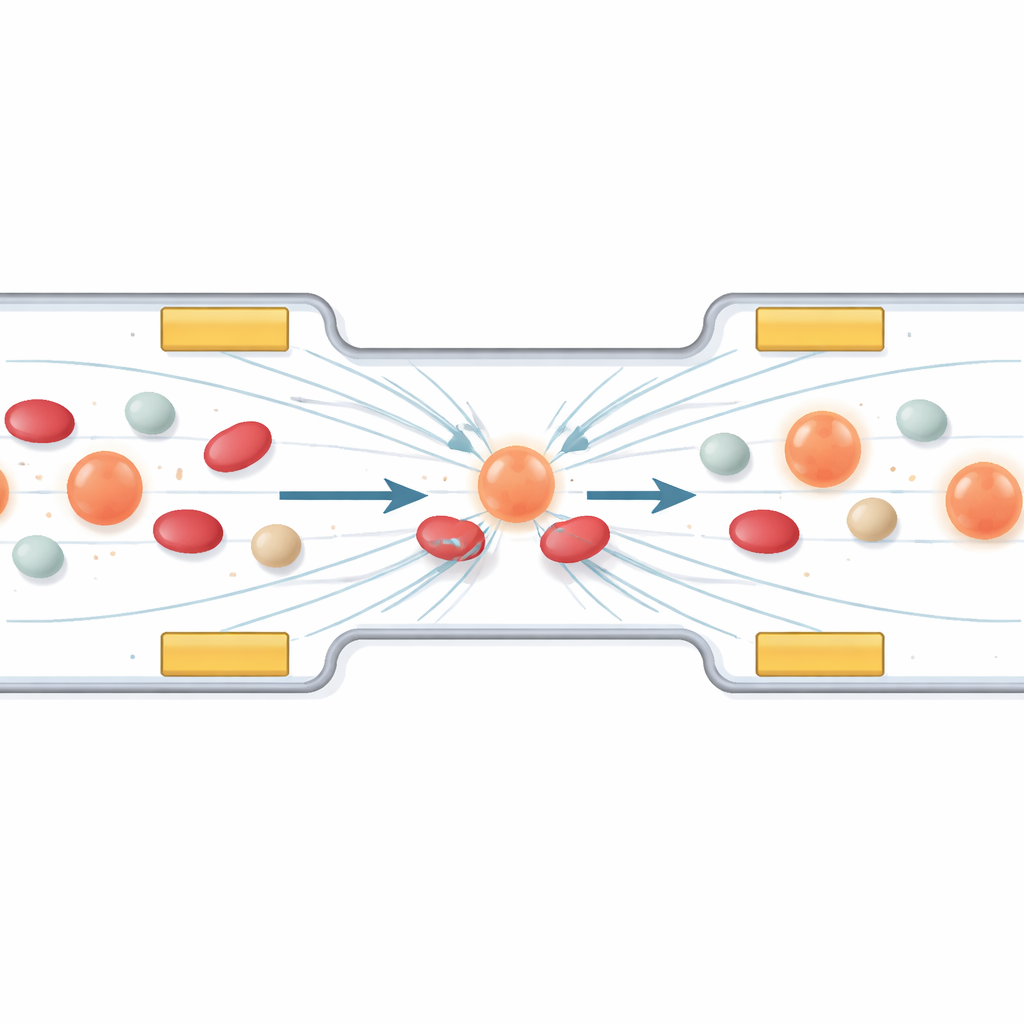
Использование невидимых сил для улавливания блуждающих раковых клеток
Первая часть работы исследует, как направлять и собирать определённые клетки с помощью явления, называемого диэлектрофорезом. Проще говоря, при приложении переменного электрического поля вдоль микроканала клетки испытывают небольшие толчки и притяжения, которые зависят от их размера и электрических свойств. Авторы разрабатывают расположение миниатюрных электродов так, чтобы циркулирующие опухолевые клетки смещались в стабильную «полосу парковки» между электродами, в то время как более мелкие или менее поляризуемые компоненты крови проходили мимо. Компьютерные симуляции показывают, как изменение напряжения и частоты формирует поле, отводя клетки от зон с высоким полем и выстраивая их в нужной области для обработки. Защитный слой над электродами предотвращает повреждение клеток при прямом контакте.
Открытие и закрытие микроскопических дверей в оболочках клеток
Когда клетки зафиксированы, устройство подаёт ультракороткие электрические импульсы, которые кратковременно пробивают в наружной мембране поры нанометрового масштаба. В исследовании построена подробная математическая модель этого процесса для трёх ключевых игроков крови: циркулирующих опухолевых клеток, лейкоцитов и тромбоцитов. Модель отслеживает, как повышается напряжение на каждой клеточной мембране, когда появляются первые поры, насколько они увеличиваются и каково их количество, а также как быстро мембрана заживает. Настраивая как силу поля, так и длительность импульса, команда выделяет оптимальные режимы, при которых мембрана становится достаточно проницаемой для введения лекарств или генетического материала, но затем восстанавливается без гибели клетки. Для опухолевых и белых кровяных клеток эффективные поля лежат в диапазоне 1–4 кВ/см, тогда как гораздо меньшим тромбоцитам требуется примерно в десять раз более сильное поле для достижения того же эффекта.
Разные клетки крови — разные оптимумы
Моделирование показывает, как размер клетки и её электрические свойства меняют отклик на поле. Более крупные циркулирующие опухолевые клетки и лейкоциты заряжаются медленнее и достигают пикового напряжения на мембране примерно через два микросекунды после начала импульса; их поры растут, а затем закрываются в течение десятков микросекунд до секунд. Напротив, крошечные тромбоциты реагируют почти мгновенно, с более быстрой формированием и закрытием пор. Для всех типов клеток наиболее интенсивные процессы происходят на «гиперполяризованной» стороне клетки, обращённой к входящему полю, где силы концентрируются. Это означает, что, выбирая подходящую силу поля для данного размера клетки, возможно способствовать открытию пор в опухолевых клетках при минимизации повреждений здоровых соседей, что закладывает основы для высокоселективных подходов.
Проверка идеи на реальных клетках на чипе
Чтобы проверить соответствие симуляций реальности, авторы изготовили микрофлюидный чип, объединяющий захватывающие электроды с центральной зоной сенсора. Они пропускали через канал модельную линию лейкоцитов (клетки THP‑1) и повышали напряжение на фиксированном зазоре. Вместо прямого наблюдения за порами они измеряли, насколько легко переменный ток проходил через суспензию. По мере роста электрического поля общая сопротивляемость смеси клеток падала, а её ёмкостное поведение снижалось — признаки того, что мембраны стали более проводящими и меньше похожими на целостные изоляторы. При наивысших испытанных полях электрический отклик был обусловлен проводимостью через открытые поры, что тесно соответствовало тенденциям, предсказанным компьютерной моделью.
Что это может значить для будущего онкологической помощи
Проще говоря, это исследование показывает, что один компактный чип может одновременно отбирать редкие раковые клетки из крови и аккуратно открывать их мембраны в строго контролируемом режиме. Подбирая силу и длительность импульса под каждый тип клетки, подход позволяет либо сохранять клетки живыми для детального анализа и тестирования лекарств, либо доводить их до необратимого повреждения для целенаправленного уничтожения, при этом минимизируя нагрев и вред здоровым клеткам. Для неспециалистов ключевая мысль такова: с правильной «электрической хореографией» мы можем превратить крошечные токи в мощные инструменты для раннего обнаружения рака, точечной доставки лекарств и, возможно, более безопасных и сфокусированных терапевтических вмешательств.
Цитирование: Sherif, S., Ghallab, Y.H. & Ismail, Y. Integrated electrical modeling of circulating tumor cells for enhanced dielectrophoretic trapping and electroporation. Sci Rep 16, 12072 (2026). https://doi.org/10.1038/s41598-026-45747-z
Ключевые слова: циркулирующие опухолевые клетки, микрофлюидная электропорация, диэлектрофорез, диагностика рака, лаборатория-на-чипе