Clear Sky Science · nl
Geïntegreerde elektrische modellering van circulerende tumorcellen voor verbeterde dielectroforetische vangst en elektroporatie
Waarom kleine elektrische schokjes voor bloedcellen ertoe doen
Kanker kan al vroeg enkele afwezige cellen in de bloedbaan loslaten, lang voordat een tumor op een scan zichtbaar is. Deze circulerende tumorcellen zijn waardevolle aanwijzingen voor vroege diagnose en gepersonaliseerde behandelingen, maar ze zijn zeldzaam en moeilijk te hanteren zonder de rest van het bloed te beschadigen. Dit artikel onderzoekt hoe zorgvuldig gevormde elektrische velden in een klein lab‑on‑a‑chip‑apparaat deze rondzwervende kankercellen zachtjes kunnen vangen, tijdelijke kleine poorten in hun membranen kunnen openen en hen daarna kunnen laten herstellen — terwijl gezonde bloedcellen grotendeels ongemoeid blijven.
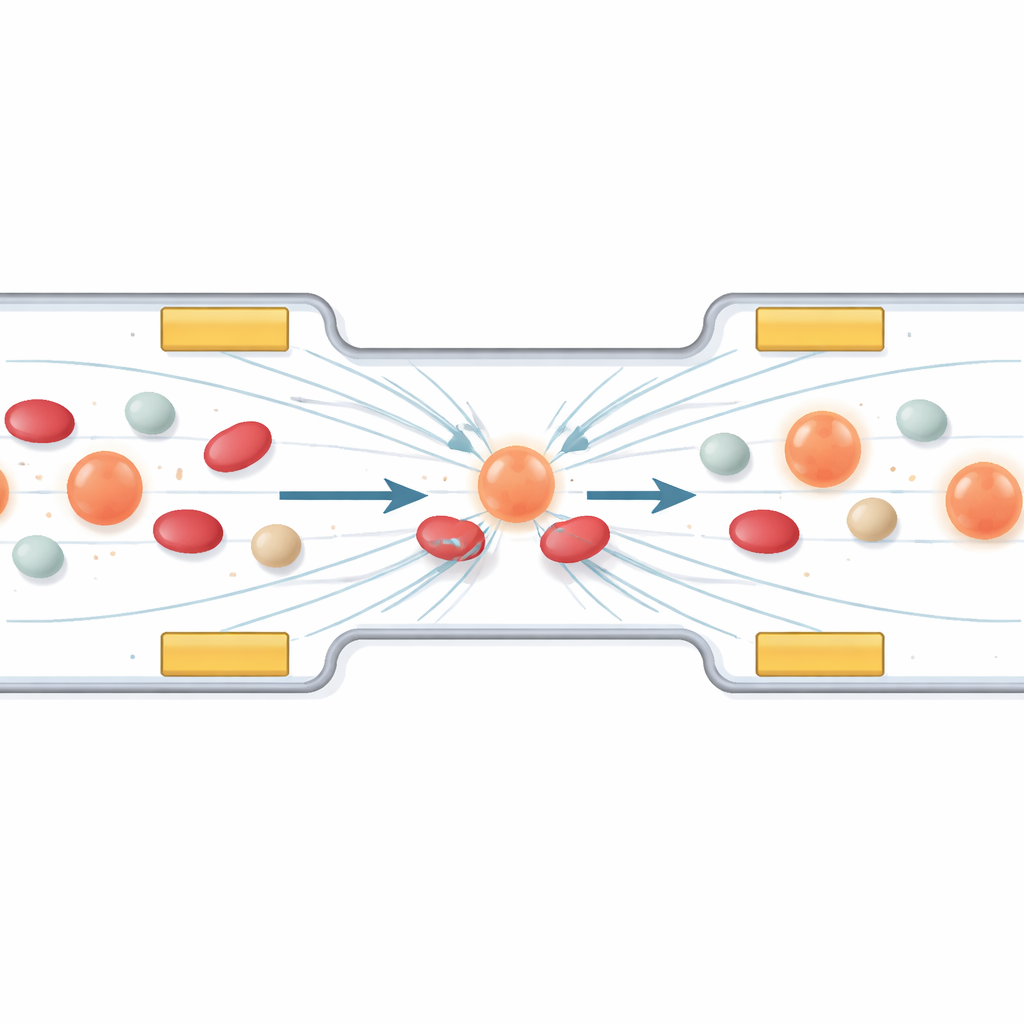
Onzichtbare krachten gebruiken om rondzwervende kankercellen te vangen
Het eerste deel van het werk onderzoekt hoe specifieke cellen te sturen en te verzamelen met behulp van een verschijnsel dat dielectroforese wordt genoemd. In eenvoudige bewoordingen: wanneer een wisselend elektrisch veld over een microkanaal wordt aangelegd, voelen cellen kleine duwtjes en trektjes die afhangen van hun grootte en elektrische eigenschappen. De auteurs ontwerpen een rangschikking van miniatuurelektroden zodat circulerende tumorcellen in een stabale “parkeerbaan” tussen de elektroden drijven, terwijl kleinere of minder polariseerbare bloedbestanddelen passeren. Computersimulaties tonen hoe het variëren van spanning en frequentie het veld vormt, waardoor cellen uit hoogveldzones worden geleid en in de juiste regio voor behandeling op een rij komen te staan. Een beschermende laag over de elektroden voorkomt dat de cellen door direct contact beschadigd raken.
Microscopische deurtjes openen en sluiten in celmembranen
Wanneer cellen op hun plaats worden gehouden, levert het apparaat ultrakorte elektrische pulsen die tijdelijk nanometergrote poriën in het buitenste membraan slaan. De studie bouwt een gedetailleerd wiskundig model van dit proces voor drie belangrijke bloedspelers: circulerende tumorcellen, witte bloedcellen en bloedplaatjes. Het volgt hoe de spanning over elk celmembraan stijgt, wanneer poriën voor het eerst verschijnen, hoe groot en talrijk ze worden en hoe snel het membraan weer sluit. Door zowel veldsterkte als pulslengte af te stemmen, identificeert het team optimale instellingen waarbij het membraan voldoende lek wordt om geneesmiddelen of genetisch materiaal binnen te laten, maar daarna geneest zonder de cel te doden. Voor tumor- en witte bloedcellen liggen effectieve velden in het bereik van 1–4 kilovolt per centimeter, terwijl de veel kleinere bloedplaatjes ongeveer tienmaal sterkere velden nodig hebben om hetzelfde effect te bereiken.
Verschillende bloedcellen, verschillende optimale instellingen
De modellering toont hoe celgrootte en elektrische eigenschappen bepalen hoe elke cel reageert. Grotere circulerende tumorcellen en witte bloedcellen laden langzamer op en bereiken een piekspanning over het membraan ongeveer twee microseconden na aanvang van de puls; hun poriën groeien en sluiten daarna over tientallen microseconden tot seconden. Kleine bloedplaatjes reageren daarentegen vrijwel onmiddellijk, met snellere porievorming en -herstel. Bij alle celtypen vindt de meest intense activiteit plaats aan de “hypergepolariseerde” zijde van de cel die naar het inkomende veld gericht is, waar de krachten zich concentreren. Dit betekent dat door de juiste veldsterkte te kiezen voor een bepaalde cellengrootte, het mogelijk is poriën in tumorcellen te bevorderen terwijl schade aan gezonde buren gering blijft, waarmee de basis wordt gelegd voor zeer selectieve behandelingen.
Het idee testen met echte cellen op een chip
Om te controleren of de simulaties overeenkomen met de werkelijkheid, bouwden de auteurs een microfluïdische chip die vangende elektroden combineert met een centraal sensorgedeelte. Ze lieten een model-lijn van witte bloedcellen (THP‑1‑cellen) door het kanaal stromen en pasten toen oplopende spanningen toe over een vaste opening. In plaats van de poriën direct te observeren, maten ze hoe gemakkelijk een wisselstroom door de suspensie liep. Naarmate het elektrische veld toenam, daalde de algehele weerstand van het cellenmengsel en verdween het capacitatieve gedrag, wat aangeeft dat de membranen geleidelijk meer geleidend waren geworden en minder op intacte isolatoren leken. Bij de hoogste geteste velden werd de elektrische respons gedomineerd door geleiding door open poriën, hetgeen nauw aansloot bij de trends die het computermodel voorspelde.
Wat dit kan betekenen voor toekomstige kankerzorg
Simpel gezegd toont deze studie aan dat één compact chip zowel zeldzame kankercellen uit bloed kan scheiden als hun membranen op een hoog gecontroleerde manier zachtelijk kan openen. Door pulssterkte en timing af te stemmen op elk celtype kan de aanpak cellen levend houden voor gedetailleerde analyse en medicijntests, of ze juist naar onomkeerbare schade sturen voor gerichte vernietiging, terwijl verwarming en schade aan gezonde cellen tot een minimum worden beperkt. Voor het brede publiek is de kernboodschap dat we met de juiste “elektrische choreografie” kleine stromen kunnen omzetten in krachtige instrumenten voor vroege kankeropsporing, precieze medicijnafgifte en mogelijk veiligere, meer gerichte kankertherapieën.
Bronvermelding: Sherif, S., Ghallab, Y.H. & Ismail, Y. Integrated electrical modeling of circulating tumor cells for enhanced dielectrophoretic trapping and electroporation. Sci Rep 16, 12072 (2026). https://doi.org/10.1038/s41598-026-45747-z
Trefwoorden: circulerende tumorcellen, microfluidische elektroporatie, dielectroforese, kankerdiagnostiek, lab-on-a-chip