Clear Sky Science · tr
Dolaşımdaki tümör hücrelerinin dielektroforetik tuzaklama ve elektroperforasyonunun geliştirilmesi için bütünleşik elektriksel modelleme
Kan hücrelerine uygulanan küçük elektrik şoklarının önemi
Tümör, görüntüleme ile bulunmadan çok önce birkaç serseri hücreyi kana bırakabilir. Bu dolaşımdaki tümör hücreleri erken tanı ve kişiye özel tedaviler için değerli ipuçlarıdır, ancak nadir ve işlenmesi zor olup diğer kan hücrelerine zarar vermeden ayrıştırılmaları zordur. Bu makale, küçük bir çip içindeki özenle şekillendirilmiş elektrik alanlarının bu dolaşan kanser hücrelerini nazikçe yakalayıp onların zarında geçici küçük kapılar açmasını ve ardından hücrelerin toparlanmasına izin vermesini — tüm bunları sağlıklı kan hücrelerine büyük oranda zarar vermeden — nasıl mümkün kılabileceğini inceliyor.
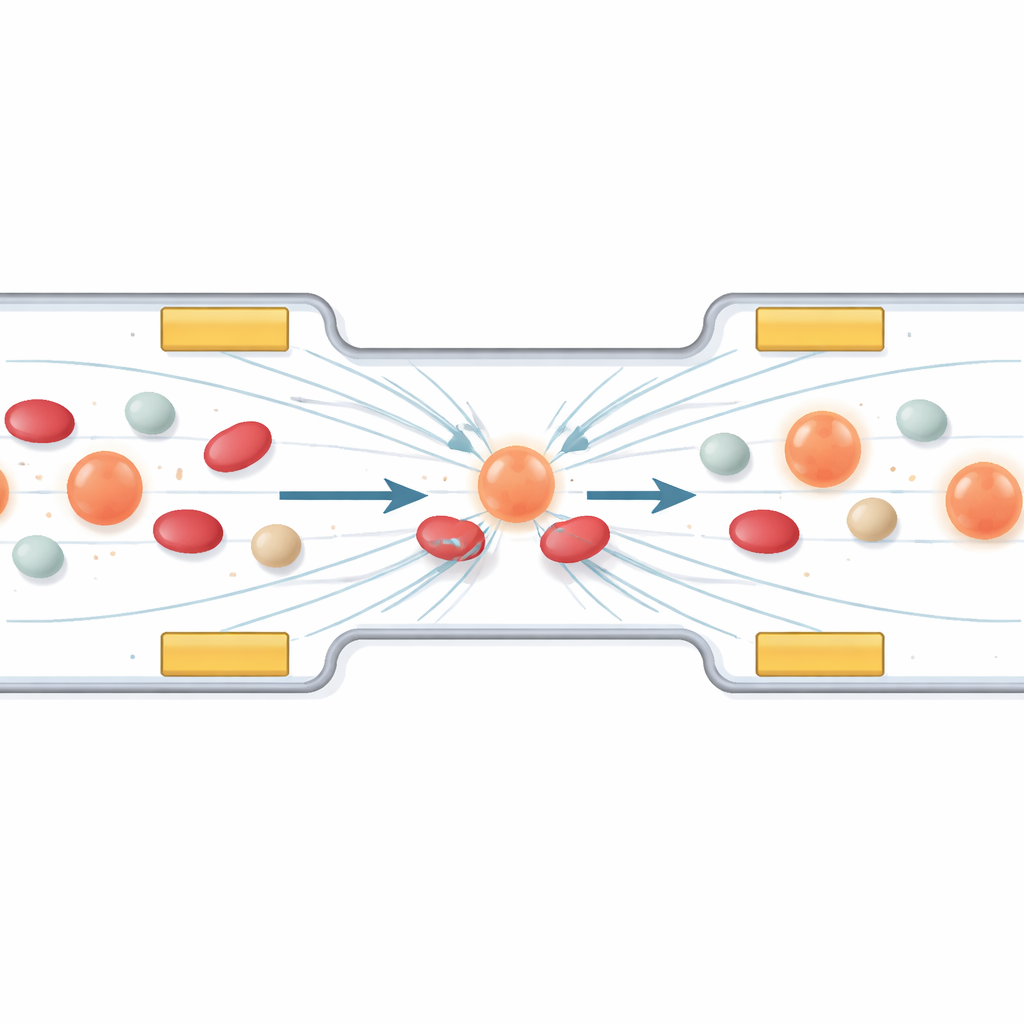
Dolaşan kanser hücrelerini yakalamak için görünmez kuvvetler kullanmak
Çalışmanın ilk bölümü, dielektroforez adı verilen bir olgunun kullanılarak belirli hücrelerin nasıl yönlendirip toplanacağını araştırıyor. Basitçe söylemek gerekirse, bir mikrokanal boyunca alternatif bir elektrik alanı uygulandığında, hücreler boyutlarına ve elektriksel yapısına bağlı olarak küçük itme ve çekme kuvvetleri hisseder. Yazarlar, dolaşımdaki tümör hücrelerinin aralarında kararlı bir “park şeridine” doğru sürüklendiği, daha küçük veya daha az polarize kan bileşenlerinin ise geçip gittiği bir minyatür elektrot düzeni tasarlar. Bilgisayar simülasyonları, voltaj ve frekansın alanı nasıl şekillendirdiğini, hücreleri yüksek alan bölgelerinden uzaklaştırıp tedavi için doğru bölgede hizaladığını gösterir. Elektrotların üzerindeki koruyucu bir katman, hücrelerin doğrudan temas nedeniyle zarar görmesini önler.
Hücre zarlarında mikroskobik kapılar açıp kapamak
Hücreler yerinde tutulduktan sonra cihaz, dış zarda nanometre ölçeğinde kısa süreli gözenekler açan ultrakısa elektrik darbeleri verir. Çalışma, dolaşımdaki üç ana kan oyuncusu için bu sürecin ayrıntılı matematiksel modelini oluşturur: dolaşımdaki tümör hücreleri, akyuvarlar ve trombositler. Her hücre zarında voltajın nasıl yükseldiğini, gözeneklerin ne zaman ilk ortaya çıktığını, ne kadar büyük ve sayıca nasıl çoğaldıklarını ve zarın ne kadar çabuk yeniden kapandığını izler. Alan şiddeti ve darbe süresini ayarlayarak ekip, zarın ilaç veya genetik madde alacak kadar sızdırgan hale gelip sonra hücreyi öldürmeden iyileştiği tatlı noktaları belirler. Tümör ve akyuvar hücreleri için etkili alanlar santimetre başına 1–4 kilovolt aralığında iken, çok daha küçük trombositlerin aynı etkiyi görmek için yaklaşık on kat daha güçlü alanlara ihtiyacı vardır.
Farklı kan hücreleri, farklı en uygun alanlar
Modelleme, hücre büyüklüğü ve elektriksel özelliklerin her hücrenin yanıtını nasıl değiştirdiğini ortaya koyuyor. Daha büyük dolaşımdaki tümör hücreleri ve akyuvarlar daha yavaş şarj olur ve darbenin yaklaşık iki mikro-saniyesinde zar voltajında tepeye ulaşır; onların gözenekleri büyür ve ardından on mikro-saniyelerden saniyelere kadar uzanan sürelerde kapanır. Buna karşılık küçük trombositler neredeyse anında yanıt verir, daha hızlı gözenek oluşumu ve yeniden kapanma gösterir. Tüm hücre tiplerinde en yoğun etki, gelen alan tarafında bulunan ve kuvvetlerin yoğunlaştığı "hiperpolarize" bölgede gerçekleşir. Bu, belirli bir hücre boyutu için doğru alan şiddeti seçildiğinde, sağlıklı komşulara zarar vermeyi düşük tutarken tümör hücrelerinde gözenek açılmasını tercih etmenin mümkün olduğu anlamına gelir; bu da yüksek seçiciliğe sahip tedaviler için zemin hazırlar.
Çip üzerinde gerçek hücrelerle fikri test etmek
Simülasyonların gerçeklikle örtüşüp örtüşmediğini kontrol etmek için yazarlar, tuzaklama elektrotlarını merkezi bir algılama bölgesiyle birleştiren bir mikroakışkan çip inşa ettiler. Kanal boyunca model bir akyuvar hücre hattı (THP‑1 hücreleri) akıttılar ve sabit bir aralık üzerinden artan voltajlar uyguladılar. Gözenekleri doğrudan izlemek yerine, süspansiyonun alternatif akıma karşı iletkenliğini ölçtüler. Elektrik alan büyüdükçe, hücre karışımının genel direnci düştü ve kapasitif davranışı azaldı; bunlar zarların daha iletken ve sağlam yalıtkanlar gibi olmaktan çıktığının işaretleridir. Test edilen en yüksek alanlarda, elektriksel yanıt açık gözenekler üzerinden iletim tarafından domine edildi ve bu, bilgisayar modelinin öngördüğü eğilimleri yakından yansıttı.
Gelecekteki kanser bakımına olası etkileri
Basitçe söylemek gerekirse, bu çalışma tek bir kompakt çipin nadir kanser hücrelerini kandan ayırabileceğini ve zarlarını yüksek derecede kontrol altında nazikçe açabileceğini gösteriyor. Darbe şiddetini ve zamanlamasını her hücre tipine göre uyarlayarak yaklaşım, hücreleri ayrıntılı analiz ve ilaç testleri için canlı tutacak şekilde kullanabileceği gibi, hedefe yönelik yıkım için geri döndürülemez hasara da yönlendirebilir; tüm bunlar ısınma ve sağlıklı hücre zararını en aza indirerek yapılabilir. Genel okuyucu için ana mesaj şudur: doğru "elektriksel koreografi" ile küçük akımlar, erken kanser tespiti, hassas ilaç teslimatı ve muhtemelen daha güvenli, daha odaklı kanser tedavileri için güçlü araçlara dönüşebilir.
Atıf: Sherif, S., Ghallab, Y.H. & Ismail, Y. Integrated electrical modeling of circulating tumor cells for enhanced dielectrophoretic trapping and electroporation. Sci Rep 16, 12072 (2026). https://doi.org/10.1038/s41598-026-45747-z
Anahtar kelimeler: dolaşımdaki tümör hücreleri, mikroakışkan elektroperforasyon, dielektroforez, kanser tanısı, çip üzerinde laboratuvar