Clear Sky Science · pt
Modelagem elétrica integrada de células tumorais circulantes para aprimorar captura por dieletroforese e eletroporação
Por que pequenas descargas elétricas nas células do sangue importam
O câncer pode liberar algumas células renegadas na corrente sanguínea muito antes de um tumor ser detectado em uma imagem. Essas células tumorais circulantes são pistas valiosas para diagnóstico precoce e tratamentos personalizados, mas são raras e difíceis de manipular sem prejudicar o restante do sangue. Este artigo explora como campos elétricos cuidadosamente moldados dentro de um pequeno dispositivo lab-on-a-chip podem capturar suavemente essas células cancerígenas errantes, abrir portinhas temporárias em suas membranas e depois permitir que se recuperem — tudo isso enquanto deixam as células sanguíneas saudáveis amplamente intactas.
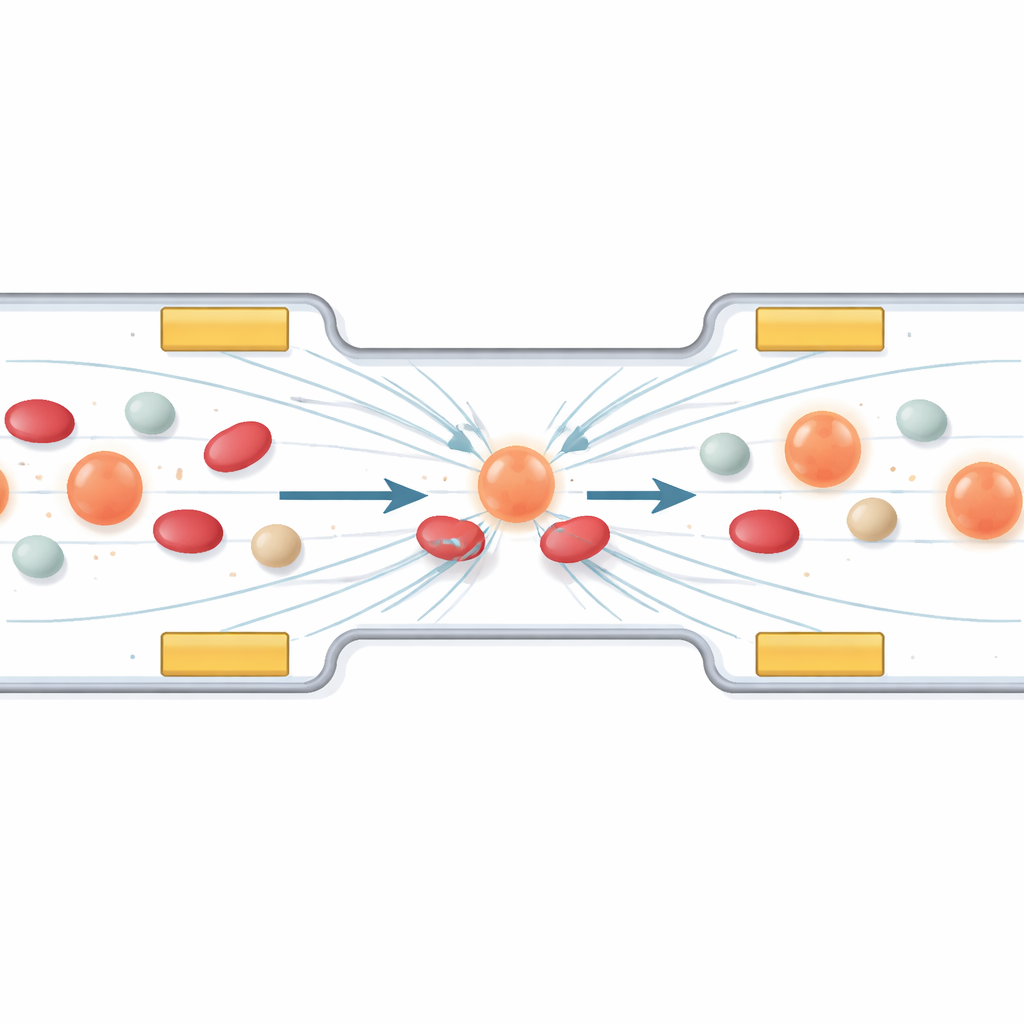
Usando forças invisíveis para capturar células cancerígenas em trânsito
A primeira parte do trabalho investiga como direcionar e coletar células específicas usando um fenômeno chamado dieletroforese. Em termos simples, quando um campo elétrico alternado é aplicado através de um microcanal, as células sentem pequenos impulsos que dependem de seu tamanho e constituição elétrica. Os autores projetam um arranjo de eletrodos em miniatura de modo que as células tumorais circulantes migrem para uma “faixa de estacionamento” estável entre eles, enquanto componentes sanguíneos menores ou menos polarizáveis passam adiante. Simulações por computador mostram como alterar a tensão e a frequência molda o campo, guiando as células para fora de zonas de campo intenso e alinhando‑as na região correta para tratamento. Uma camada protetora sobre os eletrodos evita que as células sejam danificadas por contato direto.
Abrindo e fechando portas microscópicas nas peles celulares
Uma vez que as células são mantidas no lugar, o dispositivo entrega pulsos elétricos ultracurtos que brevemente perfuram poros de escala nanométrica na membrana externa. O estudo constrói um modelo matemático detalhado desse processo para três atores-chave no sangue: células tumorais circulantes, leucócitos e plaquetas. Ele acompanha como a voltagem através de cada membrana celular aumenta, quando os poros aparecem pela primeira vez, quão grandes e numerosos eles se tornam e com que rapidez a membrana se fecha novamente. Ao ajustar tanto a intensidade do campo quanto a duração do pulso, a equipe identifica pontos ótimos onde a membrana fica suficientemente permeável para admitir drogas ou material genético e então cicatriza sem matar a célula. Para células tumorais e leucócitos, campos eficazes situam‑se na faixa de 1–4 quilovolts por centímetro, enquanto as muito menores plaquetas precisam de campos cerca de dez vezes mais intensos para alcançar o mesmo efeito.
Diferentes células sanguíneas, diferentes pontos ótimos
A modelagem revela como o tamanho celular e as propriedades elétricas alteram a resposta de cada célula. Células tumorais circulantes maiores e leucócitos carregam-se mais lentamente e alcançam a tensão máxima na membrana por volta de dois microssegundos após o pulso; seus poros crescem e depois se fecham ao longo de dezenas de microssegundos a segundos. As minúsculas plaquetas, por contraste, respondem quase instantaneamente, com formação e fechamento de poros mais rápidos. Em todos os tipos celulares, a ação mais intensa ocorre no lado “hiperpolarizado” da célula voltado para o campo incidente, onde as forças se concentram. Isso significa que, escolhendo a intensidade de campo adequada para um dado tamanho celular, é possível favorecer a abertura de poros em células tumorais enquanto se mantém o dano às vizinhas saudáveis baixo, lançando as bases para tratamentos altamente seletivos.
Testando a ideia com células reais em um chip
Para verificar se as simulações refletem a realidade, os autores construíram um chip microfluídico que combina eletrodos de captura com uma zona central de detecção. Eles fizeram fluir uma linhagem modelo de leucócitos (células THP‑1) pelo canal e aplicaram tensões crescentes através de uma fenda fixa. Em vez de observar os poros diretamente, mediram quão facilmente uma corrente alternada passava pela suspensão. À medida que o campo elétrico aumentava, a resistência global da mistura celular caiu e seu comportamento capacitivo diminuiu — assinaturas de que as membranas ficaram mais condutoras e menos parecidas com isolantes intactos. Nos campos mais altos testados, a resposta elétrica passou a ser dominada pela condução através de poros abertos, espelhando de perto as tendências previstas pelo modelo computacional.
O que isso pode significar para o futuro do cuidado contra o câncer
Em termos simples, este estudo demonstra que um único chip compacto pode tanto separar células cancerígenas raras do sangue quanto abrir suas membranas de forma controlada e delicada. Ao ajustar a intensidade e o tempo dos pulsos para cada tipo celular, a abordagem pode manter as células vivas para análises detalhadas e testes de medicamentos ou empurrá‑las rumo a danos irreversíveis para destruição direcionada, minimizando aquecimento e danos às células saudáveis. Para um público leigo, a mensagem chave é que, com a “coreografia elétrica” certa, podemos transformar correntes minúsculas em ferramentas poderosas para detecção precoce do câncer, entrega precisa de medicamentos e, possivelmente, terapias contra o câncer mais seguras e focadas.
Citação: Sherif, S., Ghallab, Y.H. & Ismail, Y. Integrated electrical modeling of circulating tumor cells for enhanced dielectrophoretic trapping and electroporation. Sci Rep 16, 12072 (2026). https://doi.org/10.1038/s41598-026-45747-z
Palavras-chave: células tumorais circulantes, eletroporação microfluídica, dieletroforese, diagnósticos de câncer, lab-on-a-chip