Clear Sky Science · de
Integrierte elektrische Modellierung zirkulierender Tumorzellen zur verbesserten dielektrophoretischen Anreicherung und Elektroporation
Warum winzige elektrische Stöße für Blutzellen wichtig sind
Krebs kann lange bevor ein Tumor im Bildgebungsverfahren sichtbar wird einzelne abtrünnige Zellen in den Blutkreislauf entlassen. Diese zirkulierenden Tumorzellen sind wertvolle Hinweise für eine frühe Diagnose und maßgeschneiderte Therapien, doch sie sind selten und schwer zu handhaben, ohne den Rest des Blutes zu schädigen. Diese Arbeit untersucht, wie sorgfältig gestaltete elektrische Felder in einem kleinen Lab‑on‑a‑Chip‑Gerät diese umherwandernden Krebszellen behutsam einfangen, kurzzeitig winzige Tore in ihren Membranen öffnen und ihnen anschließend Erholung erlauben können — und das weitgehend ohne gesunde Blutzellen zu beschädigen.
Unsichtbare Kräfte nutzen, um wandernde Krebszellen zu fangen
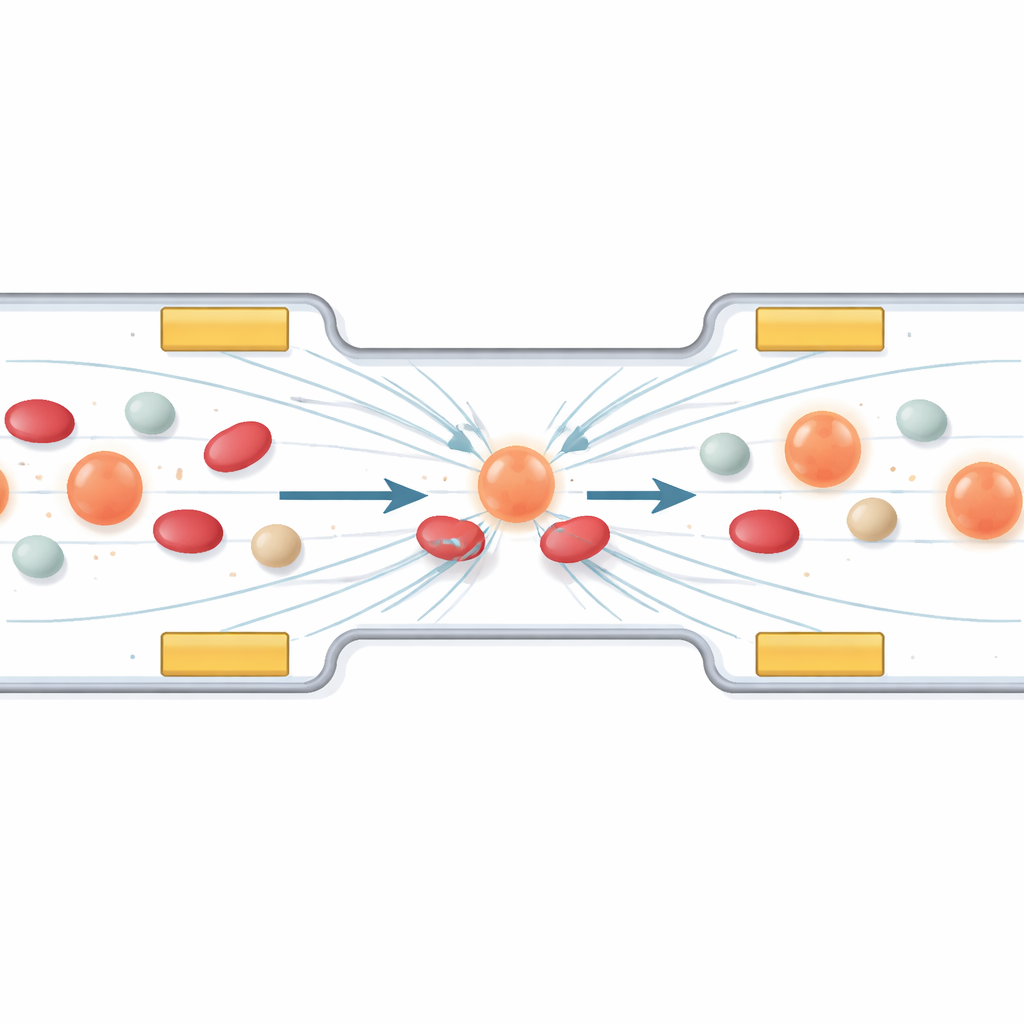
Der erste Teil der Arbeit untersucht, wie sich bestimmte Zellen mit Hilfe eines Phänomens namens Dielektrophorese steuern und sammeln lassen. Vereinfacht gesagt erfahren Zellen, wenn ein wechselndes elektrisches Feld über einem Mikrokanal angelegt wird, winzige Schub‑ und Zugkräfte, die von ihrer Größe und ihrem elektrischen Aufbau abhängen. Die Autoren entwerfen eine Anordnung winziger Elektroden, sodass zirkulierende Tumorzellen zwischen ihnen in eine stabile «Parkspur» abdriften, während kleinere oder weniger polarisierbare Blutbestandteile vorbeiziehen. Computermodelle zeigen, wie die Variation von Spannung und Frequenz das Feld formt und Zellen aus Hochfeldbereichen weglenkt, sodass sie sich in der richtigen Region für die Behandlung aufreihen. Eine Schutzschicht über den Elektroden verhindert direkten Kontakt und damit Zellschädigung.
Auf‑ und Zuschalten mikroskopischer Türen in Zellhäuten
Sobald Zellen an Ort und Stelle gehalten werden, liefert das Gerät ultrakurze elektrische Impulse, die vorübergehend Nanometer große Poren in der Außenmembran erzeugen. Die Studie entwickelt ein detailliertes mathematisches Modell dieses Prozesses für drei wichtige Blutakteure: zirkulierende Tumorzellen, weiße Blutkörperchen und Blutplättchen. Es verfolgt, wie sich die Spannung über jeder Zellmembran erhöht, wann Poren erstmals erscheinen, wie groß und zahlreich sie werden und wie schnell die Membran wieder verschließt. Durch Feinabstimmung von Feldstärke und Impulslänge identifiziert das Team Bereiche, in denen die Membran durchlässig genug wird, um Wirkstoffe oder genetisches Material aufzunehmen, dann aber ohne Zelltod heilt. Für Tumor‑ und weiße Blutkörperchen liegen effektive Feldstärken im Bereich von 1–4 Kilovolt pro Zentimeter, während die deutlich kleineren Thrombozyten etwa um den Faktor zehn stärkere Felder benötigen, um denselben Effekt zu erreichen.
Unterschiedliche Blutzellen, unterschiedliche optimale Bereiche
Das Modell zeigt, wie Zellgröße und elektrische Eigenschaften das Reaktionsverhalten jeder Zellart verändern. Größere zirkulierende Tumorzellen und weiße Blutkörperchen laden sich langsamer auf und erreichen die Spitzenmembranspannung etwa zwei Mikrosekunden nach Pulsbeginn; ihre Poren wachsen und schließen sich dann über Zeiträume von zehn Mikrosekunden bis zu Sekunden. Winzige Thrombozyten reagieren dagegen nahezu unmittelbar, mit schnellerer Porenbildung und erneutem Verschluss. Bei allen Zelltypen tritt die intensivste Wirkung auf der «hyperpolarisierten» Seite der Zelle auf, die dem einfallenden Feld zugewandt ist, wo die Kräfte konzentriert sind. Das bedeutet, dass sich durch Wahl der passenden Feldstärke für eine gegebene Zellgröße das Öffnen von Poren in Tumorzellen begünstigen lässt, während Schäden an gesunden Nachbarzellen gering bleiben — eine Grundlage für hochselektive Behandlungen.
Die Idee mit echten Zellen auf einem Chip testen
Um zu prüfen, ob die Simulationen der Realität entsprechen, bauten die Autoren einen mikrofluidischen Chip, der Fangelektroden mit einer zentralen Messzone kombiniert. Sie leiteten eine Modell‑Linie weißer Blutkörperchen (THP‑1‑Zellen) durch den Kanal und legten über einen festen Spalt zunehmende Spannungen an. Anstatt die Poren direkt zu beobachten, maßen sie, wie leicht ein Wechselstrom durch die Suspension floss. Mit zunehmendem elektrischen Feld sank der Gesamtwiderstand der Zellmischung und ihr kapazitatives Verhalten nahm ab — Kennzeichen dafür, dass die Membranen leitfähiger geworden und weniger wie intakte Isolatoren wirkten. Bei den höchsten getesteten Feldern dominierte die elektrische Antwort die Leitung durch offene Poren, was die Trends aus dem Computermodell eng widerspiegelte.
Was das für die künftige Krebsversorgung bedeuten könnte
Kurz gesagt zeigt diese Studie, dass ein kompakter Chip sowohl seltene Krebszellen aus Blut herausfiltern als auch deren Membranen auf hoch kontrollierte Weise sanft öffnen kann. Durch Anpassung von Impulsstärke und -zeit an die jeweilige Zellart kann man Zellen entweder am Leben erhalten, um sie detailliert zu analysieren und medikamentös zu testen, oder sie gezielt in irreversible Schäden treiben, um sie zu zerstören — und das bei minimierter Erwärmung und geringem Schaden für gesunde Zellen. Für ein allgemeines Publikum lautet die Kernbotschaft: Mit der richtigen «elektrischen Choreografie» lassen sich winzige Ströme in kraftvolle Werkzeuge für frühe Krebsdetektion, präzise Wirkstofffreisetzung und möglicherweise sicherere, fokussiertere Krebstherapien verwandeln.
Zitation: Sherif, S., Ghallab, Y.H. & Ismail, Y. Integrated electrical modeling of circulating tumor cells for enhanced dielectrophoretic trapping and electroporation. Sci Rep 16, 12072 (2026). https://doi.org/10.1038/s41598-026-45747-z
Schlüsselwörter: zirkulierende Tumorzellen, mikrofluidische Elektroporation, Dielektrophorese, Krebsdiagnostik, Lab-on-a-Chip