Clear Sky Science · pl
Zintegrowane modelowanie elektryczne krążących komórek nowotworowych dla ulepszonego chwytania dielektroforetycznego i elektroporacji
Dlaczego małe elektryczne impulsy mają znaczenie dla krwinek
Nowotwór może uwalniać pojedyncze złośliwe komórki do krwiobiegu na długo przed wykryciem guza w badaniu obrazowym. Te krążące komórki nowotworowe są cennymi wskazówkami dla wczesnej diagnostyki i spersonalizowanego leczenia, ale są rzadkie i trudne do wyizolowania bez uszkadzania pozostałych składników krwi. W artykule zbadano, jak odpowiednio ukształtowane pola elektryczne wewnątrz małego urządzenia lab-on-a-chip mogą delikatnie wychwytywać te wędrujące komórki nowotworowe, tymczasowo otwierać w ich błonach maleńkie bramki, a następnie pozwalać im na regenerację — wszystko to przy jednoczesnym minimalizowaniu szkód dla zdrowych komórek krwi.
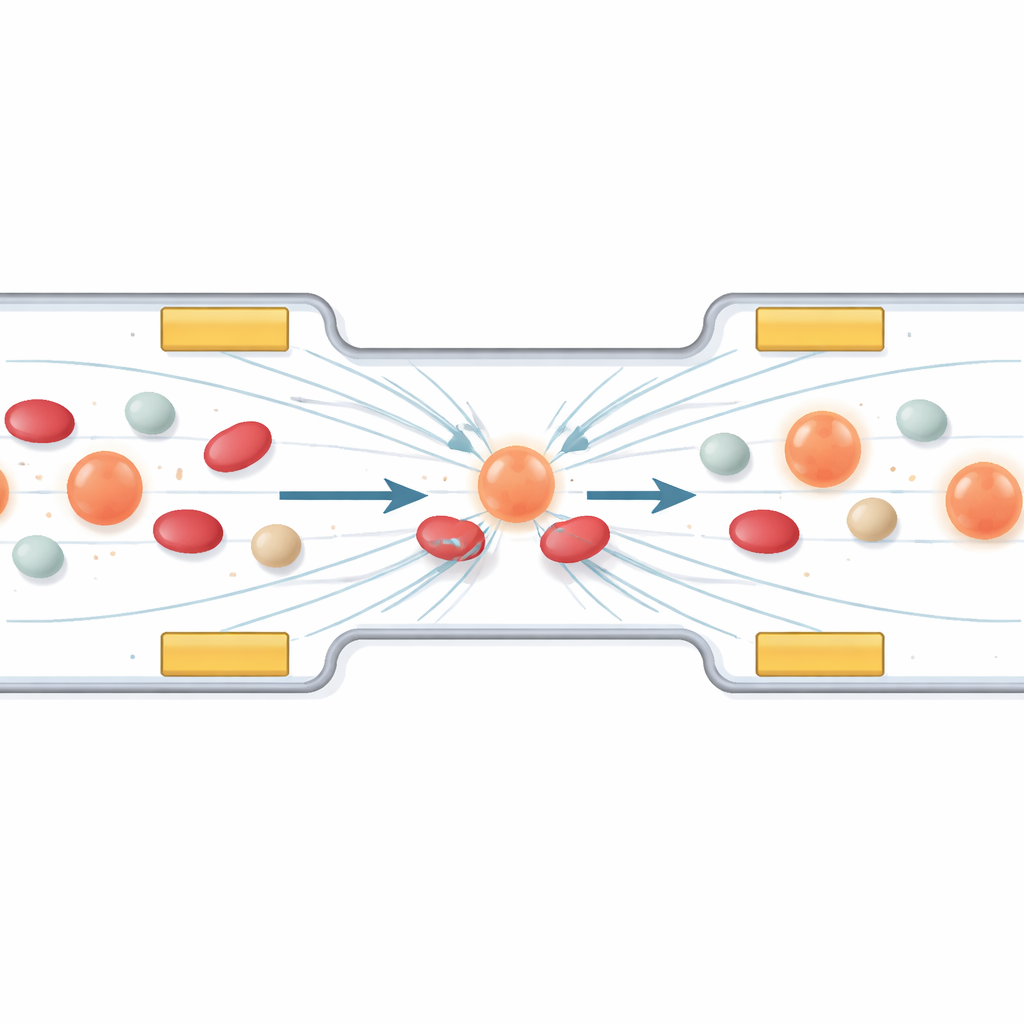
Wykorzystanie niewidzialnych sił do zatrzymywania wędrujących komórek nowotworowych
Pierwsza część pracy opisuje, jak kierować i gromadzić określone komórki za pomocą zjawiska zwanego dielektroforezą. Mówiąc prosto: gdy przez mikrokanał przyłożone zostaje przemienne pole elektryczne, komórki doświadczają drobnych pchnięć i przyciągnięć zależnych od ich rozmiaru i właściwości elektrycznych. Autorzy projektują układ miniaturowych elektrod tak, aby krążące komórki nowotworowe przemieszczaly się do stabilnego „pasa postojowego” między elektrodami, podczas gdy mniejsze lub mniej polaryzowalne składniki krwi przepływają obok. Symulacje komputerowe pokazują, jak zmiana napięcia i częstotliwości kształtuje pole, odciągając komórki z obszarów o dużym natężeniu pola i ustawiając je w odpowiednim regionie do leczenia. Warstwa ochronna na elektrodach zapobiega bezpośredniemu uszkodzeniu komórek przez kontakt.
Otwieranie i zamykanie mikroskopijnych drzwi w błonach komórkowych
Gdy komórki są utrzymane na miejscu, urządzenie dostarcza ultrakrótkie impulsy elektryczne, które tymczasowo przebijają nanometrowe pory w zewnętrznej błonie. Badanie buduje szczegółowy model matematyczny tego procesu dla trzech kluczowych graczy w krwi: krążących komórek nowotworowych, leukocytów i płytek krwi. Śledzi, jak rośnie napięcie na każdej błonie komórkowej, kiedy pojawiają się pierwsze pory, jak duże i jak liczne się stają oraz jak szybko błona się ponownie zamyka. Poprzez strojenie zarówno natężenia pola, jak i długości impulsu, zespół identyfikuje optymalne warunki, w których błona staje się wystarczająco przepuszczalna, by wpuścić leki lub materiał genetyczny, a następnie goi się bez zabijania komórki. Dla komórek nowotworowych i białych komórek krwi efektywne pola mieszczą się w zakresie 1–4 kilowoltów na centymetr, podczas gdy znacznie mniejsze płytki krwi wymagają około dziesięciokrotnie silniejszych pól, by osiągnąć ten sam efekt.
Różne typy krwinek — różne optima
Modelowanie ujawnia, jak rozmiar komórki i jej właściwości elektryczne zmieniają sposób reakcji. Większe krążące komórki nowotworowe i leukocyty ładują się wolniej i osiągają szczytowe napięcie błonowe około dwóch mikrosekund od początku impulsu; ich pory rosną, a następnie zamykają się w ciągu dziesiątek mikrosekund do sekund. Natomiast malutkie płytki krwi reagują niemal natychmiast, z szybszym powstawaniem i zamykaniem porów. Dla wszystkich typów komórek najintensywniejsze zjawiska zachodzą po stronie „hiperpolaryzowanej” komórki skierowanej ku napływającemu polu, gdzie siły się koncentrują. Oznacza to, że poprzez dobranie odpowiedniego natężenia pola do konkretnego rozmiaru komórki możliwe jest faworyzowanie otwierania porów w komórkach nowotworowych przy jednoczesnym ograniczeniu uszkodzeń sąsiednich zdrowych komórek, co tworzy podstawy dla wysoce selektywnych terapii.
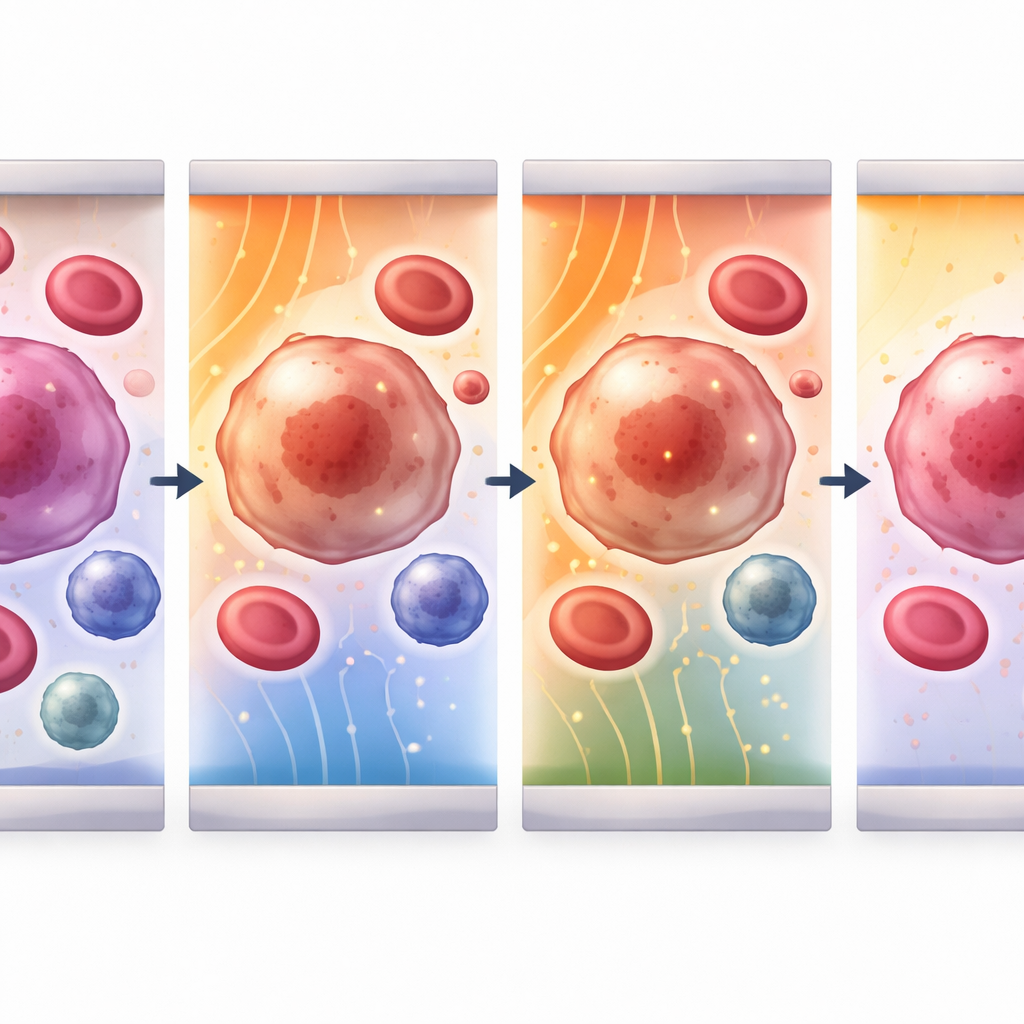
Testowanie pomysłu na prawdziwych komórkach na chipie
Aby sprawdzić zgodność symulacji z rzeczywistością, autorzy zbudowali mikrofluidyczny chip łączący elektrody chwytające z centralną strefą pomiarową. Przepuszczali przez kanał modelową linię leukocytów (komórki THP‑1) i przykładali rosnące napięcia przez stały odstęp. Zamiast obserwować pory bezpośrednio, mierzyli, jak łatwo prąd zmienny przepływa przez zawiesinę. W miarę wzrostu pola elektrycznego ogólny opór mieszaniny komórek malał, a zachowanie pojemnościowe zanikało — sygnały, że błony stały się bardziej przewodzące i mniej przypominały nienaruszone izolatory. Przy najwyższych testowanych polach odpowiedź elektryczna była zdominowana przez przewodzenie przez otwarte pory, co ściśle odzwierciedlało trendy przewidziane przez model komputerowy.
Co to może znaczyć dla przyszłej opieki onkologicznej
Mówiąc wprost, badanie pokazuje, że jeden kompaktowy chip może jednocześnie wyizolować rzadkie komórki nowotworowe z krwi i delikatnie otworzyć ich błony w wysoce kontrolowany sposób. Poprzez dopasowanie siły i czasu impulsu do każdego typu komórki, podejście to może albo utrzymać komórki przy życiu do szczegółowej analizy i testów lekowych, albo skierować je ku nieodwracalnemu uszkodzeniu w celu celowanej eliminacji, przy jednoczesnym minimalizowaniu ogrzewania i szkód dla zdrowych komórek. Dla czytelnika niebędącego specjalistą kluczowy przekaz jest taki, że przy odpowiedniej „elektrycznej choreografii” możemy przekształcić drobne prądy w potężne narzędzia do wczesnego wykrywania raka, precyzyjnego dostarczania leków i potencjalnie bezpieczniejszych, bardziej ukierunkowanych terapii przeciwnowotworowych.
Cytowanie: Sherif, S., Ghallab, Y.H. & Ismail, Y. Integrated electrical modeling of circulating tumor cells for enhanced dielectrophoretic trapping and electroporation. Sci Rep 16, 12072 (2026). https://doi.org/10.1038/s41598-026-45747-z
Słowa kluczowe: krążące komórki nowotworowe, mikrofluidyczna elektroporacja, dielektroforeza, diagnostyka raka, lab-on-a-chip