Clear Sky Science · zh
鉴定新的血液中可溶性因子H相关蛋白的结合伙伴
为何这些微小的血液蛋白很重要
我们的免疫系统依赖一种强大的化学级联反应——补体——来对抗病原体并清除细胞碎片。当这一系统失去适当控制时,会开始损伤自身组织,并促成诸如年龄相关性黄斑变性(导致失明的主要原因之一)和某些肾脏疾病等疾患。该研究关注一组鲜为人知的血液蛋白——因子H相关(FHR)蛋白,并提出一个简单却关键的问题:它们在血液中与哪些其他分子结合,这些结合如何可能将防护与有害炎症之间的平衡推向一端? 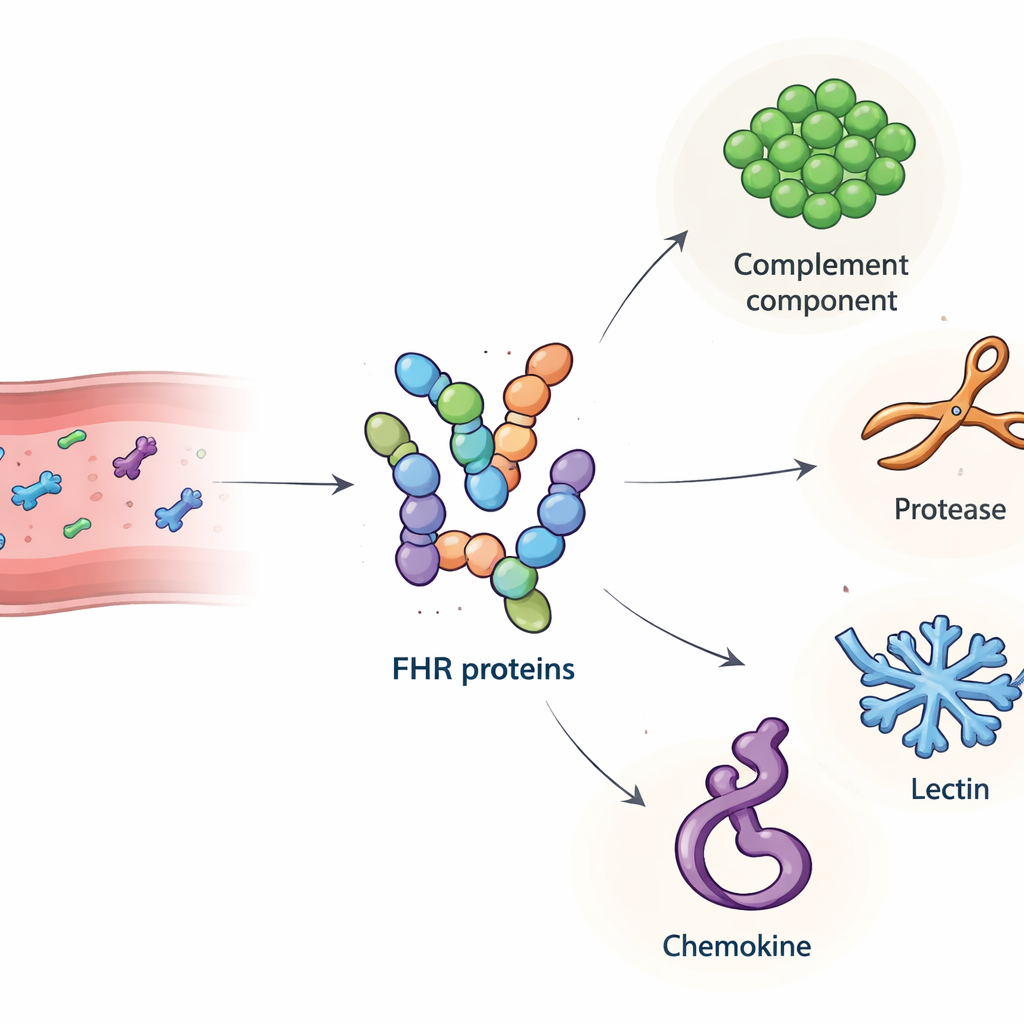
一族免疫微调器
补体因子H是对补体级联起“刹车”作用的研究较多的分子,能防止自身细胞上的过度激活。FHR蛋白是因子H的密切同源物,但缺失直接关闭补体所需的关键区段。相反,FHR可与因子H竞争结合位点,在某些情况下它们看起来更像加速器而非刹车。遗传研究将FHR水平或结构的改变与眼、肾和关节的疾病联系起来,但这些蛋白在血液中具体如何发挥作用仍不清楚。由于FHR主要在肝脏合成,随后随循环遍布全身并在组织中定位,作者推断发现其血液中可溶性结合伙伴或能揭示新的免疫调控层面。
在血流中“钓”伙伴
研究组首先在培养细胞中制备了所有主要人类FHR蛋白以及较短的因子H样蛋白1(FHL‑1)的高度纯化版本。他们确认这些实验室制备的蛋白在行为上与天然对应物一致,包括与已知靶标及肝素(一种模拟组织基质结构的糖)结合。接着,他们以每种FHR为“饵”:将其固定在微小珠子上,把珠子与人血清孵育,然后用质谱鉴定粘附的血液蛋白。此筛选得出34个候选结合伙伴。从中,研究者聚焦于四种分泌分子——具有明确免疫功能且在检测中信号清晰的蛋白:补体成分C4、切割C3b的中性粒细胞酶胰蛋白酶G(CTSG)、甘露糖结合凝集素2(MBL2),以及一种来自血小板的趋化因子血小板碱性蛋白(PPBP)。后续的板式结合实验证实这些相互作用是直接且具选择性的,不同FHR家族成员对每个伙伴呈现出不同的结合模式。 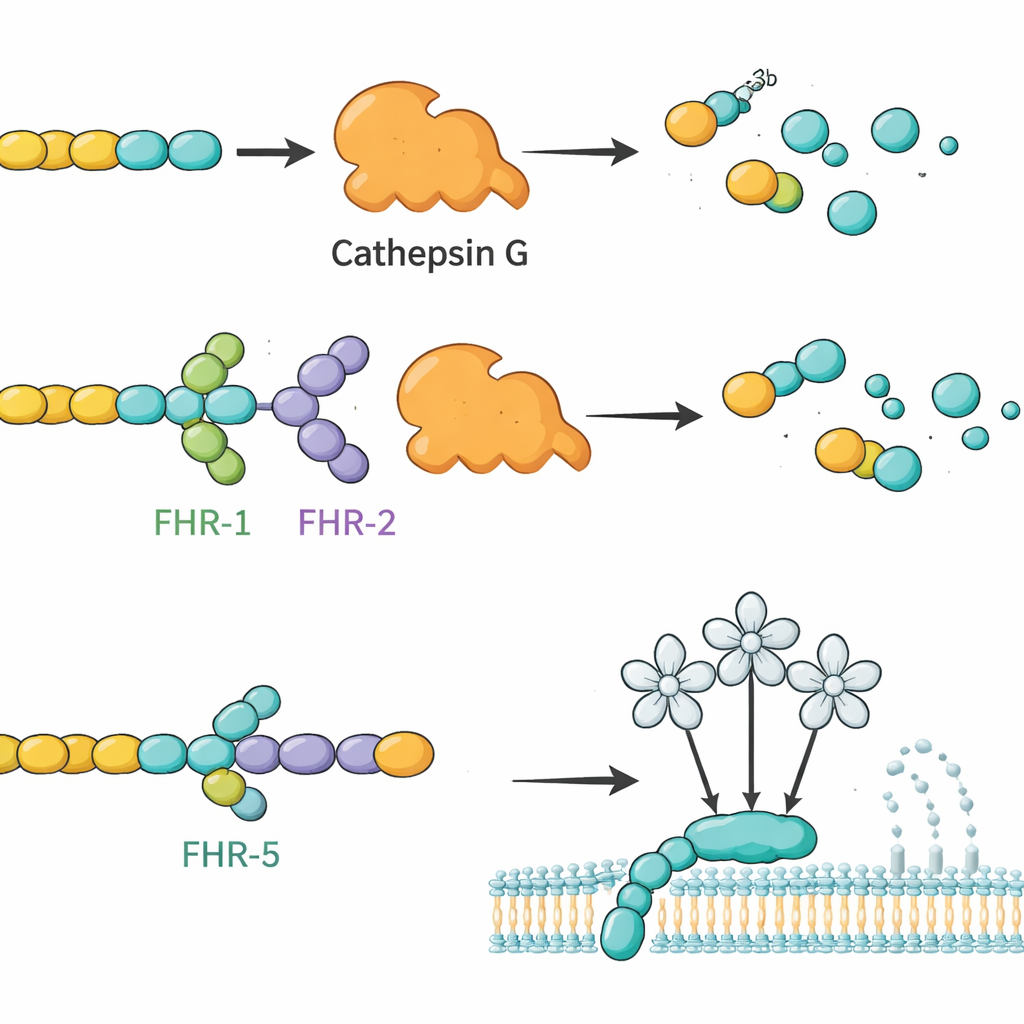
新连接如何重塑补体活性
在这些结合图谱的基础上,作者探讨FHR是否会改变这些伙伴的实际功能。他们首先关注C3b(补体的核心片段)与CTSG(已知可在无其他因子帮助下切割C3b的中性粒细胞酶)。在试管反应中,CTSG能将C3b快速降解为失活片段。当加入FHR‑1或FHR‑2时,这一降解明显减缓,提示这些FHR作为竞争性调节因子,保护C3b免受CTSG作用。相反,因子H和FHL‑1却使CTSG介导的切割更快,凸显出高度相关的蛋白可具有相反的功能效应。研究组还考察了FHR如何影响凝集素通路,该通路在MBL2识别某些糖模式时被触发。在此情形下,FHR‑5(以及在较小程度上FHL‑1和因子H)以剂量依赖的方式抑制凝集素通路活性,这与FHR‑5与MBL2结合并调节其启动级联反应的能力一致。
将免疫攻击、凝血与组织损伤联系起来
与C4和PPBP新确认的相互作用提示补体、血液凝固与炎症之间存在更广泛的串扰。C4是经典补体通路的关键早期成分,而PPBP由活化血小板释放,有助于招募白细胞。数种FHR与PPBP结合的发现表明,这些与补体相关的蛋白不仅可能在细胞表面调节化学级联,还可能与免疫细胞如何被召入发炎组织(包括视网膜和肾脏)相交叉。尽管这些结合在生物体内的确切后果尚待进一步阐明,但它们契合一种日益清晰的图景:FHR蛋白帮助在特定组织位点定位并塑造免疫反应,而非简单地作为开/关开关。
对疾病与治疗的意义
综上,这项工作扩展了FHR家族的“互作组”,揭示这些蛋白与一组参与补体激活、组织重塑与细胞招募的可溶性伙伴相互作用。对普通读者而言,关键讯息是:FHR与其他血液蛋白结合方式的微小改变,可能决定补体是默默维护组织健康,还是走向自我损伤。由于改变FHR的遗传变异与年龄相关性黄斑变性、IgA肾病及其他与补体相关的疾病有关,这些新映射出的相互作用为为何某些人更易患病提供了新的线索。从长远看,针对特定FHR配对(例如FHR‑1/FHR‑2与CTSG的相互作用或FHR‑5与MBL2的相互作用)进行干预,或能激发更精确的疗法,在不关闭自然防御的前提下恢复补体系统的平衡。
引用: Tang, J., Woerz, F., Beyer, T. et al. Identification of novel blood-borne soluble binding partners of factor H-related proteins. Sci Rep 16, 9651 (2026). https://doi.org/10.1038/s41598-026-44779-9
关键词: 补体系统, 因子H相关蛋白, 年龄相关性黄斑变性, 先天免疫, 蛋白质–蛋白质相互作用