Clear Sky Science · nl
Identificatie van nieuw in het bloed voorkomende oplosbare bindingspartners van factor H‑gerelateerde eiwitten
Waarom kleine bloedproteïnen ertoe doen
Ons immuunsysteem vertrouwt op een krachtige chemische cascade, het complement, om ziekteverwekkers te bestrijden en celafval op te ruimen. Wanneer dit systeem niet goed wordt gereguleerd, kan het onze eigen weefsels beschadigen en bijdragen aan aandoeningen zoals leeftijdsgebonden maculadegeneratie (een belangrijke oorzaak van blindheid) en bepaalde nierziekten. Deze studie onderzoekt een weinig bekend groepje bloedproteïnen, de factor H‑gerelateerde (FHR) eiwitten, en stelt een eenvoudige maar cruciale vraag: aan welke andere moleculen in het bloed hechten ze zich, en hoe kunnen die interacties het evenwicht verschuiven tussen beschermende werking en schadelijke ontsteking? 
Een familie van fijnregelaars van de immuniteit
Complement factor H is een veel bestudeerde "rem" op de complementcascade en voorkomt overactivatie op onze eigen cellen. FHR‑eiwitten zijn nauwe verwanten van factor H, maar missen de sleuteldomeinen die complement rechtstreeks uitschakelen. In plaats daarvan kunnen FHR’s concurreren met factor H om bindingsplaatsen, en in sommige situaties lijken ze meer als versnellings pedaal dan als rem te werken. Genetische studies koppelen veranderingen in FHR‑niveaus of structuur aan aandoeningen van het oog, de nieren en gewrichten, maar de precieze werkingswijzen van deze eiwitten in de bloedbaan zijn onduidelijk gebleven. Omdat FHR’s voornamelijk in de lever worden gemaakt en vervolgens door de circulatie reizen voordat ze zich in weefsels nestelen, redeneerden de auteurs dat het ontdekken van hun oplosbare bloed‑gebonden partners nieuwe lagen van immuunregulatie zou kunnen onthullen.
Vissen naar partners in de bloedbaan
Het team maakte eerst sterk gezuiverde versies van alle belangrijke menselijke FHR‑eiwitten, plus het kortere factor H‑achtige eiwit 1 (FHL‑1), in gekweekte cellen. Ze bevestigden dat deze in het laboratorium gemaakte eiwitten zich gedroegen als hun natuurlijke tegenhangers, inclusief binding aan bekende doelwitten en aan heparine, een suiker die structuren in weefselmatrices nabootst. Vervolgens gebruikten ze elk FHR als lokaas: ze immobiliseerden het op kleine bolletjes, incuberen de bolletjes met menselijk serum en gebruikten massaspectrometrie om te identificeren welke bloedproteïnen bleven plakken. Deze screening leverde 34 kandidaat‑partners op. Uit deze set richtten de onderzoekers zich op vier uitgescheiden moleculen met duidelijke immuunfuncties en heldere signalen in de test: complementcomponent C4, het enzym cathepsine G (CTSG), mannose‑bindend lectine 2 (MBL2) en een door bloedplaatjes afgeleide chemokine genaamd platelet basic protein (PPBP). Vervolg‑plaatgebaseerde bindingstesten bevestigden dat deze interacties direct en selectief zijn, waarbij verschillende FHR‑familieleden uiteenlopende bindingspatronen aan elk partner vertonen. 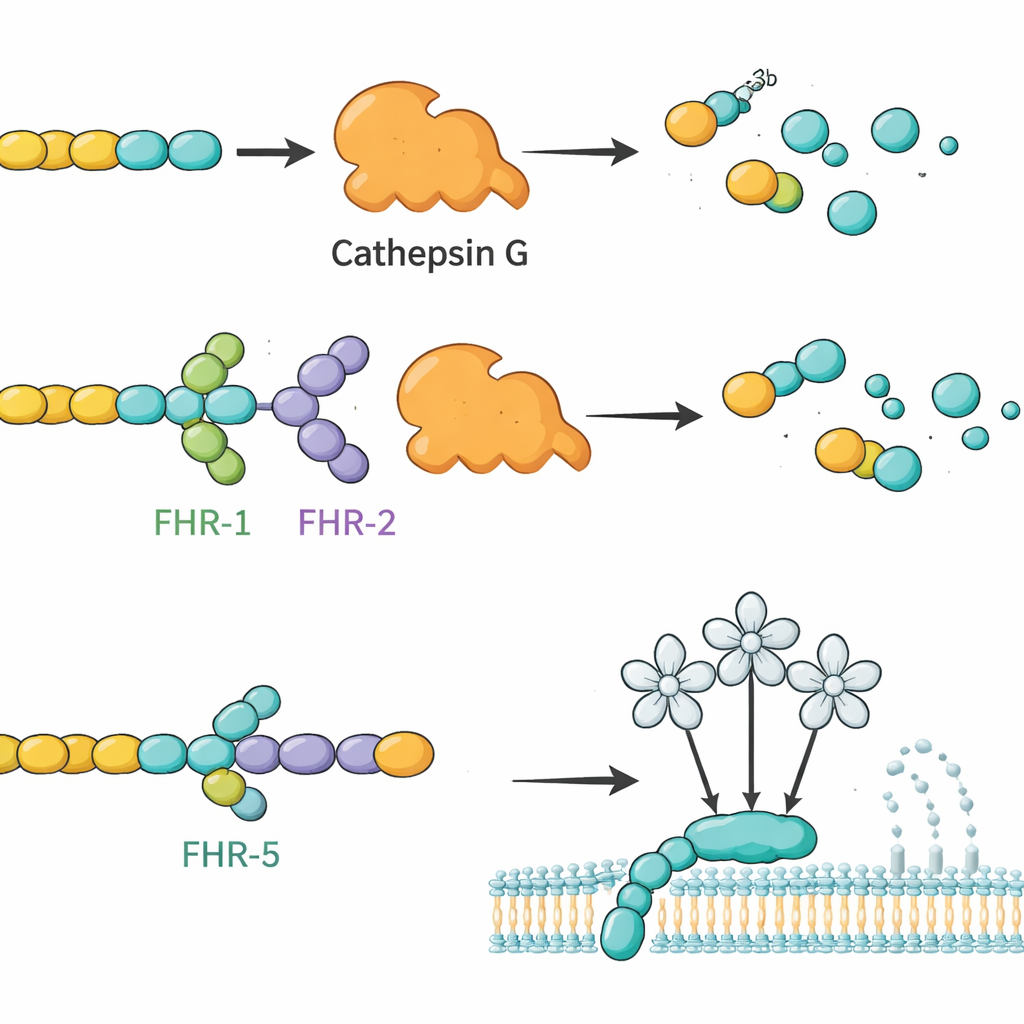
Hoe nieuwe verbindingen complementactiviteit hervormen
Op basis van deze bindingskaarten vroegen de auteurs zich af of FHR’s kunnen veranderen wat deze partners daadwerkelijk doen. Ze concentreerden zich eerst op C3b, een centraal complementfragment, en CTSG, een neutrofielenzym dat bekendstaat om het afbreken van C3b zonder hulp van andere factoren. In reageerbuisreacties degradeerde CTSG C3b gemakkelijk tot inactieve fragmenten. Toen FHR‑1 of FHR‑2 werd toegevoegd, vertraagde deze afbraak merkbaar, wat suggereert dat deze FHR’s als concurrerende regulatoren werken die C3b beschermen tegen CTSG. Daarentegen versnelden factor H en FHL‑1 de CTSG‑gedreven splitsing, wat benadrukt hoe nauwe verwanten tegenovergestelde functionele effecten kunnen hebben. De groep onderzocht ook hoe FHR’s de lectinearm van het complement beïnvloeden, die wordt geactiveerd wanneer MBL2 bepaalde suikerpatronen herkent. Hier dempte FHR‑5 (en in mindere mate FHL‑1 en factor H) de activiteit van de lectineweg in een dosisafhankelijke manier, consistent met binding van FHR‑5 aan MBL2 en het moduleren van diens vermogen om de cascade te starten.
Het verbinden van immuunaanval, stolling en weefselschade
De nieuw bevestigde interacties met C4 en PPBP wijzen op bredere kruisbesprekingen tussen complement, bloedstolling en ontsteking. C4 is een belangrijk vroeg component van de klassieke complementroute, terwijl PPBP wordt vrijgegeven door geactiveerde bloedplaatjes en helpt bij het aantrekken van witte bloedcellen. De bevinding dat meerdere FHR’s aan PPBP binden suggereert dat deze complement‑gekoppelde eiwitten niet alleen chemische cascades op celoppervlakken bijsturen, maar ook invloed hebben op hoe immuuncellen naar ontstoken weefsels worden geleid, inclusief het netvlies en de nieren. Hoewel de precieze gevolgen van deze bindingen in levende organismen nog nader moeten worden onderzocht, passen ze in een groeiend beeld waarin FHR‑eiwitten helpen immuunreacties op specifieke weefselplaatsen te positioneren en te vormen, in plaats van enkel als eenvoudige aan/uit‑schakelaars te fungeren.
Wat dit betekent voor ziekte en behandeling
Alles bij elkaar breidt dit werk het “interactoom” van de FHR‑familie uit en toont aan dat deze eiwitten een netwerk van oplosbare partners aangaan die betrokken zijn bij complementactivatie, weefselhermodellering en cellulaire rekrutering. Voor een algemeen publiek is de belangrijkste boodschap dat kleine veranderingen in hoe FHR’s aan andere bloedproteïnen binden kunnen bepalen of complement stilletjes de weefsels gezond houdt of ontspoort tot zelfbeschadiging. Omdat genetische varianten die FHR’s veranderen worden gekoppeld aan aandoeningen zoals leeftijdsgebonden maculadegeneratie, IgA‑nefropathie en andere complementgemedieerde ziekten, bieden deze nieuw in kaart gebrachte interacties nieuwe aanwijzingen waarom sommige mensen vatbaarder zijn voor dergelijke aandoeningen. Op de lange termijn kan het gericht moduleren van specifieke FHR‑partnerschappen — zoals de FHR‑1/FHR‑2 interactie met CTSG of de FHR‑5 interactie met MBL2 — aanleiding geven tot meer precieze therapieën die het evenwicht in het complementsysteem herstellen zonder onze natuurlijke afweer uit te schakelen.
Bronvermelding: Tang, J., Woerz, F., Beyer, T. et al. Identification of novel blood-borne soluble binding partners of factor H-related proteins. Sci Rep 16, 9651 (2026). https://doi.org/10.1038/s41598-026-44779-9
Trefwoorden: complementsysteem, factor H‑gerelateerde eiwitten, leeftijdsgebonden maculadegeneratie, aangeboren immuniteit, eiwit–eiwitinteracties