Clear Sky Science · ar
تحديد شركاء ربط ذائبيين جدد في الدم لبروتينات مرتبطة بالعامل H
لماذا تهم البروتينات الدقيقة في الدم
يعتمد جهازنا المناعي على سلسلة كيميائية قوية تُسمى المكمل لمكافحة الجراثيم وإزالة مخلفات الخلايا. عندما لا تتم السيطرة على هذا النظام بشكل سليم، يمكن أن يبدأ في التسبب بضرر لأنسجتنا والمساهمة في أمراض مثل الضمور البقعي المرتبط بالعمر (سبب رئيس للعمى) وبعض اضطرابات الكلى. تدرس هذه الدراسة مجموعة قليلة المعرفة من بروتينات الدم، وهي بروتينات مرتبطة بالعامل H (FHR)، وتطرح سؤالًا بسيطًا لكنه حاسمًا: بأي جزيئات أخرى في الدم ترتبط هذه البروتينات، وكيف قد تُحرّك هذه الشراكات التوازن بين الحماية الصحية والالتهاب الضار؟ 
عائلة مخصصة لضبط الاستجابة المناعية
العامل H للمكمل هو "مكبح" معروف لسلسلة المكمل، يمنع فرط النشاط على خلايانا. بروتينات FHR قريبة الصلة بالعامل H، لكنها تفتقر إلى المنطقة الأساسية التي تطفئ المكمل بشكل مباشر. بدلاً من ذلك، يمكن أن تتنافس بروتينات FHR مع العامل H على مواقع الارتباط، وفي بعض الظروف تبدو أقرب إلى دواسات تسريع منها إلى مكابح. تربط الدراسات الوراثية تغييرات في مستويات أو بنية FHR بأمراض العين والكلى والمفاصل، ومع ذلك ظلت الطرق الدقيقة التي تعمل بها هذه البروتينات في مجرى الدم غامضة. وبما أن FHRs تُنتَج بشكل رئيسي في الكبد ثم تتنقل عبر الدورة الدموية قبل الالتحام بالأنسجة، افترض المؤلفون أن اكتشاف شركائها الذائبيين في الدم قد يكشف طبقات جديدة من الضبط المناعي.
صيد الشركاء في مجرى الدم
أولاً أنتج الفريق نسخًا مُنقّاة للغاية من جميع بروتينات FHR البشرية الرئيسية، بالإضافة إلى البروتين الأقصر الشبيه بالعامل H‑1 (FHL‑1)، في خلايا مزروعة. وأكدوا أن هذه البروتينات المُصنّعة مخبريًا تتصرف مثل نظيراتها الطبيعية، بما في ذلك الارتباط بالأهداف المعروفة وبالهيبارين، وهو سكر يحاكي تركيبًا في مصفوفات الأنسجة. بعد ذلك، استخدموا كل FHR كطُعْم: ثبتوه على خرزات صغيرة، حضنوا هذه الخرزات بمصل بشري، ثم استخدموا قياس الطيف الكتلي لتحديد بروتينات الدم التي التصقت. أظهر الفحص 34 شريكًا مرشحًا. من هذه المجموعة ركز الباحثون على أربعة جزيئات مُفرَزة ذات أدوار مناعية واضحة وإشارات نقية في الاختبار: المكوّن التكميلي C4، والإنزيم الكاتيبسين G (CTSG)، والبروتين الرابط للمانوز 2 (MBL2)، وكيمياء قواطع مشتقة من الصفائح الدموية تُسمى بروتين الصفائح الأساسي (PPBP). اختبارات ارتباط لاحقة على أطباق أكدت أن هذه التفاعلات مباشرة وانتقائية، مع أن أعضاء عائلة FHR أظهروا أنماط ارتباط مميزة لكل شريك. 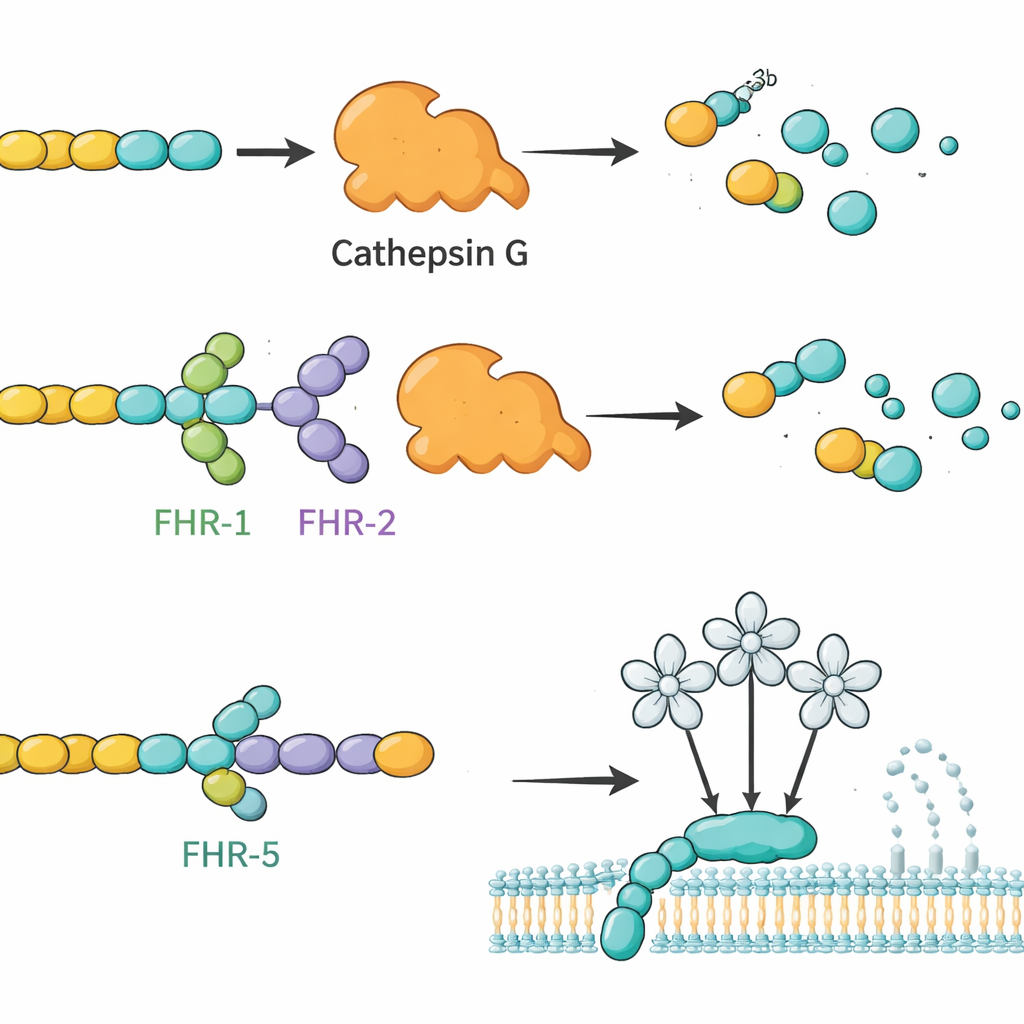
كيف تعيد الروابط الجديدة تشكيل نشاط المكمل
بناءً على خرائط الارتباط هذه، تساءل المؤلفون عما إذا كانت FHRs قادرة على تغيير ما تقوم به هذه الشركاء فعليًا. ركزوا أولًا على C3b، شظية مركزية من المكمل، وCTSG، وهو إنزيم في العدلات معروف بقص C3b دون حاجة لعوامل أخرى. في تفاعلات أنبوبية، قام CTSG بتحلل C3b بسهولة إلى قطع معطلة. عندما أضيف FHR‑1 أو FHR‑2، تباطأ هذا التحلل بشكل ملحوظ، مما يشير إلى أن هذين البروتينين يعملان كمنظِمين تنافسيين يحميان C3b من CTSG. بالمقابل، سرّع العامل H وFHL‑1 عملية قص CTSG، مما يبرز كيف أن بروتينات قريبة جدًا يمكن أن يكون لها تأثيرات وظيفية متعاكسة. كما درس الفريق كيف تؤثر FHRs على الفرع المحب للسكريات من المكمل (مسار الليكتين)، الذي يُطلق عندما يتعرف MBL2 على أنماط سكرية معينة. هنا أخمد FHR‑5 (وبدرجة أقل FHL‑1 والعامل H) نشاط مسار الليكتين بطريقة تعتمد على الجرعة، متسقًا مع ارتباط FHR‑5 بـ MBL2 وتعديله لقدرتها على بدء السلسلة.
ربط الهجوم المناعي والتخثر وتلف الأنسجة
تشير التفاعلات المؤكدة حديثًا مع C4 وPPBP إلى تداخل أوسع بين المكمل وتجلط الدم والالتهاب. يُعد C4 عنصرًا مبكرًا رئيسيًا في المسار الكلاسيكي للمكمل، في حين يُفرَز PPBP بواسطة الصفائح النشطة ويساعد في استدعاء خلايا الدم البيضاء. إن اكتشاف أن عدة FHRs ترتبط بـ PPBP يوحي بأن هذه البروتينات المرتبطة بالمكمل قد لا تضبط فقط السلاسل الكيميائية على أسطح الخلايا، بل قد تتقاطع أيضًا مع كيفية جذب الخلايا المناعية إلى الأنسجة الملتهبة، بما في ذلك الشبكية والكلى. وعلى الرغم من أن العواقب الدقيقة لهذه الارتباطات في الكائنات الحية لا تزال بحاجة إلى توضيح، إلا أنها تتسق مع صورة متنامية تُظهر أن بروتينات FHR تساعد في تموضع وتشكيل الاستجابات المناعية في مواقع نسيجية محددة، بدلًا من أن تكون مفاتيح تشغيل/إيقاف بسيطة.
ماذا يعني هذا للمرض والعلاج
باختصار، توسع هذه الدراسة "شبكة التفاعل" لعائلة FHR وتكشف أن هذه البروتينات تشترك مع شبكة من الشركاء الذائبيين المشاركين في تفعيل المكمل، وإعادة تشكيل الأنسجة، واستقطاب الخلايا. للقراء غير المتخصصين، الرسالة الرئيسية هي أن تغييرات طفيفة في كيفية ارتباط FHRs ببروتينات الدم الأخرى يمكن أن تؤثر في ما إذا كان المكمل يحافظ بهدوء على صحة الأنسجة أو ينزلق إلى تلف ذاتي. وبما أن المتغيرات الوراثية التي تغير FHR مرتبطة بحالات مثل الضمور البقعي المرتبط بالعمر، والتهاب كبيبات الكلية من نمط IgA، واضطرابات أخرى محكومة بالمكمل، فإن هذه التفاعلات المرسومة حديثًا تقدم دلائل جديدة على سبب تعرض بعض الأشخاص لمثل هذه الأمراض. على المدى الطويل، قد يلهم استهداف شراكات FHR معينة — مثل تفاعل FHR‑1/FHR‑2 مع CTSG أو تفاعل FHR‑5 مع MBL2 — علاجات أكثر دقة تستعيد التوازن في نظام المكمل دون إيقاف دفاعاتنا الطبيعية.
الاستشهاد: Tang, J., Woerz, F., Beyer, T. et al. Identification of novel blood-borne soluble binding partners of factor H-related proteins. Sci Rep 16, 9651 (2026). https://doi.org/10.1038/s41598-026-44779-9
الكلمات المفتاحية: نظام المكمل, بروتينات مرتبطة بالعامل H, الضمور البقعي المرتبط بالعمر, المناعة الفطرية, تفاعلات بروتين‑بروتين