Clear Sky Science · fr
Identification de nouveaux partenaires solubles transportés dans le sang des protéines apparentées au facteur H
Pourquoi de petites protéines sanguines comptent
Notre système immunitaire s’appuie sur une puissante cascade chimique, appelée complément, pour combattre les microbes et éliminer les débris cellulaires. Lorsque ce système n’est pas correctement contrôlé, il peut commencer à endommager nos propres tissus et contribuer à des maladies telles que la dégénérescence maculaire liée à l’âge (une cause majeure de cécité) et certains troubles rénaux. Cette étude examine un groupe peu connu de protéines sanguines, les protéines apparentées au facteur H (FHR), et pose une question simple mais cruciale : à quelles autres molécules présentes dans le sang se lient‑elles, et comment ces partenariats peuvent‑ils faire pencher la balance entre protection saine et inflammation néfaste ? 
Une famille d’ajusteurs fins du système immunitaire
Le facteur H du complément est un « frein » bien étudié de la cascade du complément, empêchant une suractivation sur nos propres cellules. Les protéines FHR sont des parentes proches du facteur H, mais elles n’ont pas la région clé qui désactive directement le complément. Au lieu de cela, les FHR peuvent entrer en compétition avec le facteur H pour des sites de liaison et, dans certains contextes, elles semblent agir davantage comme des accélérateurs que comme des freins. Des études génétiques relient des modifications des niveaux ou de la structure des FHR à des maladies de l’œil, du rein et des articulations, mais les mécanismes exacts de leur action dans le sang sont restés flous. Comme les FHR sont principalement fabriquées dans le foie puis circulent avant de se déposer dans les tissus, les auteurs ont émis l’hypothèse que découvrir leurs partenaires solubles sanguins pourrait révéler de nouveaux niveaux de régulation immune.
À la pêche aux partenaires dans le plasma
L’équipe a d’abord produit des versions hautement purifiées de tous les principaux FHR humains, ainsi que de la plus courte protéine apparentée FHL‑1, dans des cellules en culture. Ils ont confirmé que ces protéines synthétiques se comportaient comme leurs homologues naturels, y compris en se liant à des cibles connues et à l’héparine, un sucre qui mime des structures des matrices tissulaires. Ensuite, ils ont utilisé chaque FHR comme appât : l’immobiliser sur de minuscules billes, incubater les billes avec du sérum humain, puis utiliser la spectrométrie de masse pour identifier les protéines sanguines qui adhéraient. Ce criblage a révélé 34 partenaires candidats. Parmi ceux‑ci, les chercheurs se sont concentrés sur quatre molécules sécrétées ayant des rôles immunitaires clairs et des signaux nets dans le test : la composante du complément C4, l’enzyme cathepsine G (CTSG), la lectine de liaison au mannose 2 (MBL2), et une chimiokine dérivée des plaquettes appelée protéine basique plaquettaire (PPBP). Des tests de liaison supplémentaires sur plaque ont confirmé que ces interactions sont directes et sélectives, chaque membre de la famille FHR montrant des profils de liaison distincts avec chaque partenaire. 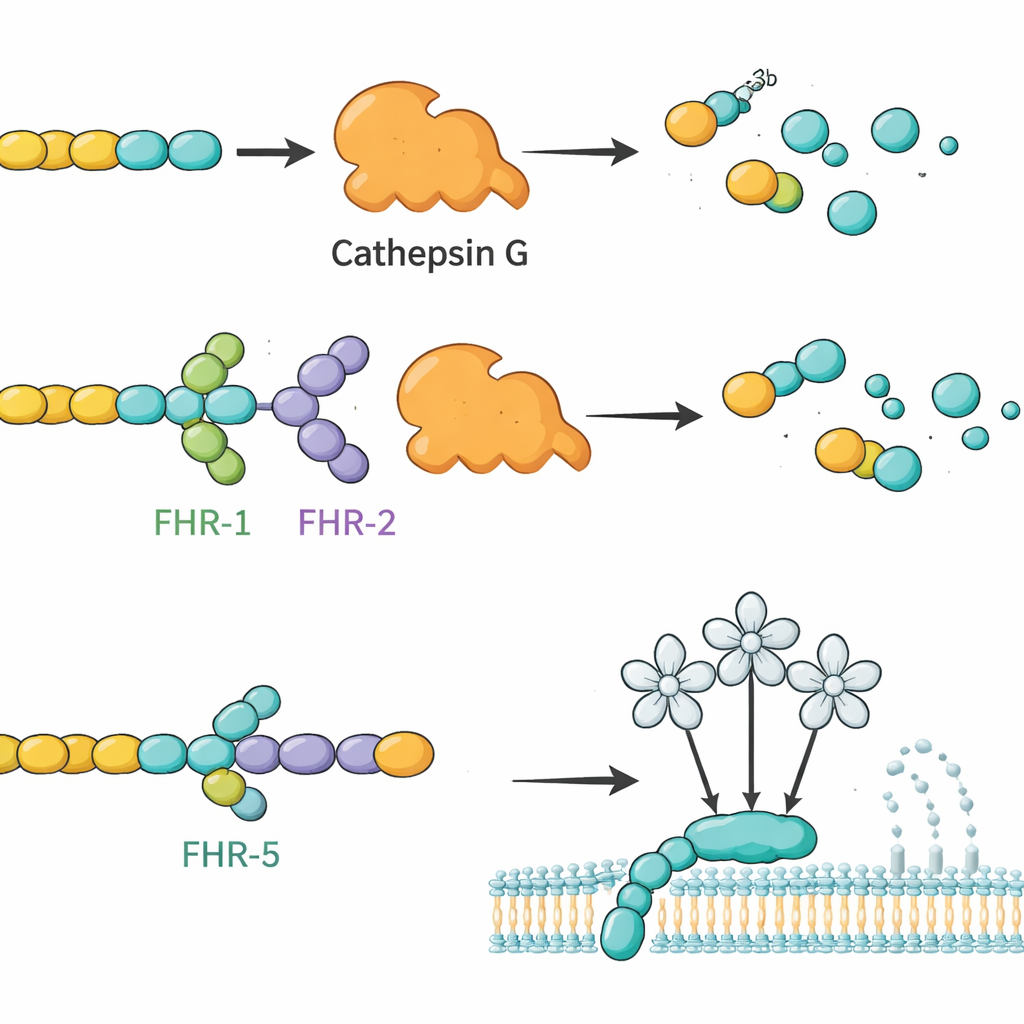
Comment ces nouvelles liaisons modifient l’activité du complément
En s’appuyant sur ces cartographies de liaison, les auteurs ont cherché à savoir si les FHR pouvaient modifier la fonction de ces partenaires. Ils se sont d’abord concentrés sur C3b, un fragment central du complément, et CTSG, une enzyme des neutrophiles connue pour couper C3b sans l’aide d’autres facteurs. Dans des réactions in vitro, CTSG dégradait facilement C3b en fragments inactifs. Lorsque FHR‑1 ou FHR‑2 était ajouté, cette dégradation ralentissait nettement, ce qui suggère que ces FHR agissent comme des régulateurs compétitifs protégeant C3b de CTSG. En revanche, le facteur H et FHL‑1 augmentaient la vitesse de clivage entraînée par CTSG, soulignant comment des protéines étroitement apparentées peuvent avoir des effets fonctionnels opposés. Le groupe a également exploré comment les FHR influencent le bras lectine du complément, déclenché lorsque MBL2 reconnaît certaines structures sucrées. Ici, FHR‑5 (et dans une moindre mesure FHL‑1 et le facteur H) a atténué l’activité de la voie lectine de façon dépendante de la dose, cohérent avec la liaison de FHR‑5 à MBL2 et la modulation de sa capacité à initier la cascade.
Relier attaque immune, coagulation et dommages tissulaires
Les interactions nouvellement confirmées avec C4 et PPBP suggèrent un dialogue plus large entre complément, coagulation sanguine et inflammation. C4 est un composant clé précoce de la voie classique du complément, tandis que PPBP est libéré par les plaquettes activées et contribue à recruter les globules blancs. Le fait que plusieurs FHR se lient à PPBP suggère que ces protéines liées au complément peuvent non seulement ajuster des cascades chimiques à la surface des cellules, mais aussi interférer avec la manière dont les cellules immunitaires sont attirées vers les tissus enflammés, y compris la rétine et les reins. Bien que les conséquences exactes de ces liaisons dans les organismes vivants restent à élucider, elles s’inscrivent dans une image de plus en plus nette où les protéines FHR aident à positionner et façonner les réactions immunitaires à des sites tissulaires spécifiques, plutôt que d’agir comme de simples interrupteurs marche/arrêt.
Ce que cela signifie pour la maladie et le traitement
Globalement, ce travail élargit l’« interactome » de la famille FHR et révèle que ces protéines engagent un réseau de partenaires solubles impliqués dans l’activation du complément, le remodelage tissulaire et le recrutement cellulaire. Pour un public non spécialiste, le message clé est que de petits changements dans la manière dont les FHR se lient à d’autres protéines sanguines peuvent influencer le fait que le complément maintienne discrètement la santé tissulaire ou dérive vers l’autodestruction. Étant donné que des variants génétiques modifiant les FHR sont associés à des affections comme la dégénérescence maculaire liée à l’âge, la néphropathie à IgA et d’autres troubles médiés par le complément, ces interactions récemment cartographiées fournissent de nouveaux indices expliquant pourquoi certaines personnes sont plus vulnérables à ces maladies. À long terme, cibler des partenariats FHR spécifiques — comme l’interaction FHR‑1/FHR‑2 avec CTSG ou l’interaction FHR‑5 avec MBL2 — pourrait inspirer des thérapies plus précises visant à rétablir l’équilibre du système du complément sans neutraliser nos défenses naturelles.
Citation: Tang, J., Woerz, F., Beyer, T. et al. Identification of novel blood-borne soluble binding partners of factor H-related proteins. Sci Rep 16, 9651 (2026). https://doi.org/10.1038/s41598-026-44779-9
Mots-clés: système du complément, protéines apparentées au facteur H, dégénérescence maculaire liée à l'âge, immunité innée, interactions protéine–protéine