Clear Sky Science · pt
Identificação de novos parceiros solúveis transportados no sangue das proteínas relacionadas ao fator H
Por que pequenas proteínas no sangue importam
Nosso sistema imunológico depende de uma cascata química poderosa, chamada complemento, para combater germes e eliminar detritos celulares. Quando esse sistema não é bem controlado, pode começar a danificar nossos próprios tecidos e contribuir para doenças como a degeneração macular relacionada à idade (uma das principais causas de cegueira) e certos distúrbios renais. Este estudo examina um grupo pouco conhecido de proteínas sanguíneas, as proteínas relacionadas ao fator H (FHR), e faz uma pergunta simples, porém crucial: a quais outras moléculas no sangue elas se ligam, e como essas parcerias podem inclinar a balança entre proteção saudável e inflamação prejudicial? 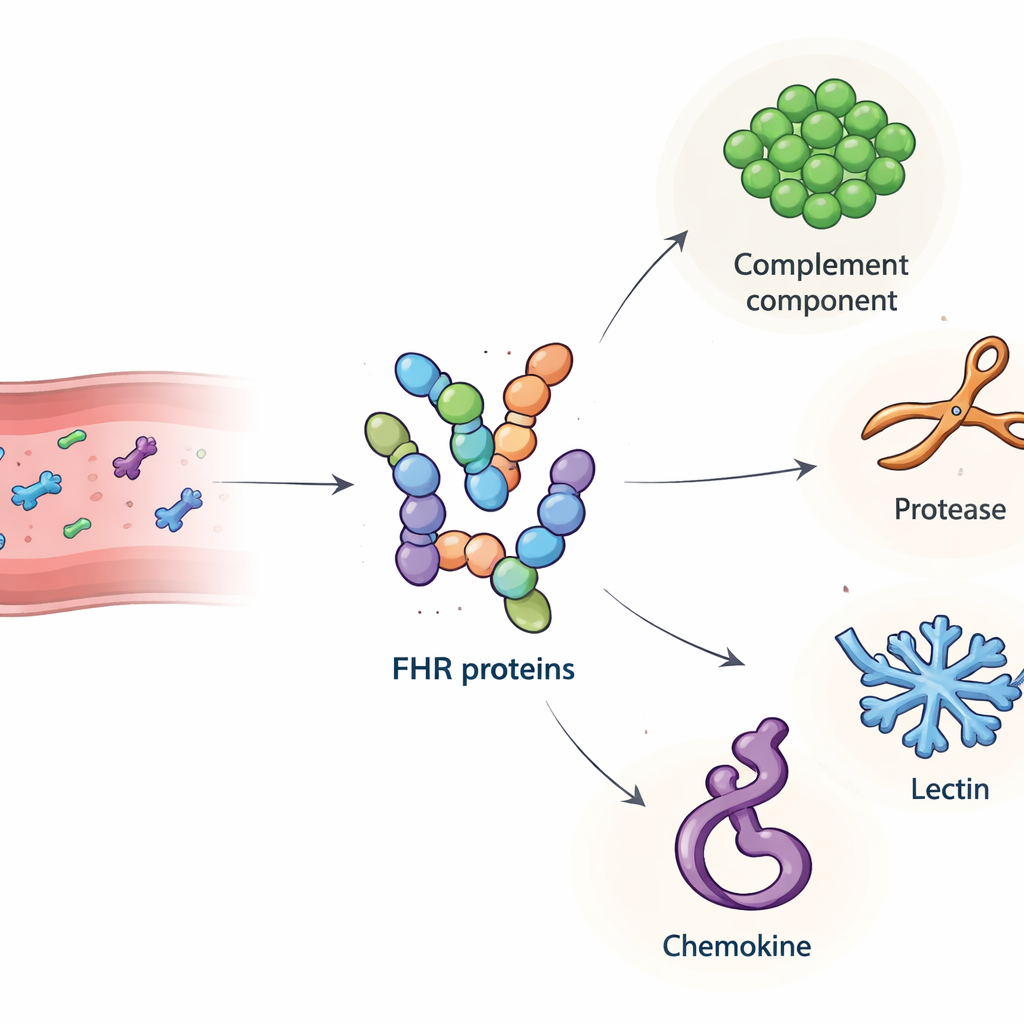
Uma família de reguladores finos do sistema imune
O fator H do complemento é um “freio” bem estudado da cascata do complemento, prevenindo a ativação excessiva em nossas próprias células. As proteínas FHR são parentes próximas do fator H, mas carecem da região chave que desliga diretamente o complemento. Em vez disso, as FHRs podem competir com o fator H por locais de ligação e, em alguns contextos, parecem atuar mais como aceleradores do que como freios. Estudos genéticos ligam alterações nos níveis ou na estrutura das FHRs a doenças dos olhos, rins e articulações, mas as formas exatas como essas proteínas atuam na corrente sanguínea permaneceram obscuras. Como as FHRs são produzidas principalmente no fígado e depois circulam pelo sangue antes de se estabelecerem nos tecidos, os autores raciocinaram que descobrir seus parceiros solúveis no sangue poderia revelar novas camadas de controle imune.
Pescando parceiros na corrente sanguínea
A equipe primeiro produziu versões altamente purificadas de todas as principais proteínas FHR humanas, além da proteína FHL‑1, uma forma mais curta semelhante ao fator H, em células cultivadas. Eles confirmaram que essas proteínas feitas em laboratório se comportavam como as naturais, incluindo a ligação a alvos conhecidos e à heparina, um açúcar que imita estruturas nas matrizes teciduais. Em seguida, usaram cada FHR como isca: imobilizando-a em pequenas esferas, incubando as esferas com soro humano e depois usando espectrometria de massa para identificar quais proteínas sanguíneas ficaram presas. Essa triagem revelou 34 parceiros candidatos. Dentre eles, os pesquisadores focaram em quatro moléculas secretadas com papéis claros no sistema imune e sinais nítidos no ensaio: o componente do complemento C4, a enzima catepsina G (CTSG), a lectina ligante de manose 2 (MBL2) e uma quimiocina derivada de plaquetas chamada proteína básica de plaquetas (PPBP). Testes subsequentes em placas confirmaram que essas interações são diretas e seletivas, com diferentes membros da família FHR exibindo padrões de ligação distintos para cada parceiro. 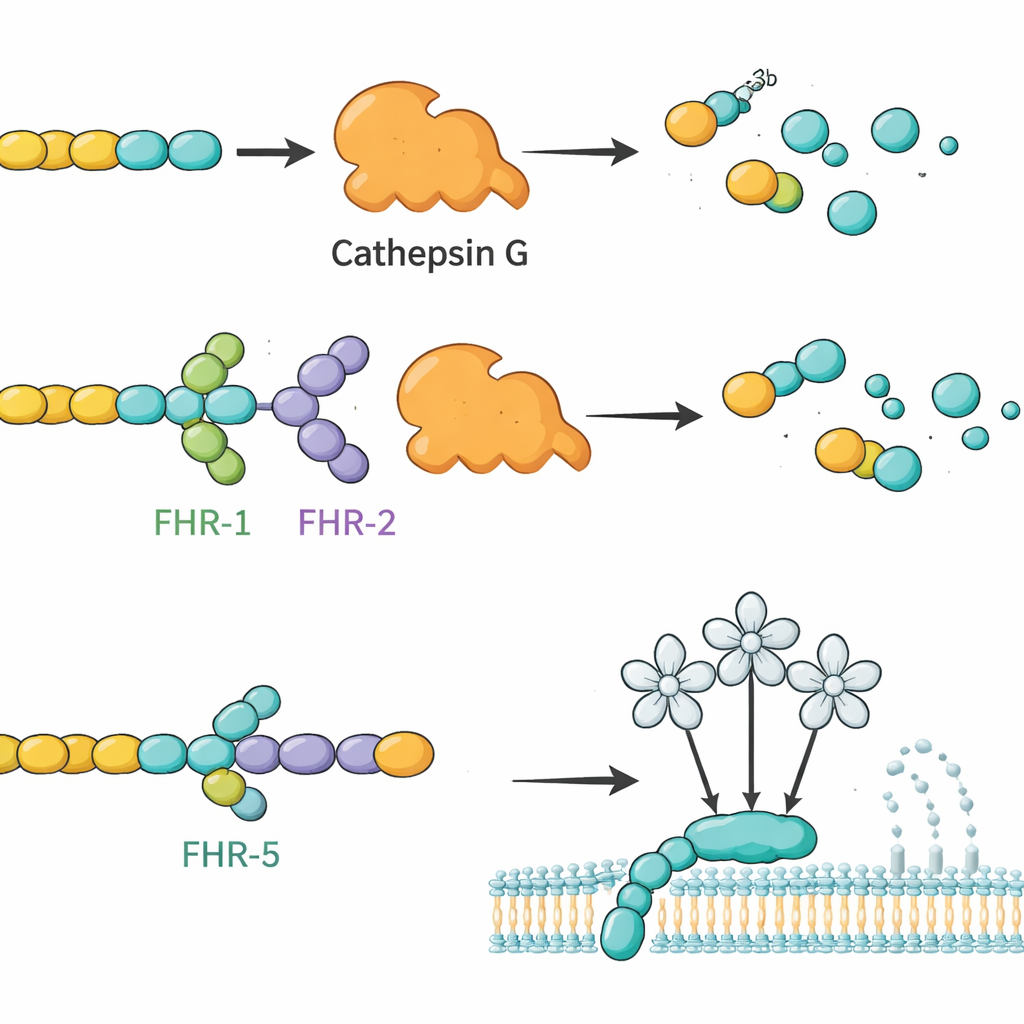
Como novos vínculos remodelam a atividade do complemento
Com base nesses mapas de ligação, os autores investigaram se as FHRs poderiam alterar o que esses parceiros realmente fazem. Eles se concentraram primeiro no C3b, um fragmento central do complemento, e na CTSG, uma enzima de neutrófilo conhecida por clivar o C3b sem ajuda de outros fatores. Em reações de tubo de ensaio, a CTSG degradou prontamente o C3b em fragmentos inativos. Quando FHR‑1 ou FHR‑2 foram adicionados, essa degradação diminuiu visivelmente, sugerindo que essas FHRs atuam como reguladores competitivos que protegem o C3b da CTSG. Em contraste, o fator H e a FHL‑1 aceleraram a clivagem dirigida pela CTSG, ressaltando como proteínas intimamente relacionadas podem ter efeitos funcionais opostos. O grupo também investigou como as FHRs influenciam o braço lecito do complemento, que é desencadeado quando a MBL2 reconhece certos padrões de açúcar. Nesse caso, a FHR‑5 (e, em menor grau, a FHL‑1 e o fator H) atenuou a atividade da via lectina de maneira dependente da dose, consistente com a ligação da FHR‑5 à MBL2 e a modulação da sua capacidade de iniciar a cascata.
Conectando ataque imune, coagulação e dano tecidual
As interações recém-confirmadas com C4 e PPBP sugerem um diálogo mais amplo entre complemento, coagulação sanguínea e inflamação. O C4 é um componente inicial chave da via clássica do complemento, enquanto a PPBP é liberada por plaquetas ativadas e ajuda a recrutar leucócitos. A descoberta de que várias FHRs se ligam à PPBP sugere que essas proteínas ligadas ao complemento podem não apenas ajustar as cascatas químicas na superfície celular, mas também interseccionar com a forma como células imunes são atraídas para tecidos inflamados, incluindo a retina e os rins. Embora as consequências exatas dessas ligações em organismos vivos ainda precisem ser esclarecidas, elas se encaixam em um quadro crescente no qual as proteínas FHR ajudam a posicionar e moldar reações imunes em locais teciduais específicos, em vez de atuar como simples interruptores liga/desliga.
O que isso significa para doença e tratamento
Em conjunto, este trabalho amplia o “interatome” da família FHR e revela que essas proteínas se engajam em uma rede de parceiros solúveis envolvidos na ativação do complemento, remodelamento tecidual e recrutamento celular. Para um público leigo, a mensagem principal é que pequenas mudanças em como as FHRs se ligam a outras proteínas sanguíneas podem influenciar se o complemento mantém silenciosamente a saúde tecidual ou se transforma em dano autoinduzido. Como variantes genéticas que alteram as FHRs estão associadas a condições como degeneração macular relacionada à idade, nefropatia por IgA e outros distúrbios mediados por complemento, essas interações recentemente mapeadas oferecem pistas novas sobre por que algumas pessoas são mais vulneráveis a essas doenças. A longo prazo, direcionar parcerias FHR específicas — como a interação FHR‑1/FHR‑2 com a CTSG ou a interação da FHR‑5 com a MBL2 — pode inspirar terapias mais precisas que restaurem o equilíbrio do sistema de complemento sem desligar nossas defesas naturais.
Citação: Tang, J., Woerz, F., Beyer, T. et al. Identification of novel blood-borne soluble binding partners of factor H-related proteins. Sci Rep 16, 9651 (2026). https://doi.org/10.1038/s41598-026-44779-9
Palavras-chave: sistema complemento, proteínas relacionadas ao fator H, degeneração macular associada à idade, imunidade inata, interações proteína–proteína