Clear Sky Science · ru
Идентификация новых растворимых кровяных партнеров связывания белков, связанных с фактором H
Почему важны крошечные белки крови
Наша иммунная система опирается на мощную химическую каскаду, называемую комплементом, чтобы бороться с микробами и убирать клеточный мусор. Если эта система некорректно контролируется, она может начать повреждать собственные ткани и способствовать таким заболеваниям, как возрастная макулярная дегенерация (ведущая причина слепоты) и некоторые заболевания почек. В этом исследовании рассматривается малоизученная группа кровяных белков — белки, связанные с фактором H (FHR) — и задается простым, но важным вопросом: за что именно в крови они цепляются и как эти партнерства могут сдвинуть равновесие между защитой и вредным воспалением? 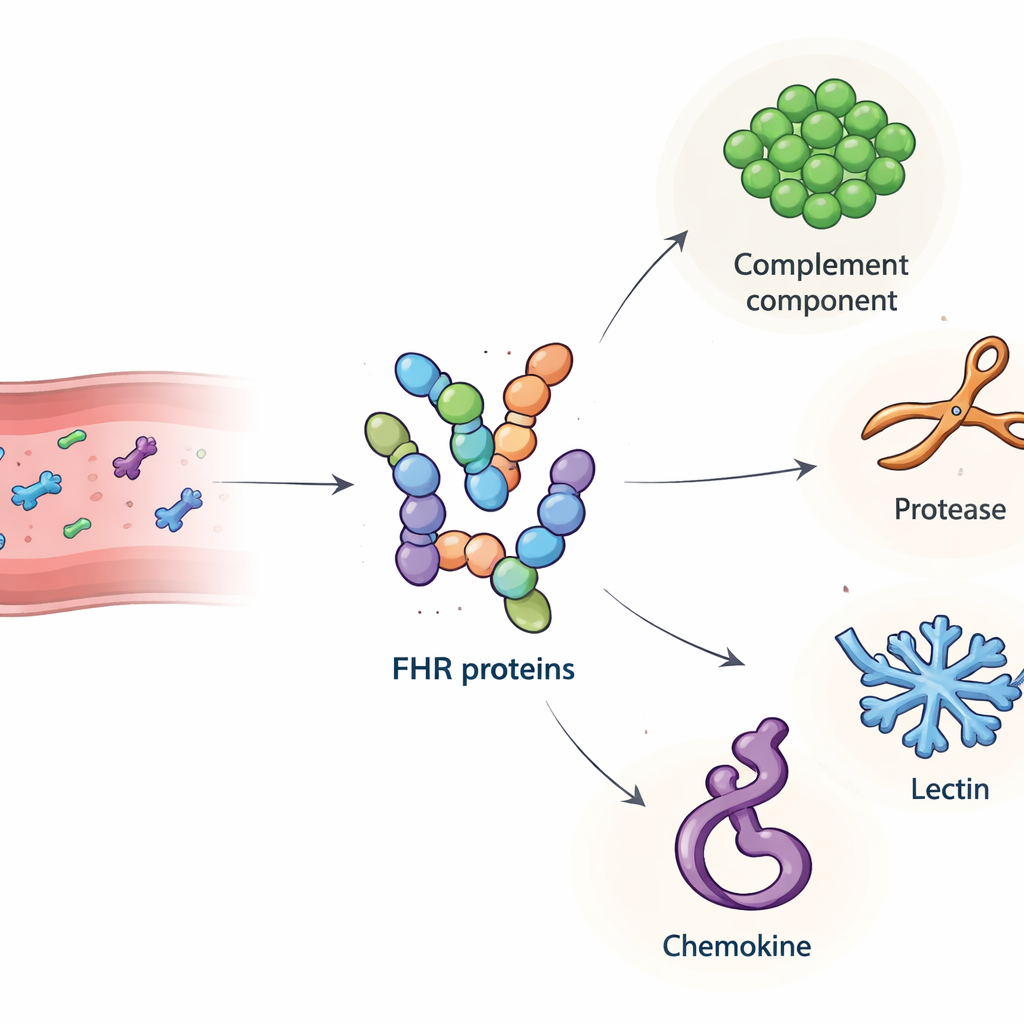
Семейство тонкой настройки иммунитета
Комплемент-фактор H — хорошо изученный «тормоз» каскада комплемента, предотвращающий его чрезмерную активацию на собственных клетках. Белки FHR — близкие родственники фактора H, но им не хватает ключевого участка, который напрямую выключает комплемент. Вместо этого FHR могут конкурировать с фактором H за сайты связывания и в некоторых условиях действовать скорее как ускорители, чем тормоза. Генетические исследования связывают изменения в уровнях или структуре FHR с заболеваниями глаз, почек и суставов, однако точные механизмы их работы в кровотоке оставались неясными. Поскольку FHR в основном синтезируются в печени, затем циркулируют в крови и оседают в тканях, авторы предположили, что выявление их растворимых кровяных партнеров может открыть новые уровни контроля иммунитета.
Поиск партнеров в кровотоке
Группа сначала получила высокоочищенные версии всех основных человеческих белков FHR, а также более короткого фактора H‑похожего белка 1 (FHL‑1) в культурах клеток. Они подтвердили, что эти лабораторно произведенные белки ведут себя как естественные аналоги, включая связывание с известными мишенями и с гепарином — сахаром, имитирующим структуры в тканевых матриксах. Затем они использовали каждый FHR как наживку: закрепляли его на крошечных бусинах, инкубировали бусины с человеческой сывороткой и с помощью масс‑спектрометрии идентифицировали, какие кровяные белки прилипали. Этот скрининг выявил 34 кандидата. Из них исследователи сосредоточились на четырех секретируемых молекулах с очевидными иммунными ролями и четкими сигналами в анализе: компоненте комплемента C4, ферменте катепсине G (CTSG), маннозосвязывающем лектине 2 (MBL2) и тромбоцитарном хемокине, называемом основным тромбоцитарным белком (PPBP). Последующие планшетные тесты связывания подтвердили, что эти взаимодействия прямые и селективные, при этом разные члены семейства FHR демонстрировали отличительные шаблоны связывания с каждым из партнеров. 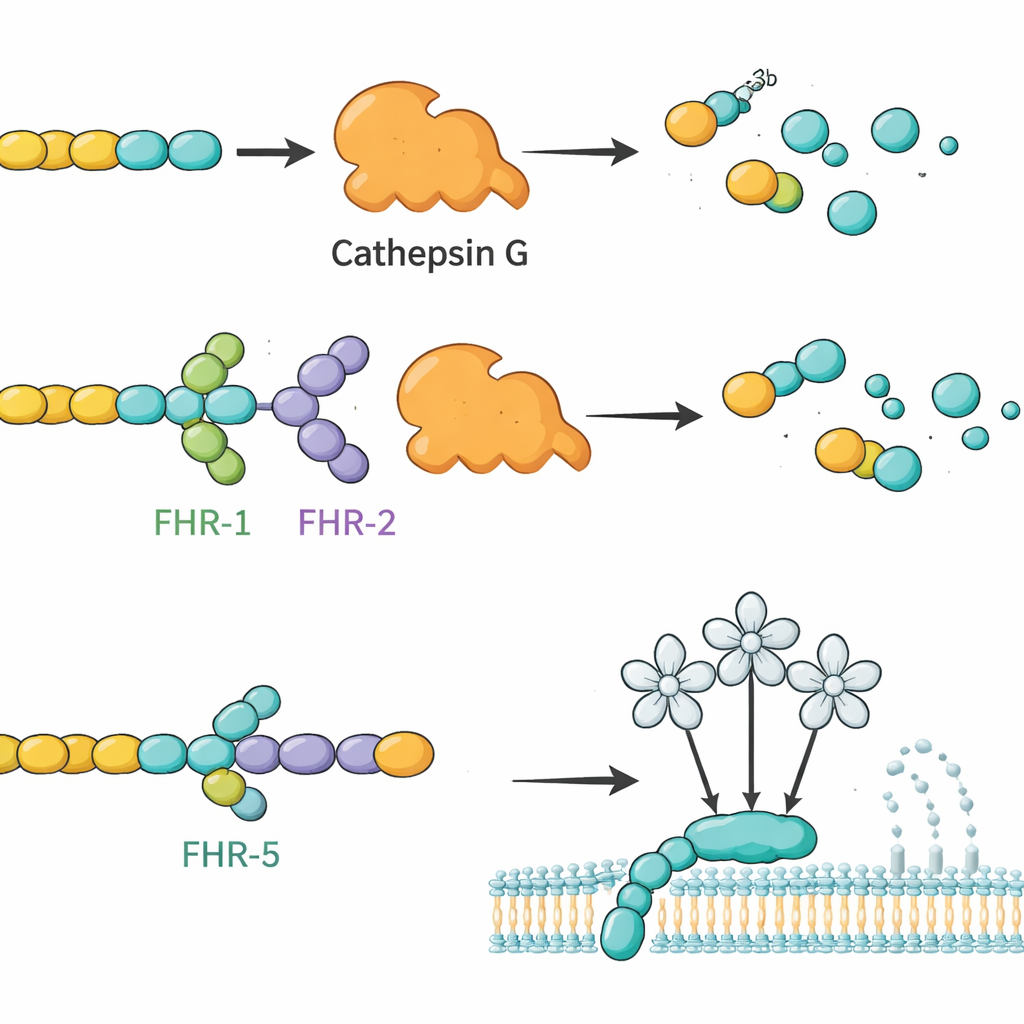
Как новые связи меняют активность комплемента
Опираясь на эти карты связываний, авторы проверили, могут ли FHR менять функции этих партнеров. Они сначала сосредоточились на C3b — центральном фрагменте комплемента — и CTSG, нейтрофильном ферменте, известном тем, что расщепляет C3b без участия других факторов. В пробирочных реакциях CTSG охотно разрушал C3b до неактивных фрагментов. При добавлении FHR‑1 или FHR‑2 это разрушение заметно замедлялось, что указывает на то, что эти FHR действуют как конкурентные регуляторы, защищающие C3b от CTSG. Напротив, фактор H и FHL‑1 ускоряли CTSG‑опосредованное расщепление, подчеркивая, как близкородственные белки могут оказывать противоположные функциональные эффекты. Группа также изучила, как FHR влияют на лектиновую ветвь комплемента, которая запускается, когда MBL2 распознает определенные сахарные узоры. Здесь FHR‑5 (и в меньшей степени FHL‑1 и фактор H) ослаблял активность лектинового пути в дозозависимом режиме, что согласуется с связыванием FHR‑5 с MBL2 и модифицирующим влиянием на его способность запускать каскад.
Связь между иммунной атакой, свертыванием и повреждением тканей
Недавно подтвержденные взаимодействия с C4 и PPBP наводят на мысль о более широкой перекрестной связи между комплементом, свертыванием крови и воспалением. C4 — ключевой ранний компонент классического пути комплемента, тогда как PPBP выделяется активированными тромбоцитами и помогает привлекать лейкоциты. Открытие того, что несколько FHR связываются с PPBP, предполагает, что эти связанные с комплементом белки могут не только настраивать химические каскады на поверхностях клеток, но и пересекаться с тем, как иммунные клетки привлекаются в воспаленные ткани, включая сетчатку и почки. Хотя точные последствия этих связей в живых организмах еще предстоит выяснить, они вписываются в растущую картину, согласно которой FHR белки помогают позиционировать и формировать иммунные реакции в конкретных тканевых участках, а не действуют как простые выключатели включения/выключения.
Что это значит для болезни и терапии
В сумме эта работа расширяет «взаимодействие» семейства FHR и показывает, что эти белки вступают в сеть растворимых партнеров, вовлеченных в активацию комплемента, ремоделирование тканей и привлечение клеток. Для неспециализированной аудитории ключевой посыл таков: небольшие изменения в том, как FHR связываются с другими белками крови, могут определять, будет ли комплемент молча поддерживать гомеостаз тканей или же перерастет в самоповреждение. Поскольку генетические варианты, изменяющие FHR, связаны с такими состояниями, как возрастная макулярная дегенерация, IgA‑нефропатия и другие заболевания, опосредованные комплементом, эти недавно нанесенные на карту взаимодействия дают новые подсказки, почему одни люди более уязвимы. В долгосрочной перспективе таргетирование конкретных партнерств FHR — например взаимодействия FHR‑1/FHR‑2 с CTSG или взаимодействия FHR‑5 с MBL2 — могло бы вдохновить создание более точных терапий, восстанавливающих баланс системы комплемента, не подавляя при этом наши естественные защитные механизмы.
Цитирование: Tang, J., Woerz, F., Beyer, T. et al. Identification of novel blood-borne soluble binding partners of factor H-related proteins. Sci Rep 16, 9651 (2026). https://doi.org/10.1038/s41598-026-44779-9
Ключевые слова: система комплемента, белки, связанные с фактором H, макулярная дегенерация, связанная с возрастом, врожденный иммунитет, белок–белковые взаимодействия