Clear Sky Science · it
Identificazione di nuovi partner solubili ematici delle proteine correlate a fattore H
Perché contano le piccole proteine del sangue
Il nostro sistema immunitario si affida a una potente cascata chimica, chiamata complemento, per combattere i germi e rimuovere i detriti cellulari. Quando questo sistema non è adeguatamente regolato, può iniziare a danneggiare i tessuti e contribuire a malattie come la degenerazione maculare legata all’età (una causa principale di cecità) e alcuni disturbi renali. Questo studio esamina un gruppo poco noto di proteine plasmatiche, le proteine correlate a fattore H (FHR), e pone una domanda semplice ma cruciale: a quali altre molecole presenti nel sangue si legano e in che modo queste interazioni possono spostare l’equilibrio tra protezione sana e infiammazione dannosa? 
Una famiglia che affina l’immunità
Il fattore H del complemento è un “freno” ben studiato della cascata del complemento, che previene la sovra‑attivazione sulle nostre cellule. Le proteine FHR sono strette parenti del fattore H, ma non possiedono la regione chiave che spegne direttamente il complemento. Invece, le FHR possono competere con il fattore H per i siti di legame e, in alcuni contesti, sembrano comportarsi più come acceleratori che come freni. Studi genetici collegano variazioni nei livelli o nella struttura delle FHR a malattie dell’occhio, del rene e delle articolazioni, tuttavia i meccanismi esatti con cui queste proteine agiscono nel sangue sono rimasti poco chiari. Poiché le FHR sono prodotte principalmente nel fegato e poi circolano prima di depositarsi nei tessuti, gli autori hanno ipotizzato che scoprire i loro partner solubili ematici potesse rivelare nuovi livelli di controllo immunitario.
Alla ricerca di partner nella circolazione
Il team ha prima prodotto versioni altamente purificate di tutte le principali FHR umane, più la forma più corta simile al fattore H (FHL‑1), in cellule coltivate. Hanno confermato che queste proteine prodotte in laboratorio si comportavano come i loro corrispettivi naturali, incluso il legame a bersagli noti e all’eparina, uno zucchero che imita strutture nelle matrici tissutali. Successivamente, hanno usato ogni FHR come esca: immobilizzandola su piccole perle, incubando le perle con siero umano e poi impiegando la spettrometria di massa per identificare quali proteine del sangue vi si attaccavano. Questo screening ha evidenziato 34 potenziali partner. Tra questi, i ricercatori si sono concentrati su quattro molecole secrete con ruoli immunitari chiari e segnali netti nell’analisi: la componente del complemento C4, l’enzima cathepsin G (CTSG), la lectina legante il mannoso 2 (MBL2) e una chemochina derivata dalle piastrine chiamata platelet basic protein (PPBP). Test successivi su piastre hanno confermato che queste interazioni sono dirette e selettive, con diversi membri della famiglia FHR che mostrano pattern di legame distinti per ciascun partner. 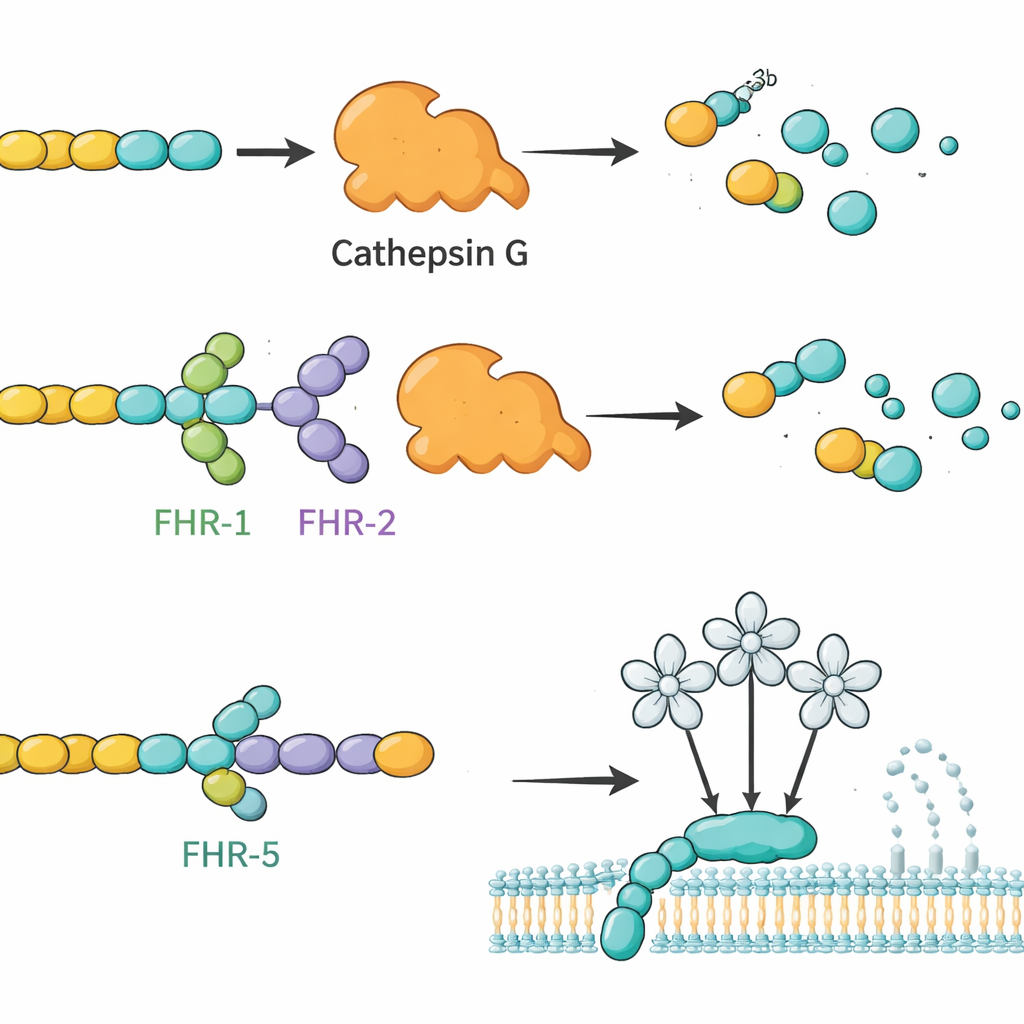
Come i nuovi legami rimodellano l’attività del complemento
Sulla base di queste mappe di legame, gli autori hanno valutato se le FHR potessero modificare la funzione di questi partner. Si sono concentrati innanzitutto su C3b, un frammento centrale del complemento, e su CTSG, un enzima dei neutrofili noto per degradare C3b senza l’aiuto di altri fattori. In reazioni in provetta, CTSG degradava prontamente C3b in frammenti inattivi. Quando venivano aggiunti FHR‑1 o FHR‑2, questa degradazione rallentava in modo evidente, suggerendo che queste FHR agiscano come regolatori competitivi che proteggono C3b da CTSG. Al contrario, il fattore H e FHL‑1 acceleravano il taglio mediato da CTSG, mettendo in luce come proteine strettamente correlate possano avere effetti funzionali opposti. Il gruppo ha inoltre esaminato come le FHR influenzino il braccio lectinico del complemento, che si attiva quando MBL2 riconosce specifici pattern zuccherini. Qui, la FHR‑5 (e, in misura minore, FHL‑1 e fattore H) attenuava l’attività della via lectinica in modo dipendente dalla dose, coerente con il legame di FHR‑5 a MBL2 e la modulazione della sua capacità di avviare la cascata.
Collegare attacco immunitario, coagulazione e danno tessutale
Le interazioni ora confermate con C4 e PPBP suggeriscono un più ampio dialogo tra complemento, coagulazione e infiammazione. C4 è una componente chiave precoce della via classica del complemento, mentre PPBP viene rilasciato dalle piastrine attivate e contribuisce a richiamare i globuli bianchi. La scoperta che diverse FHR si legano a PPBP suggerisce che queste proteine legate al complemento potrebbero non solo modulare le cascate chimiche sulle superfici cellulari, ma anche interagire con i meccanismi che reclutano le cellule immunitarie nei tessuti infiammati, inclusa la retina e i reni. Sebbene le conseguenze esatte di questi legami negli organismi viventi restino da chiarire, si inseriscono in un quadro sempre più ampio in cui le FHR aiutano a localizzare e plasmare le reazioni immunitarie in siti tissutali specifici, piuttosto che agire come semplici interruttori on/off.
Cosa significa per malattia e trattamento
Nel complesso, questo lavoro amplia l’“interattoma” della famiglia FHR e rivela che queste proteine coinvolgono una rete di partner solubili implicati nell’attivazione del complemento, nel rimodellamento tissutale e nel reclutamento cellulare. Per un pubblico non specialistico, il messaggio chiave è che piccole variazioni nel modo in cui le FHR si legano ad altre proteine del sangue possono influenzare se il complemento mantiene silenziosamente la salute dei tessuti o sfocia in autodanno. Poiché varianti genetiche che alterano le FHR sono associate a condizioni come la degenerazione maculare legata all’età, la nefropatia da IgA e altri disturbi mediati dal complemento, queste interazioni appena mappate offrono nuovi indizi sul perché alcune persone siano più vulnerabili a tali malattie. Nel lungo periodo, mirare a partnership specifiche delle FHR — come l’interazione FHR‑1/FHR‑2 con CTSG o l’interazione FHR‑5 con MBL2 — potrebbe ispirare terapie più precise che ristabiliscano l’equilibrio del sistema del complemento senza disattivare le nostre difese naturali.
Citazione: Tang, J., Woerz, F., Beyer, T. et al. Identification of novel blood-borne soluble binding partners of factor H-related proteins. Sci Rep 16, 9651 (2026). https://doi.org/10.1038/s41598-026-44779-9
Parole chiave: sistema del complemento, proteine correlate a fattore H, degenerazione maculare legata all’età, immunità innata, interazioni proteina–proteina