Clear Sky Science · de
Identifizierung neuartiger löslicher Blut-Bindungspartner der faktor H-ähnlichen Proteine
Warum winzige Blutproteine wichtig sind
Unser Immunsystem nutzt eine kraftvolle chemische Kaskade, das Komplementsystem, um Krankheitserreger zu bekämpfen und Zelltrümmer zu beseitigen. Wird diese Kontrolle gestört, kann das System körpereigene Gewebe schädigen und zu Krankheiten wie altersbedingter Makuladegeneration (eine führende Ursache für Erblindung) und bestimmten Nierenerkrankungen beitragen. Diese Studie untersucht eine wenig bekannte Gruppe von Blutproteinen, die faktor H-ähnlichen (FHR) Proteine, und stellt eine einfache, aber entscheidende Frage: An welche anderen Moleküle im Blut binden sie, und wie könnten diese Partnerschaften das Gleichgewicht zwischen schützender Immunfunktion und schädlicher Entzündung verschieben? 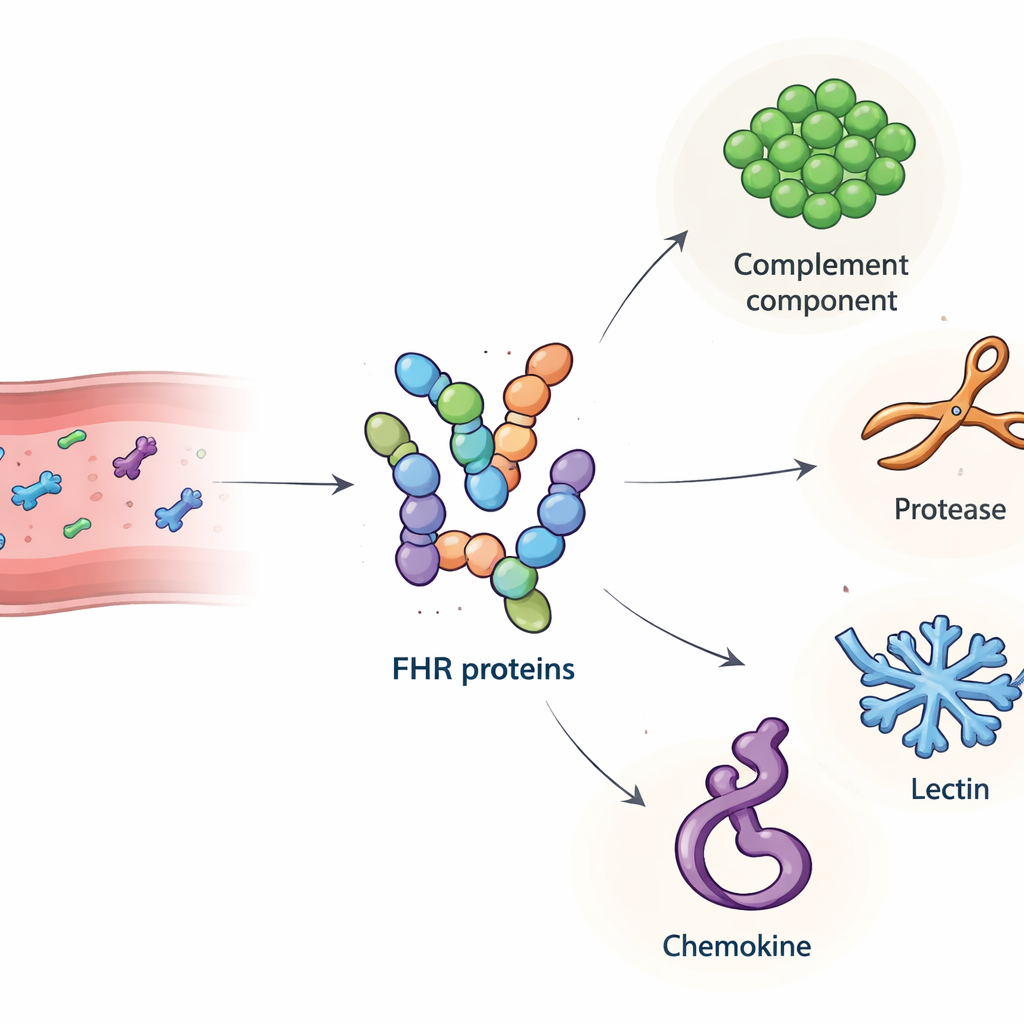
Eine Familie von Feineinstellern des Immunsystems
Komplementfaktor H ist ein gut untersuchtes „Bremssystem“ der Komplementkaskade, das eine Überaktivierung auf körpereigenen Zellen verhindert. FHR-Proteine sind nahe Verwandte von Faktor H, besitzen jedoch nicht die entscheidende Region, die das Komplement direkt abschaltet. Stattdessen können FHRs mit Faktor H um Bindungsstellen konkurrieren und scheinen in manchen Situationen eher wie Beschleuniger als wie Bremsen zu wirken. Genetische Studien verknüpfen Veränderungen in Menge oder Struktur der FHRs mit Erkrankungen von Auge, Niere und Gelenken, doch die genauen Wirkweisen dieser Proteine im Blut blieben unklar. Da FHRs hauptsächlich in der Leber gebildet werden und im Blutkreislauf zirkulieren, bevor sie sich in Geweben anreichern, vermuteten die Autor:innen, dass die Identifizierung ihrer löslichen, blutgebundenen Partner neue Ebenen der Immunregulation enthüllen könnte.
Fischen nach Partnern im Blutstrom
Das Team stellte zunächst hochreine Versionen aller wichtigen menschlichen FHR-Proteine sowie das kürzere faktor H-ähnliche Protein 1 (FHL‑1) in Zellkulturen her. Sie bestätigten, dass diese Laborproteine sich wie ihre natürlichen Gegenstücke verhielten, einschließlich der Bindung an bekannte Zielmoleküle und an Heparin, einen Zucker, der Strukturen in Gewebsmatrizes nachahmt. Anschließend nutzten sie jedes FHR als Köder: Sie immobilisierten es auf winzigen Kügelchen, inkubierten die Kügelchen mit menschlichem Serum und identifizierten mittels Massenspektrometrie, welche Blutproteine haften blieben. Dieses Screening ergab 34 Kandidatenpartner. Aus diesen konzentrierten sich die Forschenden auf vier sekretierte Moleküle mit klaren Immunfunktionen und eindeutigen Signalen im Test: Komplementkomponente C4, das Enzym Cathepsin G (CTSG), Mannose‑bindendes Lektin 2 (MBL2) und ein von Thrombozyten stammender Chemokin namens Platelet Basic Protein (PPBP). Nachfolgende Plattenbindungs-Tests bestätigten, dass diese Interaktionen direkt und selektiv sind, wobei unterschiedliche FHR-Familienmitglieder jeweils charakteristische Bindungsmuster zu den Partnern zeigten. 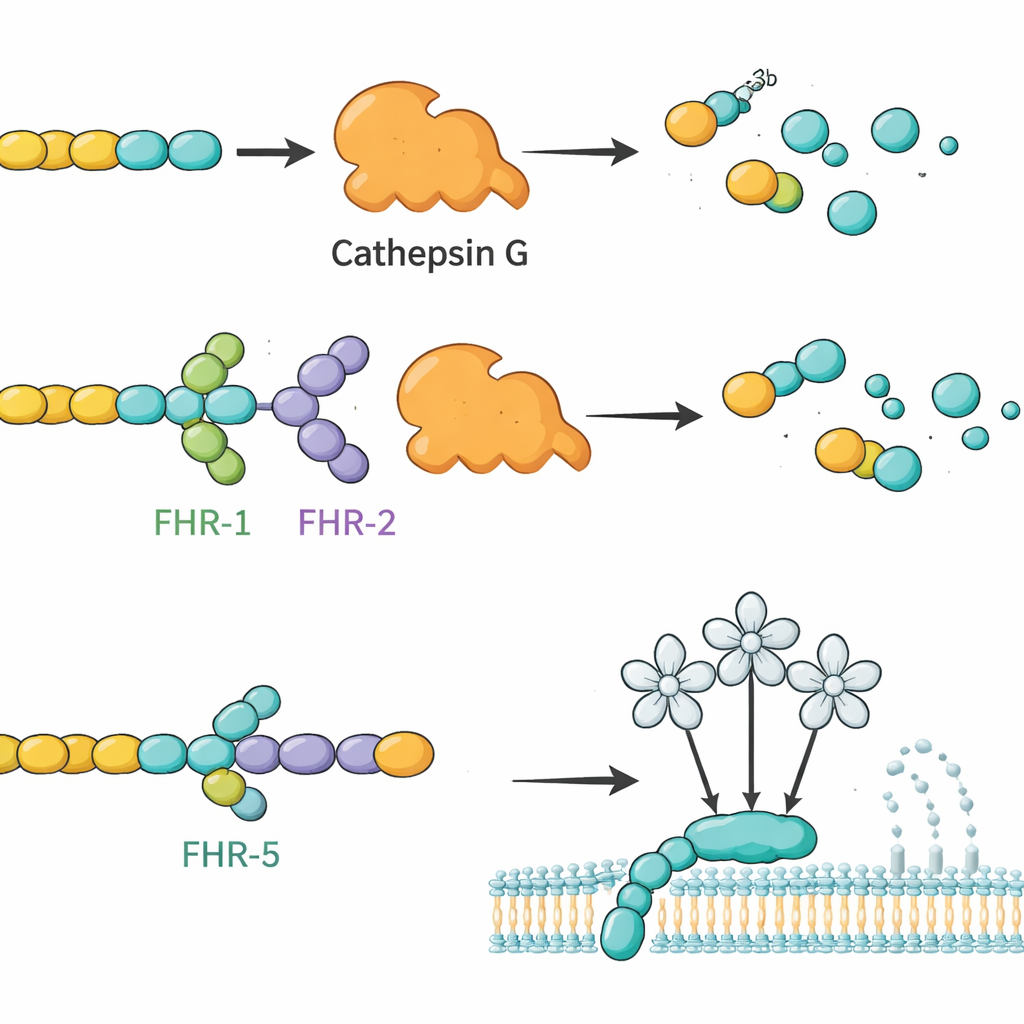
Wie neue Verbindungen die Komplementaktivität umgestalten
Auf Basis dieser Bindungskarten fragten die Autor:innen, ob FHRs das tatsächliche Funktionieren dieser Partner verändern können. Sie konzentrierten sich zunächst auf C3b, ein zentrales Komplementfragment, und CTSG, ein Neutrophilen-Enzym, das bekanntlich C3b ohne Hilfe anderer Faktoren zerschneidet. In Reaktionen im Reagenzglas baute CTSG C3b zuverlässig in inaktive Fragmente ab. Wurde FHR‑1 oder FHR‑2 zugegeben, verlangsamte sich dieser Abbau deutlich, was darauf hindeutet, dass diese FHRs als kompetitive Regulatoren wirken und C3b vor CTSG abschirmen. Im Gegensatz dazu beschleunigten Faktor H und FHL‑1 die CTSG‑vermittelte Spaltung, was unterstreicht, wie eng verwandte Proteine entgegengesetzte funktionelle Effekte haben können. Die Gruppe untersuchte außerdem, wie FHRs den Lektin‑Arm des Komplements beeinflussen, der ausgelöst wird, wenn MBL2 bestimmte Zuckerstrukturen erkennt. Hier dämpfte FHR‑5 (und in geringerem Maße FHL‑1 und Faktor H) die Aktivität des Lektinwegs dosisabhängig, was zu FHR‑5s Bindung an MBL2 und der Modulation seiner Fähigkeit passt, die Kaskade zu starten.
Verbindung von Immunangriff, Gerinnung und Gewebeschaden
Die neu bestätigten Interaktionen mit C4 und PPBP deuten auf eine breitere Vernetzung zwischen Komplement, Blutgerinnung und Entzündung hin. C4 ist eine wichtige frühe Komponente des klassischen Komplementwegs, während PPBP von aktivierten Thrombozyten freigesetzt wird und die Rekrutierung weißer Blutkörperchen unterstützt. Der Befund, dass mehrere FHRs an PPBP binden, legt nahe, dass diese komplement‑assoziierten Proteine nicht nur chemische Kaskaden an Zelloberflächen feinregulieren, sondern auch Einfluss darauf haben können, wie Immunzellen in entzündete Gewebe — etwa Netzhaut und Nieren — angezogen werden. Obwohl die genauen Folgen dieser Bindungen im lebenden Organismus noch geklärt werden müssen, fügen sie sich in ein wachsendes Bild, in dem FHR‑Proteine helfen, Immunreaktionen an bestimmten Gewebeorten zu positionieren und zu formen, statt als einfache An/Aus‑Schalter zu fungieren.
Was das für Krankheit und Therapie bedeutet
Insgesamt erweitert diese Arbeit das „Interaktom“ der FHR‑Familie und zeigt, dass diese Proteine ein Netzwerk löslicher Partner engagieren, die an Komplementaktivierung, Gewebsumbau und Zellenrekrutierung beteiligt sind. Für ein Publikum außerhalb der Fachwelt lautet die Kernbotschaft: Kleine Veränderungen darin, wie FHRs an andere Blutproteine binden, können entscheiden, ob das Komplement still die Gewebeintegrität wahrt oder sich zu selbstschädigender Aktivität aufschaukelt. Da genetische Varianten, die FHRs verändern, mit Erkrankungen wie altersbedingter Makuladegeneration, IgA‑Nephropathie und anderen komplementvermittelten Störungen verknüpft sind, liefern diese neu kartierten Interaktionen neue Hinweise darauf, warum manche Menschen anfälliger für solche Krankheiten sind. Langfristig könnten gezielte Eingriffe in spezifische FHR‑Partnerschaften — etwa die FHR‑1/FHR‑2‑Interaktion mit CTSG oder die FHR‑5‑Interaktion mit MBL2 — präzisere Therapien inspirieren, die das Gleichgewicht im Komplementsystem wiederherstellen, ohne unsere natürlichen Abwehrkräfte auszuschalten.
Zitation: Tang, J., Woerz, F., Beyer, T. et al. Identification of novel blood-borne soluble binding partners of factor H-related proteins. Sci Rep 16, 9651 (2026). https://doi.org/10.1038/s41598-026-44779-9
Schlüsselwörter: Komplementsystem, faktor H-ähnliche Proteine, altersbedingte Makuladegeneration, angeborene Immunität, Protein–Protein-Interaktionen