Clear Sky Science · sv
Identifiering av nya blodburna lösliga bindningspartner till faktor H‑relaterade proteiner
Varför små blodproteiner spelar roll
Vårt immunsystem förlitar sig på en kraftfull kemisk kaskad, kallad komplement, för att bekämpa mikrober och rensa cellulärt skräp. När detta system inte kontrolleras korrekt kan det börja skada våra egna vävnader och bidra till sjukdomar som åldersrelaterad makuladegeneration (en ledande orsak till blindhet) och vissa njursjukdomar. Denna studie undersöker en lite känd grupp blodproteiner, de faktor H‑relaterade (FHR) proteinerna, och ställer en enkel men avgörande fråga: vilka andra molekyler i blodet binder de till, och hur kan dessa partnerskap rubba balansen mellan skyddande aktivitet och skadlig inflammation? 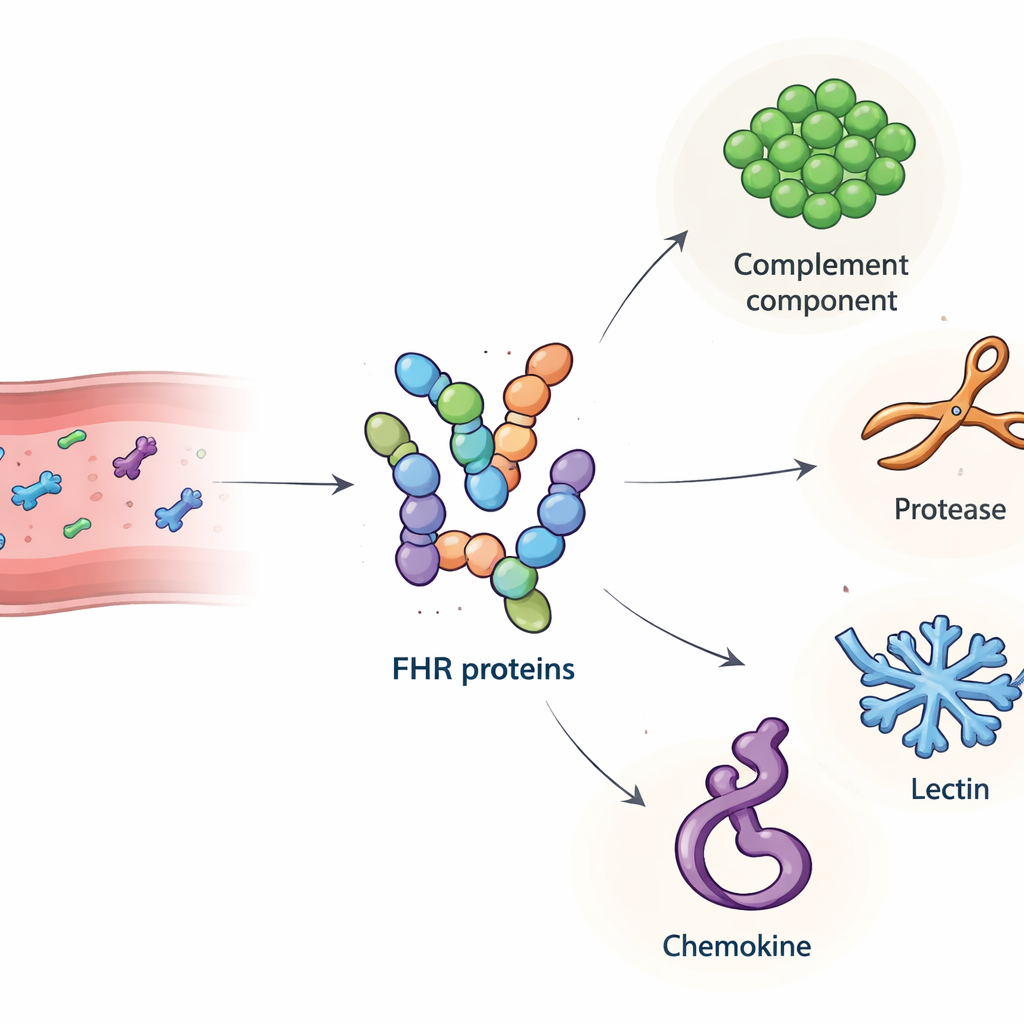
En familj av finjusterare i immunförsvaret
Komplementfaktor H är en välstuderad ”broms” i komplementkaskaden som förhindrar överaktivering på våra egna celler. FHR‑proteiner är nära släktingar till faktor H, men saknar det avgörande området som direkt stänger av komplementet. Istället kan FHR:er konkurrera med faktor H om bindningsställen, och i vissa situationer verkar de fungera mer som gaspedaler än bromsar. Genetiska studier kopplar förändringar i FHR‑nivåer eller struktur till sjukdomar i öga, njure och leder, men exakt hur dessa proteiner verkar i blodomloppet har förblivit oklart. Eftersom FHR:er huvudsakligen bildas i levern och sedan cirkulerar innan de slår sig ner i vävnader, resonerade författarna att upptäcka deras lösliga blodburna partner skulle kunna avslöja nya nivåer av immunreglering.
Fiska efter partner i blodomloppet
Gruppen producerade först höggradigt renade versioner av alla större mänskliga FHR‑proteiner, samt den kortare faktor H‑lika proteinet 1 (FHL‑1), i cellkulturer. De bekräftade att dessa laboratorieframställda proteiner uppträdde som sina naturliga motsvarigheter, inklusive bindning till kända mål och till heparin, ett socker som efterliknar strukturer i vävnadsmatriser. Därefter använde de varje FHR som bete: immobiliserade det på små kulor, inkuberade kulorna med human serum och använde masspektrometri för att identifiera vilka blodproteiner som fastnade. Denna screening gav 34 kandidatpartner. Av dessa fokuserade forskarna på fyra utsöndrade molekyler med tydliga immunroller och klara signaler i assayen: komplementkomponenten C4, enzymet kathepsin G (CTSG), mannosbindande lektin 2 (MBL2) och en trombocyt‑deriverad kemokin kallad platelet basic protein (PPBP). Uppföljande plattformsbaserade bindningstester bekräftade att dessa interaktioner är direkta och selektiva, med olika FHR‑familjemedlemmar som visar distinkta bindningsmönster till varje partner. 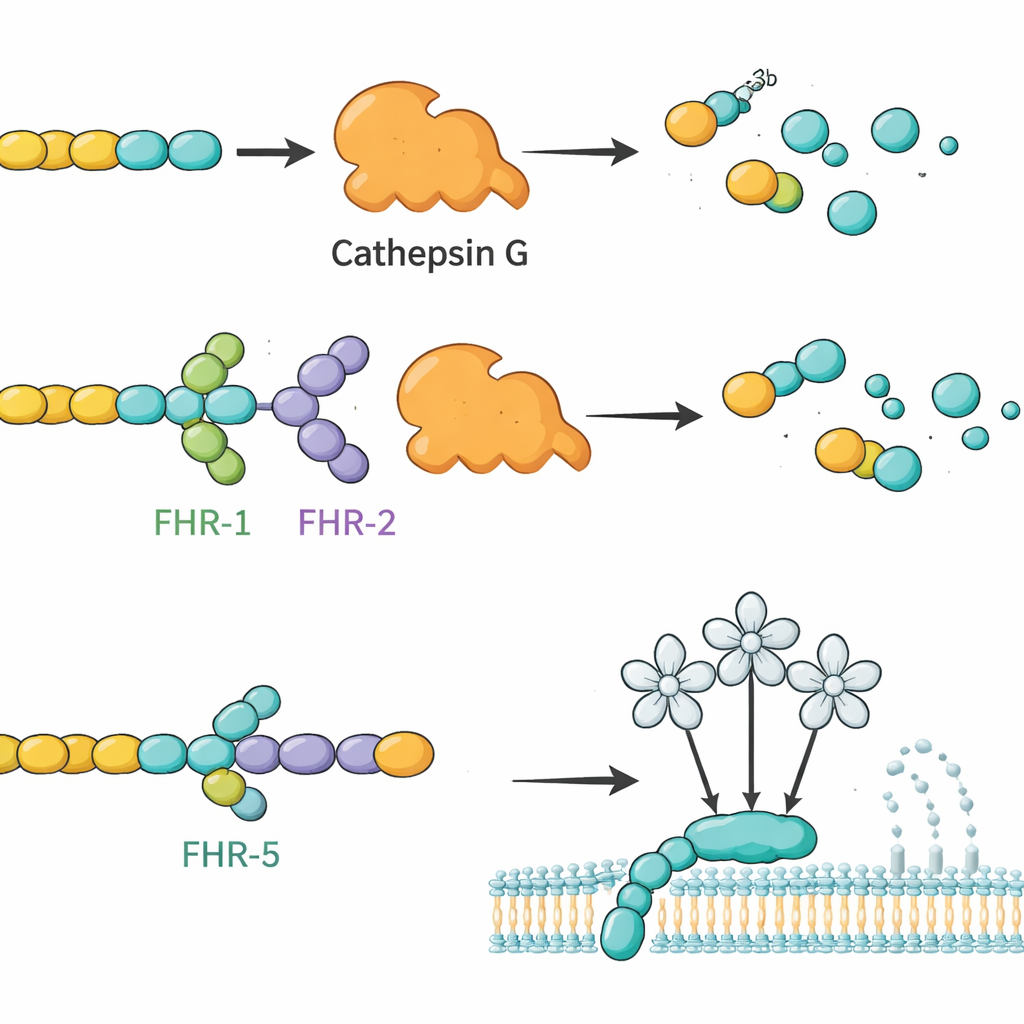
Hur nya länkar omformar komplementaktivitet
Med dessa bindningskartor som grund frågade författarna om FHR:er kunde förändra vad dessa partner faktiskt gör. De började med C3b, en central komplementfragment, och CTSG, ett neutrofilenzym känt för att klyva C3b utan hjälp av andra faktorer. I reaktioner i provrör degraderade CTSG lätt C3b till inaktiva fragment. När FHR‑1 eller FHR‑2 tillsattes gick denna nedbrytning tydligt långsammare, vilket tyder på att dessa FHR:er fungerar som konkurrerande regulatorer som skyddar C3b från CTSG. I kontrast gjorde faktor H och FHL‑1 CTSG‑driven klyvning snabbare, vilket understryker hur nära besläktade proteiner kan ha motsatta funktionella effekter. Gruppen undersökte också hur FHR:er påverkar lektinarmen av komplementet, som triggas när MBL2 känner igen vissa sockerstrukturer. Här dämpade FHR‑5 (och i mindre grad FHL‑1 och faktor H) lektinvägens aktivitet beroende på dos, i linje med att FHR‑5 binder MBL2 och modulerar dess förmåga att starta kaskaden.
Kopplingar mellan immunsvar, koagulation och vävnadsskada
De nybekräftade interaktionerna med C4 och PPBP antyder bredare korsprat mellan komplement, blodkoagulation och inflammation. C4 är en tidig nyckelkomponent i den klassiska komplementvägen, medan PPBP frigörs av aktiverade trombocyter och hjälper till att rekrytera vita blodkroppar. Upptäckten att flera FHR:er binder PPBP tyder på att dessa komplement‑kopplade proteiner inte bara finjusterar kemiska kaskader på cellsystem, utan även kan påverka hur immunceller lockas till inflammerade vävnader, inklusive näthinnan och njurarna. Även om de exakta konsekvenserna av dessa bindningar i levande organismer återstår att klarlägga, stämmer de med en växande bild där FHR‑proteiner hjälper till att positionera och forma immunsvar på specifika vävnadsplatser snarare än att fungera som enkla av‑/på‑brytare.
Vad detta betyder för sjukdom och behandling
Sammanslaget utvidgar detta arbete FHR‑familjens ”interaktom” och visar att dessa proteiner engagerar ett nätverk av lösliga partner involverade i komplementaktivering, vävnadsombyggnad och cellrekrytering. För en allmän publik är huvudbudskapet att små förändringar i hur FHR:er binder andra blodproteiner kan avgöra om komplement lugnt upprätthåller vävnadshälsa eller snedvrider till självskada. Eftersom genetiska varianter som ändrar FHR:er kopplas till tillstånd som åldersrelaterad makuladegeneration, IgA‑nefropati och andra komplementmedierade sjukdomar, ger dessa nykartlagda interaktioner nya ledtrådar till varför vissa människor är mer sårbara för sådana sjukdomar. På sikt skulle riktade terapier mot specifika FHR‑partnerskap — såsom FHR‑1/FHR‑2‑interaktionen med CTSG eller FHR‑5‑interaktionen med MBL2 — kunna inspirera mer precisa behandlingar som återställer balansen i komplementsystemet utan att stänga av våra naturliga försvar.
Citering: Tang, J., Woerz, F., Beyer, T. et al. Identification of novel blood-borne soluble binding partners of factor H-related proteins. Sci Rep 16, 9651 (2026). https://doi.org/10.1038/s41598-026-44779-9
Nyckelord: komplementsystemet, faktor H‑relaterade proteiner, åldersrelaterad makuladegeneration, medfödd immunitet, protein–protein‑interaktioner