Clear Sky Science · es
Identificación de nuevas proteínas solubles en sangre que se unen a las proteínas relacionadas con el factor H
Por qué importan las pequeñas proteínas sanguíneas
Nuestro sistema inmunitario se basa en una poderosa cascada química, llamada complemento, para combatir gérmenes y eliminar restos celulares. Cuando este sistema no está bien controlado, puede comenzar a dañar nuestros propios tejidos y contribuir a enfermedades como la degeneración macular relacionada con la edad (una causa principal de ceguera) y ciertos trastornos renales. Este estudio examina un grupo poco conocido de proteínas sanguíneas, las proteínas relacionadas con el factor H (FHR), y plantea una pregunta sencilla pero crucial: ¿a qué otras moléculas en la sangre se unen, y cómo podrían esas asociaciones inclinar la balanza entre una protección saludable y una inflamación perjudicial? 
Una familia de reguladores finos del sistema inmunitario
El factor H del complemento es un “freno” bien estudiado de la cascada del complemento, que evita la sobreactivación sobre nuestras propias células. Las FHR son parientes cercanos del factor H, pero carecen de la región clave que apaga directamente el complemento. En su lugar, las FHR pueden competir con el factor H por sitios de unión y, en algunos contextos, parecen actuar más como aceleradores que como frenos. Estudios genéticos vinculan cambios en los niveles o la estructura de las FHR con enfermedades del ojo, el riñón y las articulaciones, aunque las formas exactas en que estas proteínas actúan en el torrente sanguíneo han seguido siendo oscuras. Dado que las FHR se producen principalmente en el hígado y luego circulan por la sangre antes de asentarse en los tejidos, los autores razonaron que descubrir sus socios solubles en sangre podría revelar nuevas capas de control inmunitario.
Pesca de socios en el torrente sanguíneo
El equipo primero produjo versiones altamente purificadas de todas las principales FHR humanas, además de la versión más corta similar al factor H llamada proteína 1 parecida al factor H (FHL‑1), en células en cultivo. Confirmaron que estas proteínas sintetizadas en el laboratorio se comportaban como sus contrapartes naturales, incluida la unión a objetivos conocidos y a la heparina, un azúcar que imita estructuras en las matrices tisulares. A continuación, usaron cada FHR como cebo: la inmovilizaron en pequeñas perlas, incubaron las perlas con suero humano y luego emplearon espectrometría de masas para identificar qué proteínas sanguíneas se adherían. Esta prueba identificó 34 candidatos. De éstos, los investigadores se centraron en cuatro moléculas secretadas con funciones inmunitarias claras y señales nítidas en el ensayo: el componente del complemento C4, la enzima catepsina G (CTSG), la lectina ligada a manosa 2 (MBL2) y una quimiocina derivada de plaquetas llamada proteína básica plaquetaria (PPBP). Pruebas de unión adicionales en placas confirmaron que estas interacciones son directas y selectivas, con distintos miembros de la familia FHR mostrando patrones de unión diferentes a cada socio. 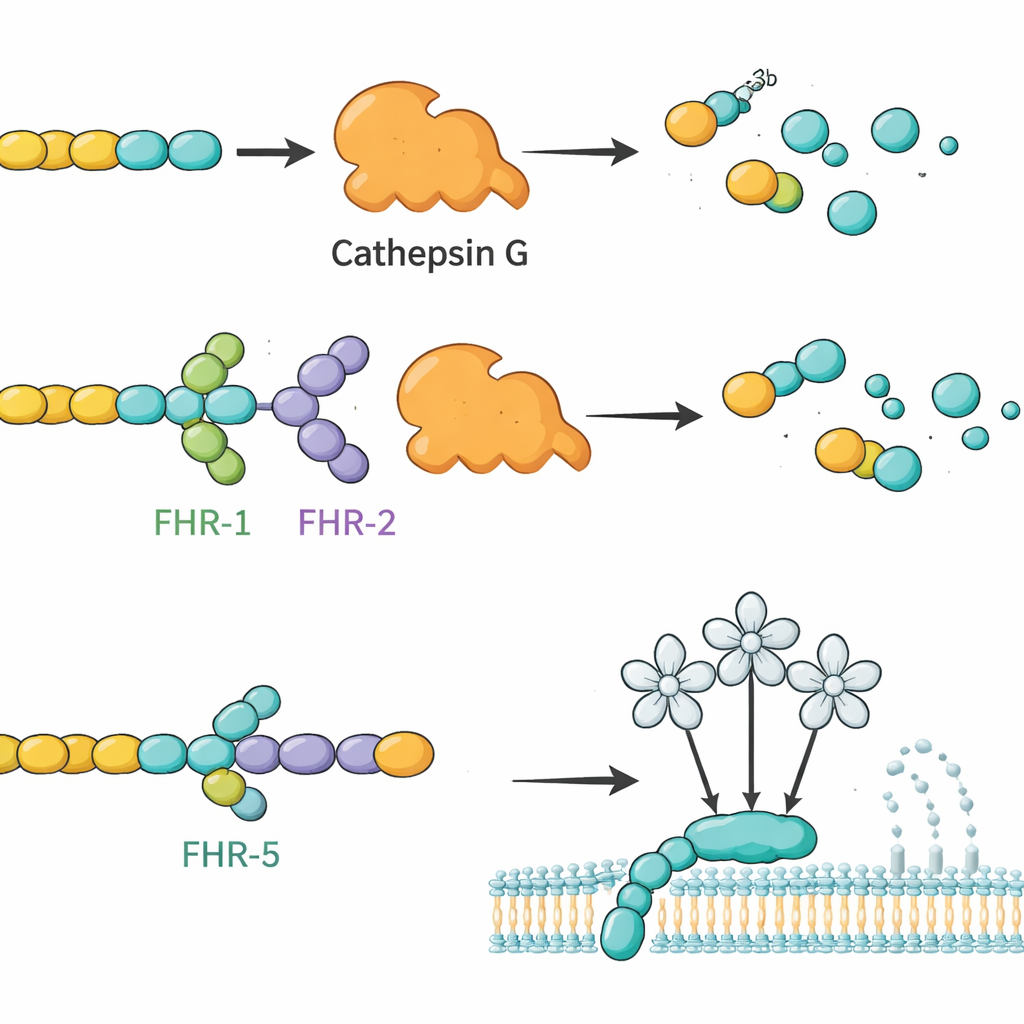
Cómo los nuevos vínculos remodelan la actividad del complemento
Partiendo de estos mapas de unión, los autores preguntaron si las FHR podrían cambiar lo que estos socios hacen realmente. Se centraron primero en C3b, un fragmento central del complemento, y en la CTSG, una enzima de neutrófilos conocida por degradar C3b sin ayuda de otros factores. En reacciones de tubo de ensayo, la CTSG degradó con facilidad C3b en fragmentos inactivos. Cuando se añadió FHR‑1 o FHR‑2, esta degradación se ralentizó notablemente, lo que sugiere que estas FHR actúan como reguladores competitivos que protegen C3b de la CTSG. En contraste, el factor H y FHL‑1 aceleraron la escisión mediada por CTSG, subrayando cómo proteínas estrechamente relacionadas pueden tener efectos funcionales opuestos. El grupo también investigó cómo las FHR influyen en la rama lectina del complemento, que se activa cuando MBL2 reconoce ciertos patrones de azúcares. Aquí, FHR‑5 (y en menor medida FHL‑1 y factor H) atenuó la actividad de la vía lectina de forma dependiente de la dosis, coherente con que FHR‑5 se une a MBL2 y modula su capacidad para iniciar la cascada.
Conectando el ataque inmunitario, la coagulación y el daño tisular
Las interacciones recién confirmadas con C4 y PPBP apuntan a una comunicación más amplia entre complemento, coagulación sanguínea e inflamación. C4 es un componente temprano clave de la vía clásica del complemento, mientras que PPBP se libera por plaquetas activadas y ayuda a reclutar leucocitos. El hallazgo de que varias FHR se unen a PPBP sugiere que estas proteínas vinculadas al complemento pueden no solo ajustar las cascadas químicas en superficies celulares, sino también intersecarse con la forma en que las células inmunitarias son atraídas hacia los tejidos inflamados, incluida la retina y los riñones. Aunque las consecuencias exactas de estas uniones en organismos vivos aún deben aclararse, encajan con una imagen creciente en la que las FHR ayudan a posicionar y dar forma a las reacciones inmunitarias en sitios tisulares específicos, en lugar de actuar como simples interruptores de encendido/apagado.
Qué significa esto para la enfermedad y el tratamiento
En conjunto, este trabajo amplía el “interactoma” de la familia FHR y revela que estas proteínas interactúan con una red de socios solubles implicados en la activación del complemento, la remodelación tisular y el reclutamiento celular. Para un público general, el mensaje clave es que pequeños cambios en cómo las FHR se unen a otras proteínas sanguíneas pueden influir en si el complemento mantiene silenciosamente la salud tisular o deriva hacia la autolesión. Dado que variantes genéticas que alteran las FHR se asocian con afecciones como la degeneración macular relacionada con la edad, la nefropatía por IgA y otros trastornos mediados por el complemento, estas interacciones recientemente cartografiadas ofrecen pistas sobre por qué algunas personas son más vulnerables a dichas enfermedades. A largo plazo, dirigir asociaciones específicas de las FHR —como la interacción de FHR‑1/FHR‑2 con CTSG o la de FHR‑5 con MBL2— podría inspirar terapias más precisas que restablezcan el equilibrio del sistema del complemento sin desactivar nuestras defensas naturales.
Cita: Tang, J., Woerz, F., Beyer, T. et al. Identification of novel blood-borne soluble binding partners of factor H-related proteins. Sci Rep 16, 9651 (2026). https://doi.org/10.1038/s41598-026-44779-9
Palabras clave: sistema del complemento, proteínas relacionadas con el factor H, degeneración macular relacionada con la edad, inmunidad innata, interacciones proteína–proteína