Clear Sky Science · zh
氨基己二酸半醛合成酶:在戊二酸血症1型中作为底物减少疗法的潜在靶点
为何这种罕见儿童疾病很重要
戊二酸血症1型是一种罕见的遗传性疾病,多见于婴幼儿,但它说明了一个更广泛的理念:通过调整体内化学反应的单一步骤,就能保护大脑免受终生损伤。尽管有现代的新生儿筛查和严格的饮食控制,许多患儿仍然出现运动障碍、脑部改变和肾脏问题。本研究探索了一种在源头上阻断有害物质生成的新途径——称为底物减少疗法,并评估其是否有望带来更安全、更有效的治疗方法。
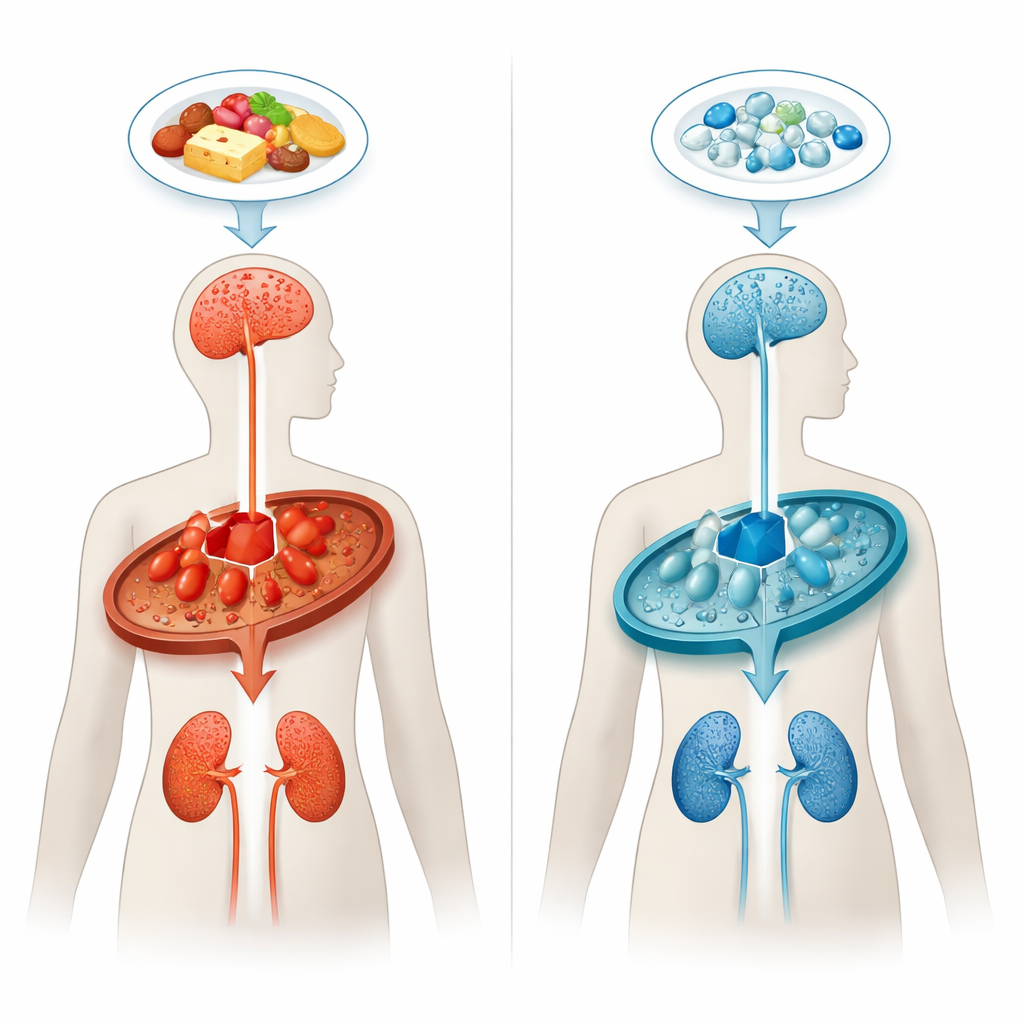
体内化学的交通堵塞
在戊二酸血症1型中,人体无法正常分解某些蛋白质构件,尤其是氨基酸赖氨酸。缺失或功能异常的酶——谷酰基辅酶A脱氢酶,会引发代谢“交通堵塞”,导致戊二酸及相关化合物积聚。这些物质对控制运动的特定脑区尤为有毒,尤其在生命早期更易受损。即便在出生后很快被发现并接受低赖氨酸特殊饮食,大约三分之一的患儿仍会出现严重神经系统症状,且随着年龄增长,许多人表现出进展性的白质和肾脏问题。
一个可以设置路障的新位置
目前的治疗侧重于限制进入体内的赖氨酸量并帮助清除有毒代谢产物,但并不直接改变该异常通路本身。研究者提出了一个关键问题:与其应对不断积累的废物,不如减慢进入这条异常通路的输入是否可行?他们将注意力转向另一种酶——氨基己二酸半醛合成酶(aminoadipate-semialdehyde synthase),它在赖氨酸分解的主要途径之一中执行前两步。天生缺乏该酶的人通常赖氨酸水平较高,但很少或没有明显健康问题,这表明阻断它可能相对安全。
在基因改造小鼠中测试这一想法
为验证这一策略,研究团队使用了缺乏谷酰基辅酶A脱氢酶的小鼠,这是一种成熟的人类疾病模型。这些动物在组织中会积累大量有毒酸类,当给予富含赖氨酸的饮食刺激时,会出现癫痫、运动障碍、脑损伤并常致死。研究者随后构建了双敲除小鼠,同时缺失疾病相关酶和氨基己二酸半醛合成酶。在常规喂养条件下,这些双敲除小鼠在广泛的行为和生理测试中表现得像健康动物,且仅显示轻度生化异常。
更少的有毒积聚与更好的脑部健康
真正的考验是在两类疾病模型小鼠均暴露于旨在挑战该脆弱通路的高赖氨酸饮食时进行的。仅缺失疾病相关酶的小鼠在脑、肝、肾、血液和尿液中积累了极高水平的有毒酸,许多出现严重神经症状、癫痫和体重下降。相比之下,双敲除动物在所有这些组织中的戊二酸水平显著降低,疾病表现明显减少,行为近乎正常。对其大脑的显微检查显示,单敲除小鼠中常见的细小空泡和结构改变在双敲除中大为减少或消失。重要的是,对体成分、骨密度、心脏功能、免疫标志物和血液化学的详细检查未发现因阻断赖氨酸分解早期步骤而引起的重大非神经系统问题。
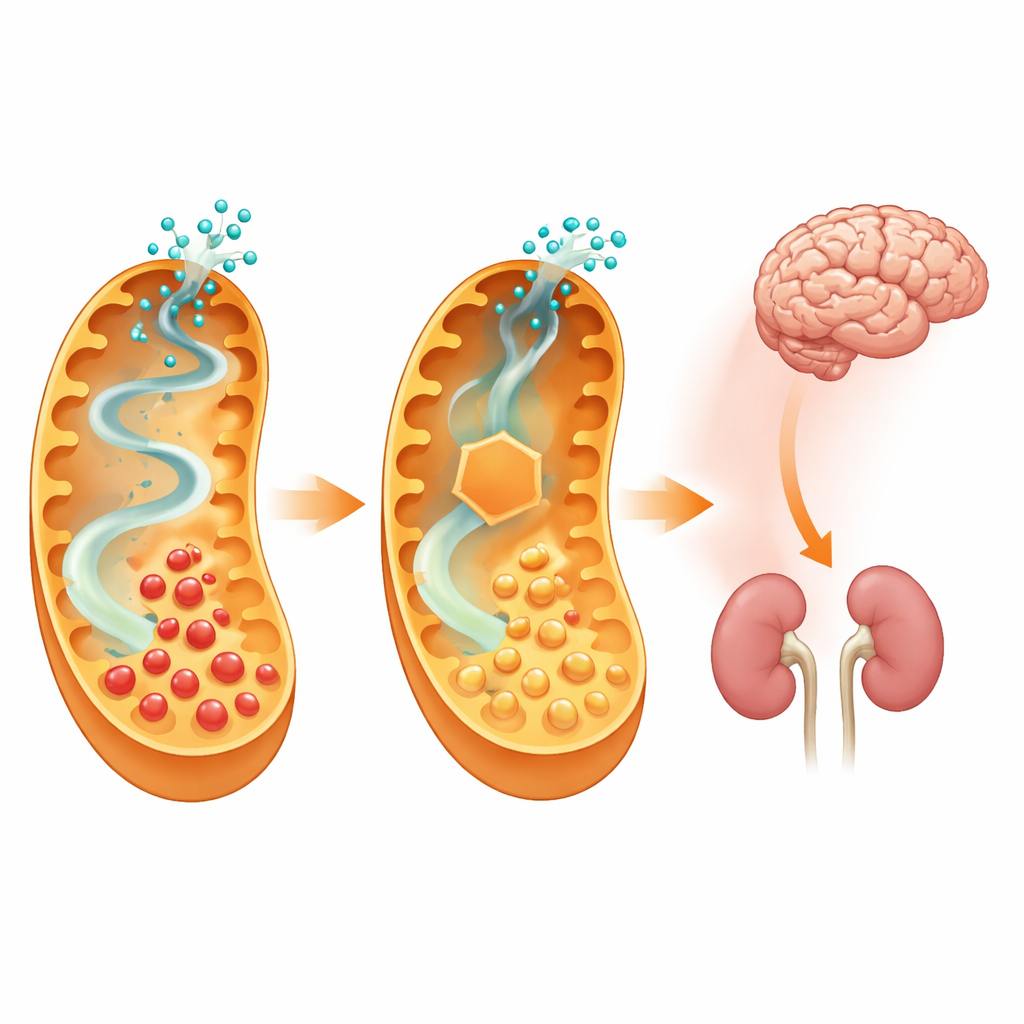
这对未来治疗的意义
通过关闭特定赖氨酸通路的第一步,研究者能够降低大脑对有毒代谢物的暴露,并在很大程度上保护小鼠免受由饮食触发的严重疾病爆发,同时未引发明显的新健康问题。这表明,设计用于部分抑制氨基己二酸半醛合成酶的药物,可能成为与饮食及其他治疗方法并用的强大新工具,用于治疗戊二酸血症1型的儿童。尽管目前的工作依赖于小鼠基因工程,且适宜的药物仍需开发并在人体中进行安全性测试,但该研究为有针对性地封堵上游代谢步骤可以改写这种毁灭性代谢性脑病的病程提供了有力的原理性证据。
引用: Saad, C., Jung-Klawitter, S., Dimitrov, B. et al. Aminoadipate-semialdehyde synthase, a potential target for substrate reduction therapy in glutaric aciduria type 1. Sci Rep 16, 10995 (2026). https://doi.org/10.1038/s41598-026-44377-9
关键词: 戊二酸血症1型, 赖氨酸代谢, 底物减少疗法, AASS抑制, 遗传代谢性疾病