Clear Sky Science · ja
アミノアジピンアルデヒド合成酵素:グルタル酸尿症タイプ1に対する基質低減療法の潜在的標的
なぜこのまれな小児疾患が重要なのか
グルタル酸尿症タイプ1は、主に乳児や幼児に影響する稀な先天性疾患ですが、より広い視点を示しています:体内の化学反応の一段階を調整することで、脳の生涯にわたる損傷を防げる可能性があるということです。新生児スクリーニングや厳格な食事療法が普及しているにもかかわらず、多くの患児は運動障害、脳の変化、腎機能の問題を発症します。本研究は、基質低減療法と呼ばれる戦略を用いて有害物質の産生を根本から減らす新たな方法を探り、それがより安全で効果的な治療につながるかを検証しています。
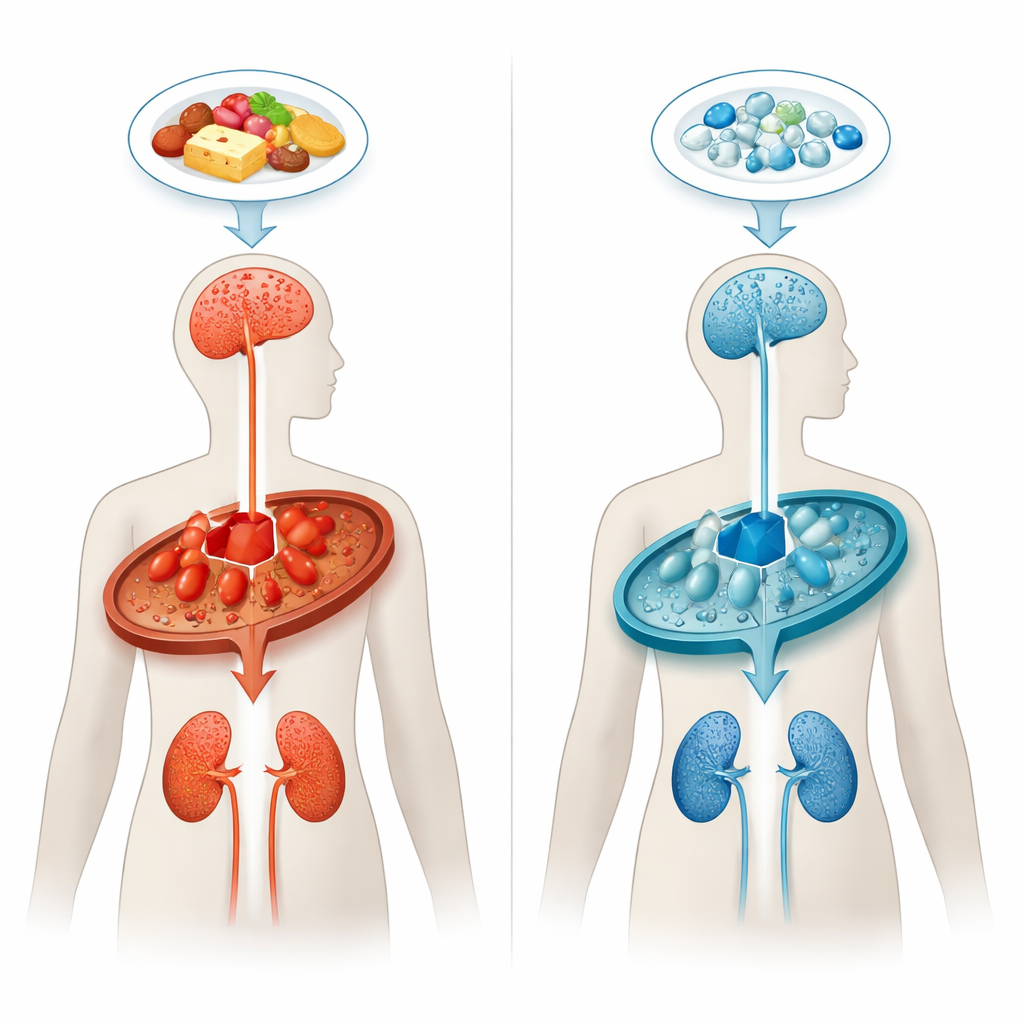
体内化学の渋滞
グルタル酸尿症タイプ1では、特にアミノ酸のリジンなど、タンパク質の一部を適切に分解できません。グルタリル-CoA脱水素酵素という酵素の欠損や機能不全により代謝の渋滞が起き、グルタル酸や関連化合物が蓄積します。これらの物質は、特に運動を制御する特定の脳領域に対して幼少期に強い毒性を示します。出生直後に早期発見され低リジン食にされても、約3分の1の子どもが重篤な神経症状を発症し、多くは成長に伴って白質変化や腎障害を示します。
新たに道を塞ぐ場所
現在の治療はリジンの体内流入を制限し、有害副産物の排除を助けることに重点が置かれていますが、欠損した経路そのものの働きを直接変えるものではありません。研究者らは重要な疑問を投げかけました:蓄積する廃棄物を扱うのではなく、故障した経路への入力自体を遅らせることはできないか?彼らは、主要なリジン分解経路の最初の二段階を担うアミノアジピンアルデヒド合成酵素(AASS)に注目しました。この酵素を自然に欠く人は通常リジン値が高くても健康問題がほとんどまたは全く見られないことから、これを遮断することは比較的安全である可能性が示唆されます。
遺伝子改変マウスでの検証
この戦略を検証するため、研究チームはヒト疾患のよく確立されたモデルであるグルタリル-CoA脱水素酵素欠損マウスを用いました。これらの動物は組織に大量の有毒酸を蓄積し、リジン豊富な食餌にさらされると発作、運動障害、脳損傷を起こし、しばしば死亡します。研究者らは次に、疾患酵素とアミノアジピンアルデヒド合成酵素の両方を欠く二重ノックアウトマウスを作成しました。標準的な飼育条件下では、これらの二重ノックアウトマウスは幅広い検査で外見や行動が健常動物と同様であり、化学的変化も軽度にとどまりました。
有害な蓄積の減少と脳の改善
本当の試験は、両タイプの疾患モデルマウスにリジンを多く含む食餌を与えて脆弱な経路に負荷をかけたときに行われました。疾患酵素のみを欠くマウスは脳、肝臓、腎臓、血液、尿に非常に高いレベルの有毒酸を蓄積し、多くが重度の神経症状、発作、体重減少を示しました。対照的に、二重ノックアウト動物ではこれらの組織のグルタル酸レベルが劇的に低く、病気の徴候ははるかに少なく、行動はほぼ正常でした。顕微鏡観察でも、単独ノックアウトで見られた小さな空胞や構造変化は二重ノックアウトでは大幅に減少または消失していました。重要なことに、体組成、骨密度、心機能、免疫マーカー、血液化学の詳細な検査でも、リジン分解の初期段階を遮断したことによる重大な神経以外の問題は見つかりませんでした。
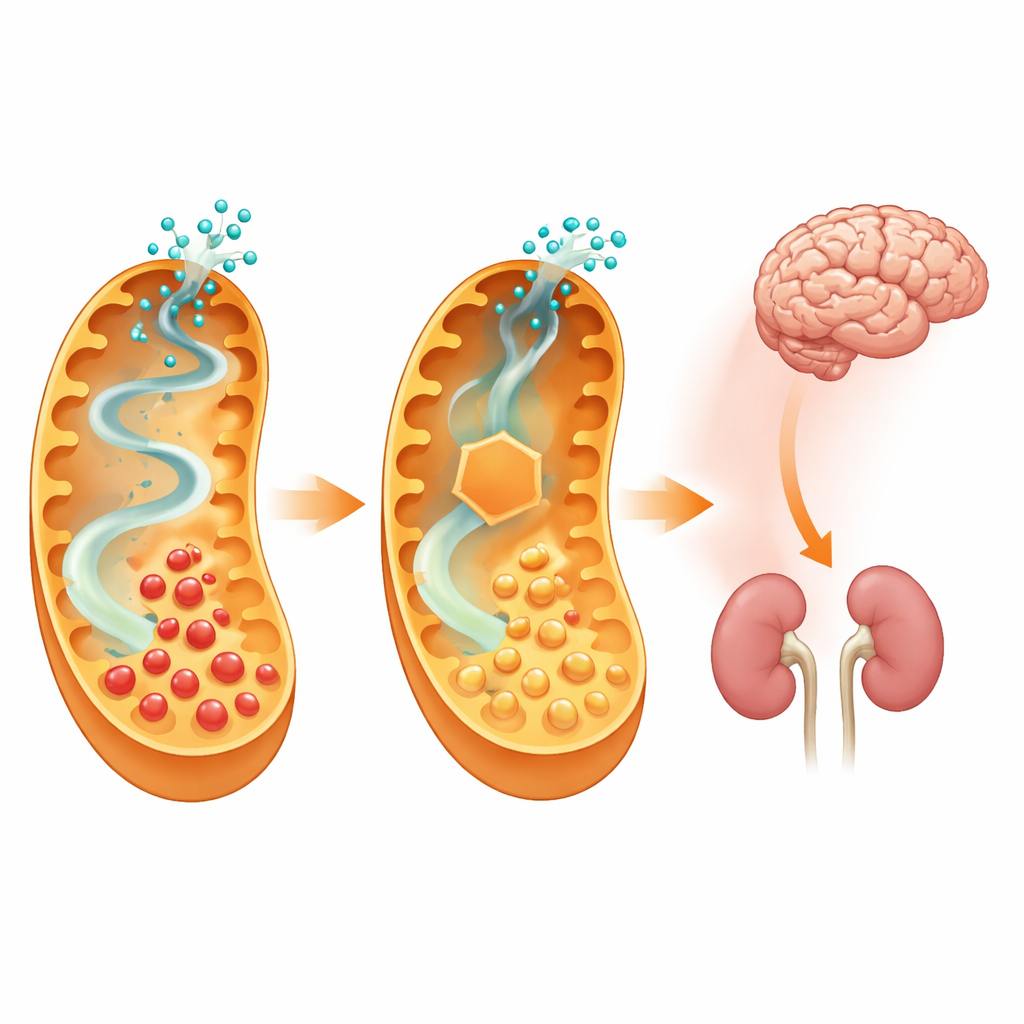
今後の治療への示唆
特定のリジン経路の最初の段階を遮断することで、研究者らは脳が有毒代謝産物にさらされる量を減らし、重篤な食事誘発性の発症からマウスを大部分守ることができました。しかも明らかな新たな健康問題は生じませんでした。これは、アミノアジピンアルデヒド合成酵素を部分的に阻害する薬剤が、低リジン食など既存の治療に加わる強力な新しい手段となり得ることを示唆します。現在の研究は遺伝子改変マウスに基づくものであり、適切な薬剤の開発とヒトでの安全性試験が今後必要ですが、上流の化学反応を慎重に標的化してブロックすることで、壊滅的な代謝性脳疾患の経過を変えられるという強い原理的証拠を提供しています。
引用: Saad, C., Jung-Klawitter, S., Dimitrov, B. et al. Aminoadipate-semialdehyde synthase, a potential target for substrate reduction therapy in glutaric aciduria type 1. Sci Rep 16, 10995 (2026). https://doi.org/10.1038/s41598-026-44377-9
キーワード: グルタル酸尿症タイプ1, リジン代謝, 基質低減療法, AASS阻害, 先天代謝異常