Clear Sky Science · he
אמינו-אדיפטאלדהיד סינתאז, מטרה פוטנציאלית לטיפול בהפחתת תת-רעף בתסמונת החומצה הגלוטארית סוג 1
מדוע המחלה הילדותית הנדירה הזו חשובה
תסמונת החומצה הגלוטארית סוג 1 היא הפרעה תורשתית נדירה הפוגעת בעיקר בתינוקות וילדים קטנים, אך היא ממחישה רעיון רחב יותר: כיצד שינוי של שלב בודד בכימיה של הגוף יכול להגן על המוח מנזק מתמשך. למרות בדיקות לכלל התינוקות לאחר הלידה ותזונה זהירה, רבים מהילדים עם מצב זה עדיין מפתחים בעיות תנועה, שינויים מוחיים ובעיות כלייתיות. מחקר זה בוחן גישה חדשה לקטיעה של ייצור חומרים מזיקים במקורם — באמצעות אסטרטגיה הנקראת טיפול בהפחתת מצע — ובודק האם היא עשויה להוביל לטיפולים בטוחים ויעילים יותר.
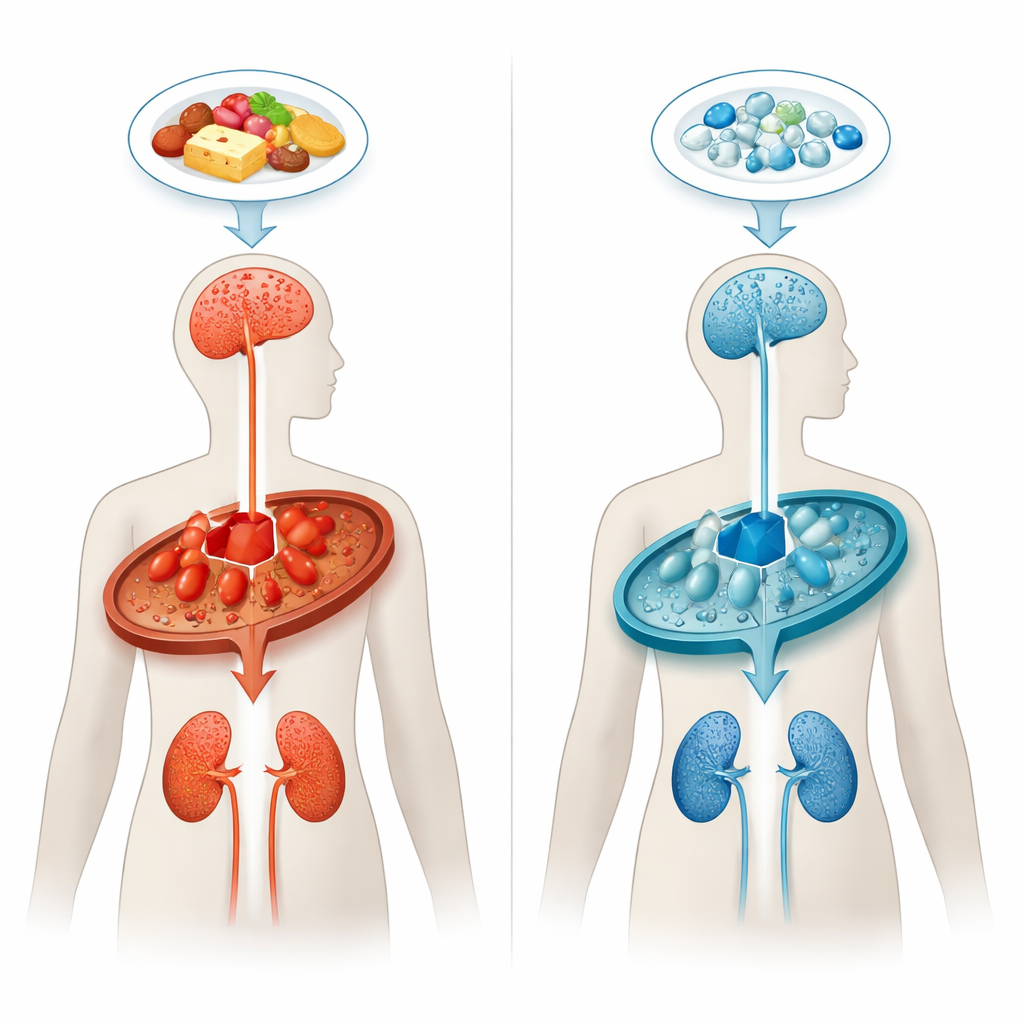
פקק תנועה בכימיה של הגוף
בתסמונת החומצה הגלוטארית סוג 1, הגוף אינו מפרק כראוי רכיבי בניין של חלבון מסוימים, ובעיקר את חומצת האמינו ליזין. אנזים חסר או לקוי הנקרא גלוטאיל-CoA דהידרוגנאז יוצר פקק מטבולי, שגורם להצטברות של חומצה גלוטארית וחומרים קשורים. חומרים אלה רעילים במיוחד לאזורים מוחיים ספציפיים השולטים בתנועה, במיוחד בשנים הראשונות לחיים. גם כאשר ילדים מאובחנים זמן קצר לאחר הלידה ומקבלים דיאטה דלת ליזין, כשליש מהם עדיין מפתחים תסמינים נוירולוגיים חמורים, ורבים מראים בהמשך לבן (white matter) ותפקוד כלייתי מתדרדרים.
מקום חדש להציב מחסום
הטיפול הנוכחי מתמקד בהגבלת כמות הליזין שנכנסת למערכת ובעזרה להיחלץ מהגוף תוצרים רעילים, אך הוא אינו משנה ישירות את פעילות המסלול התקול. החוקרים שאלו שאלה מרכזית: במקום לנסות להתמודד עם הפסולת המצטברת, האם ניתן להאט את הזרימה אל תוך המסלול התקול עצמו? הם התמקדו באנזים נוסף הנקרא אמינואדיפטאלדהיד סינתאז (aminoadipate-semialdehyde synthase), המבצע את שני הצעדים הראשונים באחד ממסלולי פירוק הליזין העיקריים. אנשים בעלי חוסר טבעי באנזים זה בדרך כלל מציגים רמות ליזין גבוהות אך מעט או ללא תסמינים בריאותיים, מה שמרמז כי חסימתו עשויה להיות יחסית בטוחה.
בוחנים את הרעיון בעכברים מהונדסים
כדי לבדוק אסטרטגיה זו, הצוות השתמש בעכברים שעברו הכלאה חסרת גלוטאיל-CoA דהידרוגנאז, מודל מבוסס למחלה האנושית. בעלי חיים אלה צוברים כמות גדולה של חומצות רעילות ברקמותיהם, וכאשר נחשפים לתזונה עשירה בליזין הם מפתחים רעידות, בעיות תנועה, נזק מוחי ולעתים מתים. לאחר מכן יצרו החוקרים עכבר כפול knock-out שאיבד גם את האנזים המחלה וגם את אמינואדיפטאלדהיד סינתאז. בתנאי תזונה סטנדרטיים, עכברים כפולי ה-knockout נראו והתנהגו כחיות בריאות במגוון רחב של מבחנים, ולא הראו אלא חריגויות ביוכימיות קלות.
פחות הצטברות רעילה ובריאות מוחית משופרת
המבחן האמיתי בא כאשר שני סוגי עכברי המודל הושמו על דיאטה עתירת ליזין שנועדה ללחוץ על המסלול הפגיע. עכברים שאיבדו רק את אנזים המחלה צברו רמות גבוהות מאוד של חומצות רעילות במוח, בכבד, בכליה, בדם ובשתן, ורבים מהם פיתחו תסמינים נוירולוגיים קשים, פרכוסים ואובדן משקל. לעומת זאת, בעלי החיים הכפולים הראו רמות חומצה גלוטארית נמוכות בהרבה בכל הרקמות הללו, מעט סימני מחלה והתנהגות כמעט תקינה. בדיקה מיקרוסקופית של מוחם הראתה שהוואקולות הקטנטנות והשינויים המבניים שזוהו בעכברי ה-single knockout הופחתו במידה ניכרת או נעדרו בעכברי ה-double knockout. חשוב לציין שהבדיקות המפורטות של הרכב הגוף, צפיפות העצם, תפקוד הלב, סמני חיסון וכימיה בדם לא מצאו בעיות לא-נירולוגיות משמעותיות הנגרמות על ידי חסימת השלב המוקדם הזה בפירוק הליזין.
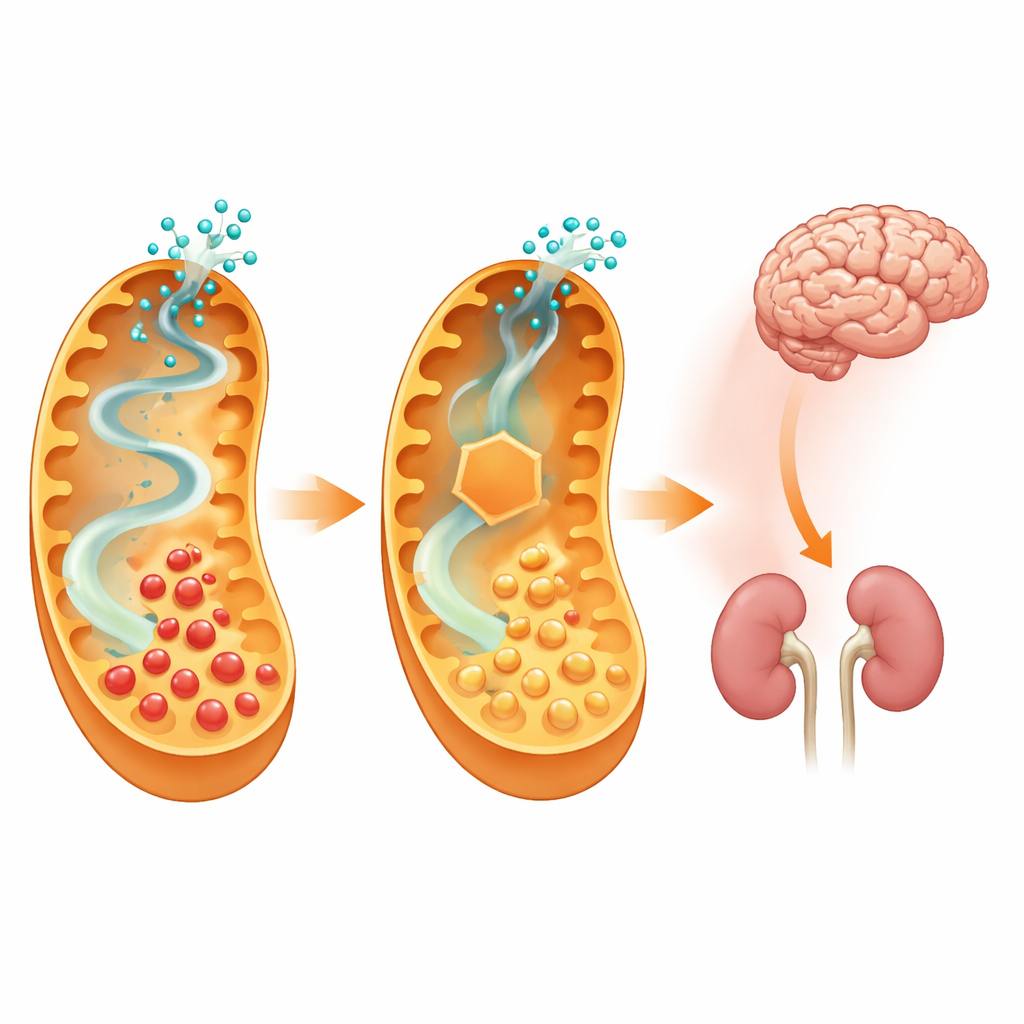
מה משמעות הדבר לטיפולים עתידיים
על ידי סגירת צעד ראשון במסלול ליזין מסוים, הצליחו החוקרים להפחית את חשיפת המוח למטבוליטים רעילים ולהגן ברובו על עכברים מהתלקחות מחלה קשה המועדת על ידי דיאטה, ללא יצירת בעיות בריאותיות חדשות ברורות. ממצא זה מצביע על כך שתרופות המיועדות לעכב באופן חלקי את אמינואדיפטאלדהיד סינתאז עשויות להציע כלי חזק חדש לצד דיאטה וטיפולים אחרים לילדים עם תסמונת החומצה הגלוטארית סוג 1. למרות שהעבודה הנוכחית נשענת על הנדסה גנטית בעכברים, וכי יש לפתח תרופות מתאימות ולבדוק את בטיחותן בבני אדם, המחקר מספק הוכחת עיקרון חזקה לכך שיחסית ממוקדת שליטה בכימיה מעלה יכולה לעצב מחדש את מהלך מחלת מוח מטבולית הרסנית.
ציטוט: Saad, C., Jung-Klawitter, S., Dimitrov, B. et al. Aminoadipate-semialdehyde synthase, a potential target for substrate reduction therapy in glutaric aciduria type 1. Sci Rep 16, 10995 (2026). https://doi.org/10.1038/s41598-026-44377-9
מילות מפתח: תסמונת החומצה הגלוטארית סוג 1, חילוף חומרים של ליזין, טיפול בהפחתת מצע, עיכוב AASS, הפרעות מטבוליות תורשתיות