Clear Sky Science · ru
Аминоадипат-семигальдегид-синтаза — потенциальная мишень для терапии снижения субстрата при глаутаровой ацидурии типа 1
Почему это редкое детское заболевание важно
Глутаровая ацидурия типа 1 — редкое наследственное заболевание, которое в основном поражает младенцев и маленьких детей, но оно иллюстрирует более общую идею: как изменение одного шага в биохимии организма может защитить мозг от пожизненного повреждения. Несмотря на современный скрининг новорождённых и строгие диеты, многие дети с этим заболеванием всё равно развивают нарушения движений, изменения в мозге и проблемы с почками. В этом исследовании рассматривается новый способ прекратить образование вредных веществ у источника, используя стратегию, называемую терапией снижения субстрата, и проверяется, может ли она привести к более безопасным и эффективным методам лечения.
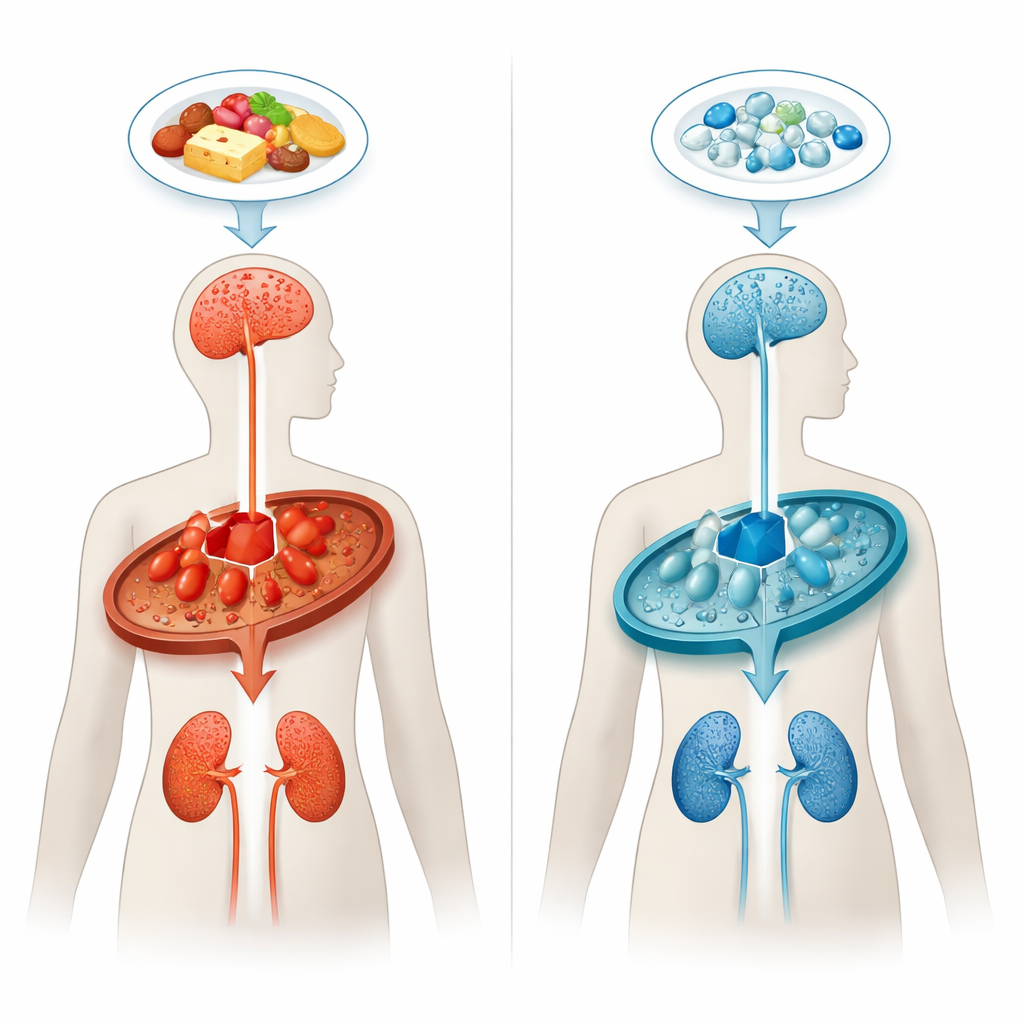
Транспортная пробка в биохимии организма
При глутаровой ацидурии типа 1 организм не может правильно разлагать некоторые строительные блоки белков, особенно аминокислоту лизин. Отсутствие или дефект фермента глутарил-СоА-дегидрогеназы вызывает метаболическую «пробку», приводящую к накоплению глутаровой кислоты и родственных соединений. Эти вещества особенно токсичны для определённых областей мозга, ответственных за контроль движений, особенно в раннем детстве. Даже если детей выявляют вскоре после рождения и переводят на специальную диету с низким содержанием лизина, примерно каждый третий всё равно развивается серьёзные неврологические симптомы, и у многих со временем прогрессируют поражения белого вещества и почечные проблемы.
Новое место для установки заграждения
Текущее лечение направлено на ограничение поступления лизина и помощь организму в удалении токсичных побочных продуктов, но оно не изменяет непосредственно работу повреждённого пути. Исследователи задали ключевой вопрос: вместо попыток справиться с накапливающимися отходами, можно ли замедлить приток в сам дефектный путь? Они сосредоточились на другом ферменте — аминоадипат-семигальдегид-синтазе, который осуществляет первые два шага в одном из основных путей распада лизина. Люди с естественным дефицитом этого фермента обычно имеют высокие уровни лизина, но небольшие или вовсе отсутствующие проблемы со здоровьем, что говорит о том, что его блокада может быть относительно безопасной.
Тестирование идеи на генетически модифицированных мышах
Чтобы проверить эту стратегию, команда использовала мышей, лишённых глутарил-СоА-дегидрогеназы, хорошо установленную модель человеческого заболевания. Эти животные накапливают большие количества токсичных кислот в тканях и при нагрузке диетой с высоким содержанием лизина развивают судороги, двигательные расстройства, повреждение мозга и часто гибнут. Затем исследователи создали двойных нокаутов — мышей, лишённых обоих ферментов: и фермента болезни, и аминоадипат-семигальдегид-синтазы. При стандартном кормлении эти двойные нокауты выглядели и вели себя как здоровые животные во многих тестах, при этом проявляя лишь незначительные биохимические отклонения.
Меньше токсичного накопления и лучшая сохранность мозга
Реальное испытание последовало, когда оба типа моделей заболевания подвергли диете с высоким содержанием лизина, призванной нагрузить уязвимый путь. Мыши, лишённые только фермента болезни, накапливали очень высокие уровни токсичных кислот в мозге, печени, почках, крови и моче, у многих развивались тяжёлые неврологические симптомы, судороги и потеря веса. Напротив, у двойных нокаутов уровни глутаровой кислоты во всех этих тканях были драматически ниже, признаков болезни было намного меньше, а поведение близко к нормальному. Микроскопическое исследование их мозгов показало, что мелкие вакуоли и структурные изменения, наблюдаемые у одиночных нокаутов, были значительно снижены или отсутствовали у двойных нокаутов. Важно, что детальные проверки состава тела, плотности костной ткани, функции сердца, иммунных маркеров и биохимии крови не выявили серьёзных вне-нервных проблем, вызванных блокированием этого раннего шага распада лизина.
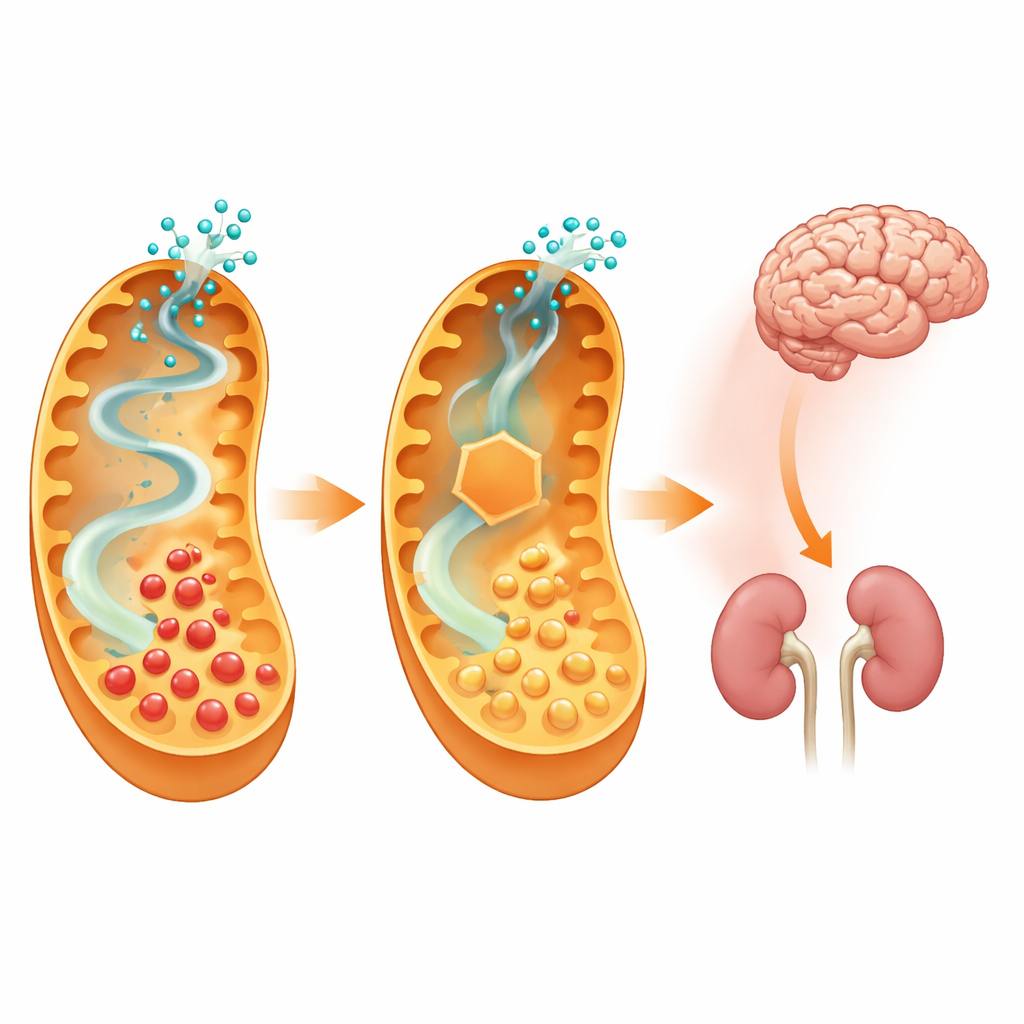
Что это означает для будущих методов лечения
Отключив первый шаг в специфическом пути распада лизина, исследователи смогли снизить воздействие токсичных метаболитов на мозг и во многом защитить мышей от тяжёлого приступа болезни, вызванного диетой, без очевидных новых проблем со здоровьем. Это говорит о том, что препараты, разработанные для частичной ингибиции аминоадипат-семигальдегид-синтазы, могут стать мощным дополнением к диете и другим методам лечения детей с глутаровой ацидурией типа 1. Хотя нынешняя работа основана на генетической модификации мышей, и подходящие лекарства всё ещё предстоит разработать и проверить на безопасность у людей, исследование предоставляет сильное доказательство принципа: целенаправленная блокада вышестоящей химии может изменить течение разрушительного метаболического заболевания мозга.
Цитирование: Saad, C., Jung-Klawitter, S., Dimitrov, B. et al. Aminoadipate-semialdehyde synthase, a potential target for substrate reduction therapy in glutaric aciduria type 1. Sci Rep 16, 10995 (2026). https://doi.org/10.1038/s41598-026-44377-9
Ключевые слова: глутаровая ацидурия типа 1, метаболизм лизина, терапия снижения субстрата, ингибирование AASS, наследственные метаболические заболевания