Clear Sky Science · nl
Aminoadipaat-semialdehyde-synthase, een potentiële doelwit voor substraatreductietherapie bij glutarische acidurie type 1
Waarom deze zeldzame kinderziekte ertoe doet
Glutarische acidurie type 1 is een zeldzame erfelijke aandoening die vooral zuigelingen en jonge kinderen treft, maar illustreert een veel breder idee: hoe het bijsturen van een enkele stap in de biochemie van het lichaam de hersenen kan beschermen tegen levenslange schade. Ondanks moderne hielprikscreening en zorgvuldig dieet ontwikkelen veel kinderen met deze aandoening toch bewegingsstoornissen, hersenveranderingen en nierproblemen. Deze studie onderzoekt een nieuwe manier om de productie van schadelijke stoffen bij de bron te stoppen, met een strategie die substraatreductietherapie wordt genoemd, en test of dat kan leiden tot veiliger en effectievere behandelingen.
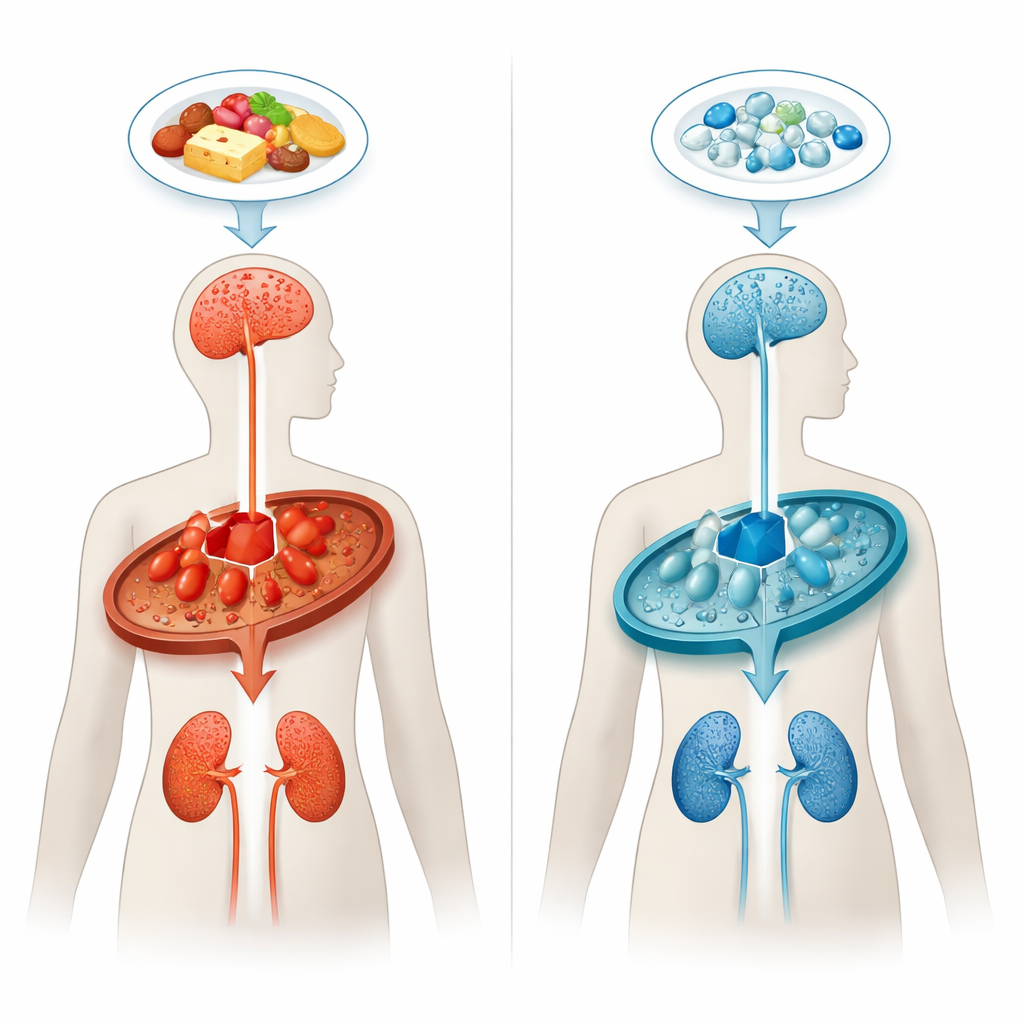
Een verkeersopstopping in de biochemie van het lichaam
Bij glutarische acidurie type 1 kan het lichaam bepaalde bouwstenen van eiwitten, met name het aminozuur lysine, niet goed afbreken. Een ontbrekend of defect enzym, bekend als glutaryl-CoA-dehydrogenase, veroorzaakt een metabole verkeersopstopping, wat leidt tot ophoping van glutarinezuur en verwante verbindingen. Deze stoffen zijn bijzonder toxisch voor specifieke hersengebieden die de beweging regelen, vooral vroeg in het leven. Zelfs wanneer kinderen kort na de geboorte worden opgespoord en op een speciaal lysinearm dieet worden gezet, ontwikkelt ongeveer één op de drie nog steeds ernstige neurologische symptomen, en velen tonen na verloop van tijd progressieve witte-stofveranderingen en nierproblemen.
Een nieuwe plek om een blokkade op te werpen
De huidige behandeling richt zich op het beperken van de hoeveelheid lysine die het lichaam binnenkomt en op het helpen verwijderen van toxische bijproducten, maar verandert de foutieve route niet rechtstreeks. De onderzoekers stelden een cruciale vraag: in plaats van te proberen het zich ophopende afval te verwerken, konden ze de toevoer naar de defecte route zelf vertragen? Ze richtten zich op een ander enzym, aminoadipaat-semialdehyde-synthase, dat de eerste twee stappen uitvoert in een van de belangrijkste lysineafbraakroutes. Mensen die van nature dit enzym missen hebben doorgaans hoge lysinewaarden maar weinig of geen gezondheidsproblemen, wat suggereert dat het blokkeren ervan relatief veilig zou kunnen zijn.
Het idee testen in genetisch aangepaste muizen
Om deze strategie te onderzoeken gebruikten de onderzoekers muizen die geen glutaryl-CoA-dehydrogenase bezaten, een goed vastgesteld model van de menselijke ziekte. Deze dieren hopen grote hoeveelheden toxische zuren op in hun weefsels en, wanneer ze een lysinerijk dieet krijgen, ontwikkelen ze aanvallen, bewegingsproblemen, hersenschade en sterven vaak. De onderzoekers creëerden vervolgens een dubbel knock-outmuismodel dat zowel het ziekte-enzym als aminoadipaat-semialdehyde-synthase miste. Onder standaardvoeding gedroegen deze dubbel knock-outmuizen zich in een breed scala aan tests als gezonde dieren, terwijl ze slechts milde biochemische afwijkingen vertoonden.
Minder toxische ophoping en betere hersengezondheid
De echte proef kwam toen beide typen ziektemuizen werden blootgesteld aan een lysinerijk dieet bedoeld om de kwetsbare route te belasten. Muizen die slechts het ziekte-enzym misten stapelden zeer hoge niveaus toxische zuren op in hersenen, lever, nieren, bloed en urine, en velen ontwikkelden ernstige neurologische symptomen, aanvallen en gewichtsverlies. Daarentegen hadden de dubbel knock-outdieren dramatisch lagere concentraties glutarinezuur in al deze weefsels, veel minder ziekteverschijnselen en vrijwel normaal gedrag. Microscopisch onderzoek van hun hersenen toonde dat de kleine vacuolen en structurele veranderingen die bij de enkelvoudige knock-outs werden gezien, sterk verminderd of afwezig waren bij de dubbel knock-outs. Belangrijk is dat gedetailleerde controles van lichaamssamenstelling, botdichtheid, hartfunctie, immuunsignalen en bloedchemie geen grote niet-neurologische problemen vonden die werden veroorzaakt door het blokkeren van deze vroege stap in de lysineafbraak.
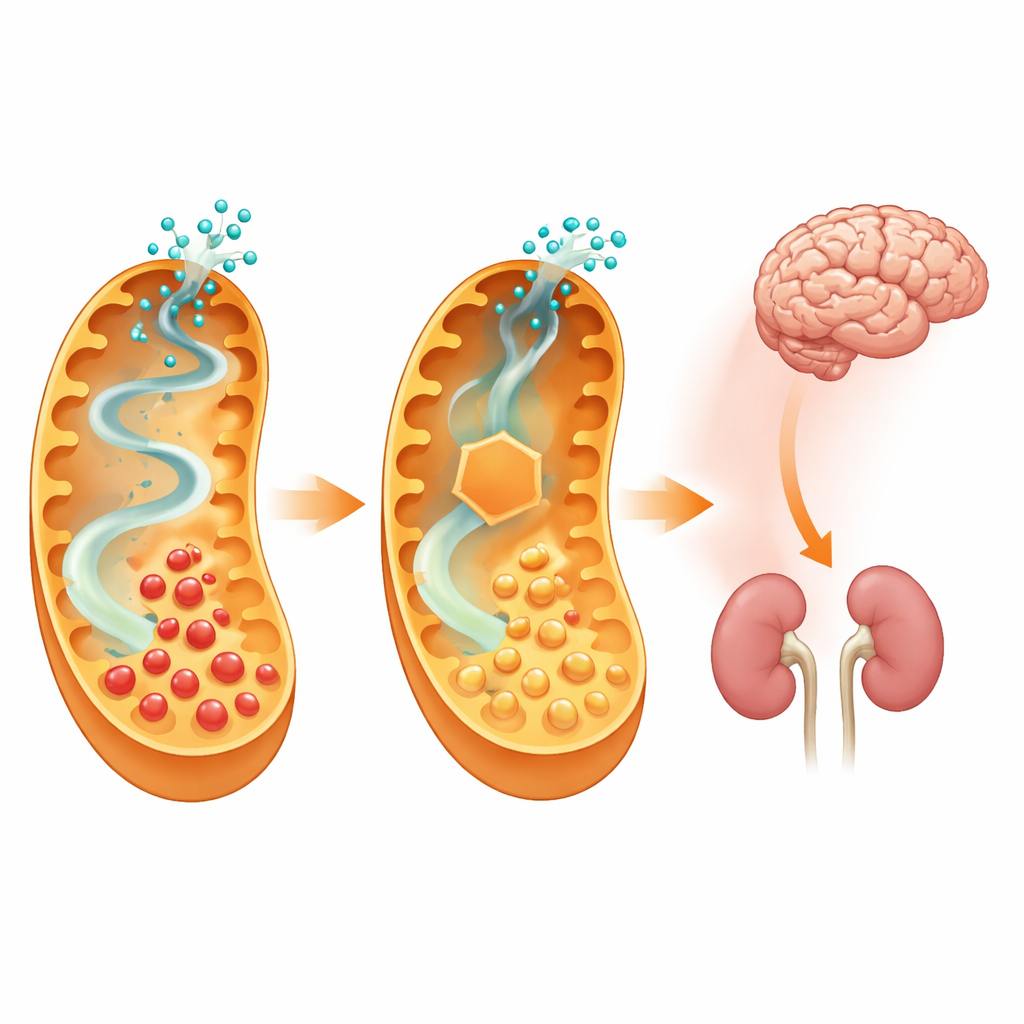
Wat dit betekent voor toekomstige behandelingen
Door de eerste stap van een specifieke lysineroute stil te leggen konden de onderzoekers de blootstelling van de hersenen aan toxische metabolieten verlagen en muizen grotendeels beschermen tegen een ernstige, dieet-geïnduceerde ziekteopvlamming, zonder duidelijke nieuwe gezondheidsproblemen te veroorzaken. Dit suggereert dat geneesmiddelen die aminoadipaat-semialdehyde-synthase gedeeltelijk remmen een krachtig nieuw hulpmiddel zouden kunnen vormen naast dieet en andere behandelingen voor kinderen met glutarische acidurie type 1. Hoewel het huidige werk steunt op genetische manipulatie in muizen, en geschikte medicijnen nog ontwikkeld en op veiligheid in mensen getest moeten worden, levert de studie sterk bewijs dat zorgvuldig gerichte blokkade van upstream-biochemie het beloop van een verwoestende metabole hersenziekte kan veranderen.
Bronvermelding: Saad, C., Jung-Klawitter, S., Dimitrov, B. et al. Aminoadipate-semialdehyde synthase, a potential target for substrate reduction therapy in glutaric aciduria type 1. Sci Rep 16, 10995 (2026). https://doi.org/10.1038/s41598-026-44377-9
Trefwoorden: glutarische acidurie type 1, lysinemetabolisme, substraatreductietherapie, AASS-remming, aangeboren stofwisselingsziekten