Clear Sky Science · ar
أمينوأديبات-سيميالدهيد سينثاز، هدف محتمل لعلاج تخفيض الركيزة في حُماضة الجلوتاريك من النوع الأول
لماذا هذه الحالة الطفيلية النادرة مهمة
حُماضة الجلوتاريك من النوع الأول هي اضطراب وراثي نادر يؤثر أساساً على الرُّضَّع والأطفال الصغار، لكنها تجسّد فكرة أوسع: كيف أن تعديل خطوة واحدة في كيمياء الجسم يمكن أن يحمي الدماغ من تلف دائم. بالرغم من فحوصات المواليد الحديثة والأنظمة الغذائية الدقيقة، فإن العديد من الأطفال المصابين بهذه الحالة ما يزالون يطوّرون مشاكل حركية وتغيرات دماغية ومشكلات كلوية. تبحث هذه الدراسة طريقة جديدة لقطع إنتاج المواد الضارة من مصدرها، باستخدام استراتيجية تسمى علاج تخفيض الركيزة، وتختبر ما إذا كان بإمكانها أن تؤدي إلى علاجات أكثر أماناً وفاعلية.
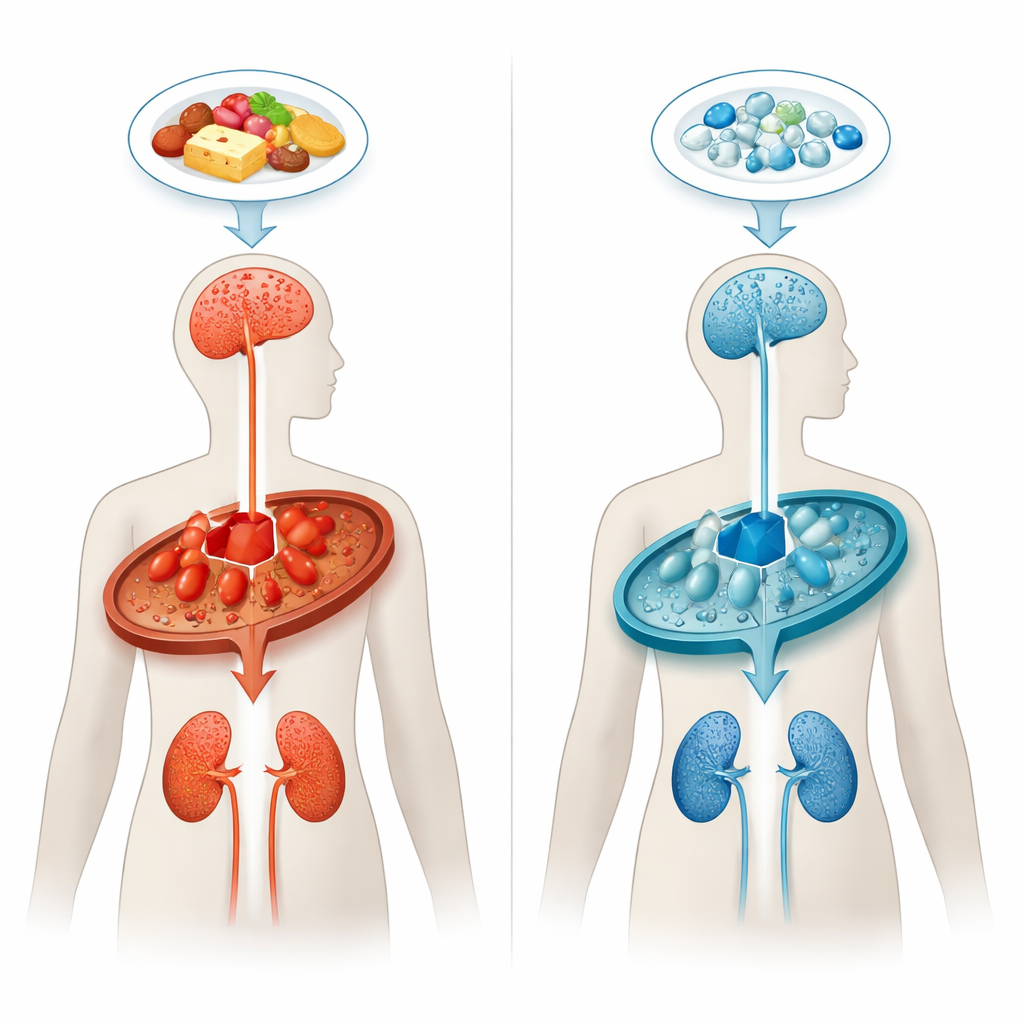
اختناق مروري في كيمياء الجسم
في حُماضة الجلوتاريك من النوع الأول، لا يستطيع الجسم تفكيك بعض وحدات بناء البروتين بشكل صحيح، خصوصاً حمض الأمين الليسين. إن نقص أو خللاً في الإنزيم المعروف باسم غلوتاريل-كوإنزيم A ديهيدروجيناز يسبب ازدحاماً استقلابياً، يؤدي إلى تراكم حمض الجلوتاريك ومركبات ذات صلة. هذه المواد سامة بشكل خاص لمناطق دماغية محددة تساعد على التحكم في الحركة، لا سيما في المراحل المبكرة من الحياة. حتى عندما يُكتشف الأطفال بعد الولادة ويوضعون على أنظمة غذائية منخفضة الليسين، فإن حوالي واحد من كل ثلاثة لا يزال يطوّر أعراضاً عصبية خطيرة، وكثيرون يظهر لديهم تدهور في المادة البيضاء ومشكلات كلوية مع تقدم العمر.
مكان جديد لوضع حاجز
يركز العلاج الحالي على الحد من كمية الليسين التي تدخل الجسم ومساعدة إزالة النواتج السامة، لكنه لا يغير مباشرةً طريقة عمل المسار المُعيب. طرح الباحثون سؤالاً رئيسياً: بدلاً من محاولة التعامل مع النفايات المتراكمة، هل يمكننا إبطاء مدخلات المسار المعيب نفسه؟ ركّزوا على إنزيم آخر يُدعى أمينوأديبات-سيميالدهيد سينثاز، الذي يؤدي أول خطوتين في أحد المسارات الرئيسية لتحلل الليسين. الأشخاص الذين يفتقرون طبيعياً إلى هذا الإنزيم عادة ما تكون لديهم مستويات عالية من الليسين لكن قليل من المشاكل الصحية أو من دونها، ما يشير إلى أن حظراً عليه قد يكون آمناً نسبياً.
اختبار الفكرة في فئران مُهندَسة
لاختبار هذه الاستراتيجية، استخدم الفريق فئراناً مُهندَسة تفتقر إلى غلوتاريل-كوإنزيم A ديهيدروجيناز، وهو نموذج راسخ لمرض الإنسان. تتراكم لدى هذه الحيوانات كميات كبيرة من الأحماض السامة في أنسجتها، وعندما تُعرّض لنظام غذائي غني بالليسين تُصاب بالتشنجات، ومشاكل حركية، وتلف دماغي، وغالباً ما تموت. ثم أنشأ الباحثون فئراناً مُبطَّلة مزدوجة افتقرت إلى كل من إنزيم المرض وأمينوأديبات-سيميالدهيد سينثاز. تحت ظروف التغذية القياسية، بدا أن هذه الفئران المبطلة المزدوجة تشبه الحيوانات الصحية في مجموعة واسعة من الاختبارات، بينما أظهرت فقط شذوذات بيوكيميائية طفيفة.
تراكم سام أقل وصحة دماغية أفضل
جاء الاختبار الحقيقي عندما عُرِضت كلا المجموعتين من نماذج المرض لنظام غذائي عالي الليسين مصمم لإجهاد المسار الضعيف. الفئران التي تفتقد الإنزيم المسبب للمرض فقط تراكمت لديها مستويات مرتفعة جداً من الأحماض السامة في الدماغ والكبد والكلى والدم والبول، وكثير منها طوّر أعراضاً عصبية شديدة، وتشنجات، وفقدان وزن. في المقابل، كانت لدى الحيوانات المبطلة المزدوجة مستويات حمض الجلوتاريك أقل بكثير في جميع هذه الأنسجة، وكانت أعراض المرض أقل بكثير وسلوكها شبه طبيعي. أظهر الفحص المجهري لأدمغتها أن الحجيرات الصغيرة والتغيرات البنائية التي لوحظت في الفئران المبطلة المفردة قد تقلصت أو اختفت في المبطلات المزدوجة. ومن المهم أن الفحوص التفصيلية لتركيب الجسم، وكثافة العظام، ووظيفة القلب، وعلامات المناعة، وكيمياء الدم لم تكشف عن مشاكل غير عصبية رئيسية ناجمة عن حجب هذه الخطوة المبكرة في تحلل الليسين.
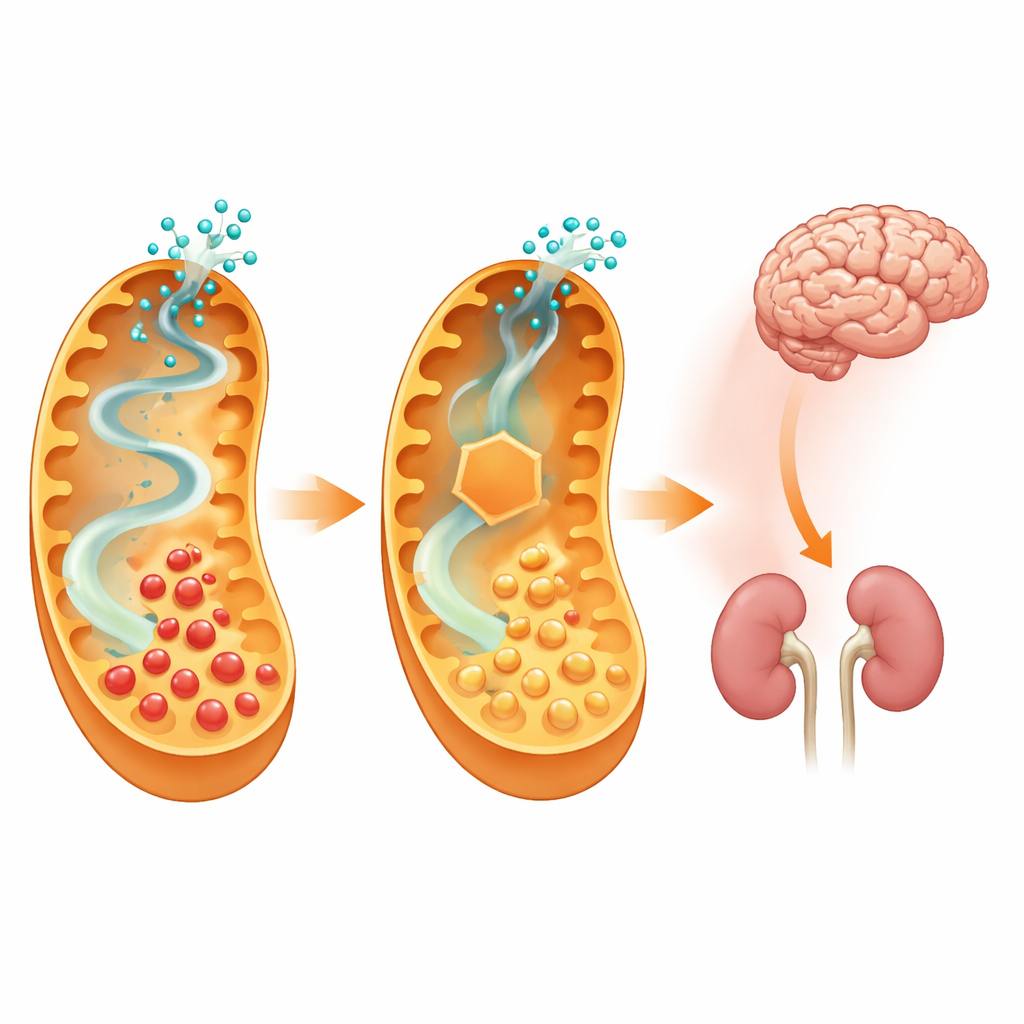
ماذا يعني هذا للعلاجات المستقبلية
بإغلاق الخطوة الأولى في مسار محدد لتحلل الليسين، استطاع الباحثون تقليل تعرض الدماغ للمواد الأيضية السامة وحماية الفئران إلى حد كبير من نوبة مرضية شديدة مثارة بالنظام الغذائي، دون التسبب في مشكلات صحية واضحة جديدة. يشير ذلك إلى أن أدوية مُصمَّمة لتثبيط أمينوأديبات-سيميالدهيد سينثاز جزئياً قد توفر أداة قوية جديدة إلى جانب الحمية والعلاجات الأخرى للأطفال المصابين بحُماضة الجلوتاريك من النوع الأول. وعلى الرغم من أن العمل الحالي يعتمد على هندسة وراثية في الفئران، وأنه لا تزال هناك حاجة لتطوير أدوية مناسبة واختبار سلامتها لدى البشر، فإن الدراسة تقدم دليلاً قوياً على المبدأ أن حجب الكيمياء المبكرة المستهدف بعناية يمكن أن يعيد تشكيل مسار مرض دماغي أيضي مدمّر.
الاستشهاد: Saad, C., Jung-Klawitter, S., Dimitrov, B. et al. Aminoadipate-semialdehyde synthase, a potential target for substrate reduction therapy in glutaric aciduria type 1. Sci Rep 16, 10995 (2026). https://doi.org/10.1038/s41598-026-44377-9
الكلمات المفتاحية: حُماضة الجلوتاريك من النوع الأول, استقلاب الليسين, علاج تخفيض الركيزة, مثبطات AASS, الاضطرابات الأيضية الوراثية