Clear Sky Science · zh
巨噬细胞中的 ID1 通过增强 NF-κB/NPM1/SHP1/SHP2 信号诱导的 M2 极化促进非小细胞癌进展
为何身体的防御者会变成肺癌的帮手
肺癌仍是全球最致命的癌症之一,部分原因在于许多肿瘤学会躲避甚至利用人体自身的免疫系统。本研究关注一类聚集在肺肿瘤内的特殊免疫细胞,并提出了一个简单而关键的问题:是什么促使这些细胞从抗癌转变为助癌?理解这一转变可能为新的治疗策略打开大门——这些策略不是直接攻击肿瘤,而是重新训练免疫系统。
会“倒戈”的免疫细胞
每个肿瘤内部都有一个由非癌细胞组成的繁忙社区,称为肿瘤微环境。其中最重要的居民之一是巨噬细胞,这类免疫细胞通常负责吞噬病原体和清理损伤组织。在肺肿瘤中,许多这类被称为肿瘤相关巨噬细胞(TAMs)的细胞进入一种所谓的“M2”状态,该状态抑制炎症、修复组织,但不幸的是也滋养癌细胞。患有非小细胞肺癌的患者往往富含这类 M2 型巨噬细胞,这与肿瘤快速生长、转移和对治疗反应差相关。
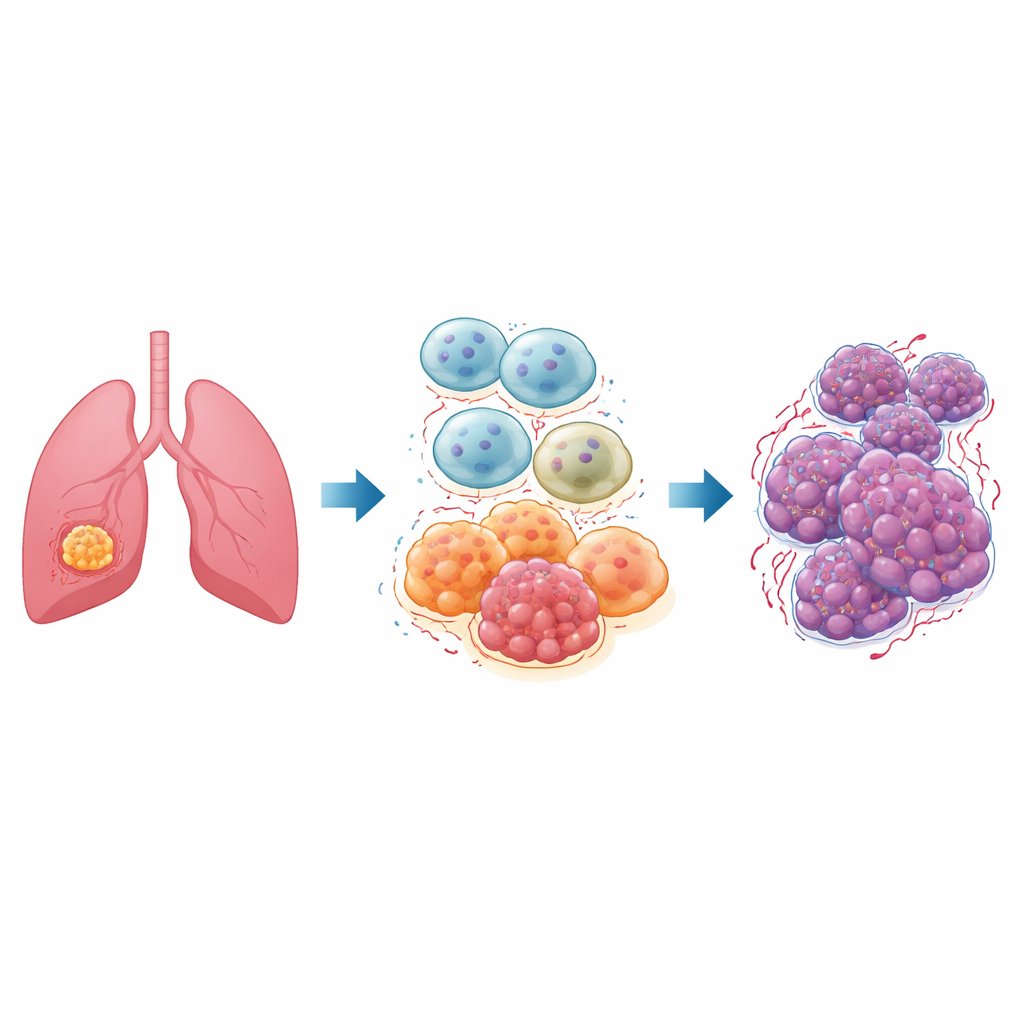
名为 ID1 的主控开关
研究人员聚焦于一种名为 ID1 的蛋白,该蛋白已知能推动多种癌症向更具侵袭性的表型发展。他们怀疑肿瘤相关巨噬细胞中的 ID1 有助于将这些细胞引导为支持癌症的 M2 状态。研究者首先利用公开的基因数据库显示,在肺癌样本中 ID1 水平与一个关键调控因子 NF-κB 同步升高,提示这些分子可能协同工作。随后他们构建了人体巨噬细胞的实验模型,使用遗传工具和药物来增强 ID1 或抑制 NF-κB,并仔细追踪这一链中其他分子的变化。
ID1 如何重编程巨噬细胞
在这些巨噬细胞中,较高的 ID1 水平激活了 NF-κB 和另一种蛋白 NPM1,两者共同激活了一对酶 SHP1 和 SHP2。这一连锁反应促使 NF-κB 亚基进入细胞核,在那里开启有利于 M2 样状态的基因表达。结果,巨噬细胞开始产生更多诸如 IL‑4、IL‑10、精氨酸酶‑1(arginase‑1)、CD206 以及若干组织蛋白酶(cathepsins)等物质——这些分子已知能抑制抗肿瘤免疫、重塑组织并使癌细胞更易迁移和侵袭。当研究人员通过抑制 NF‑κB 或精细调控 NPM1 来中断这一信号时,SHP1、SHP2 及这些与 M2 相关物质的水平下降,巨噬细胞的促肿瘤特征也随之减弱。
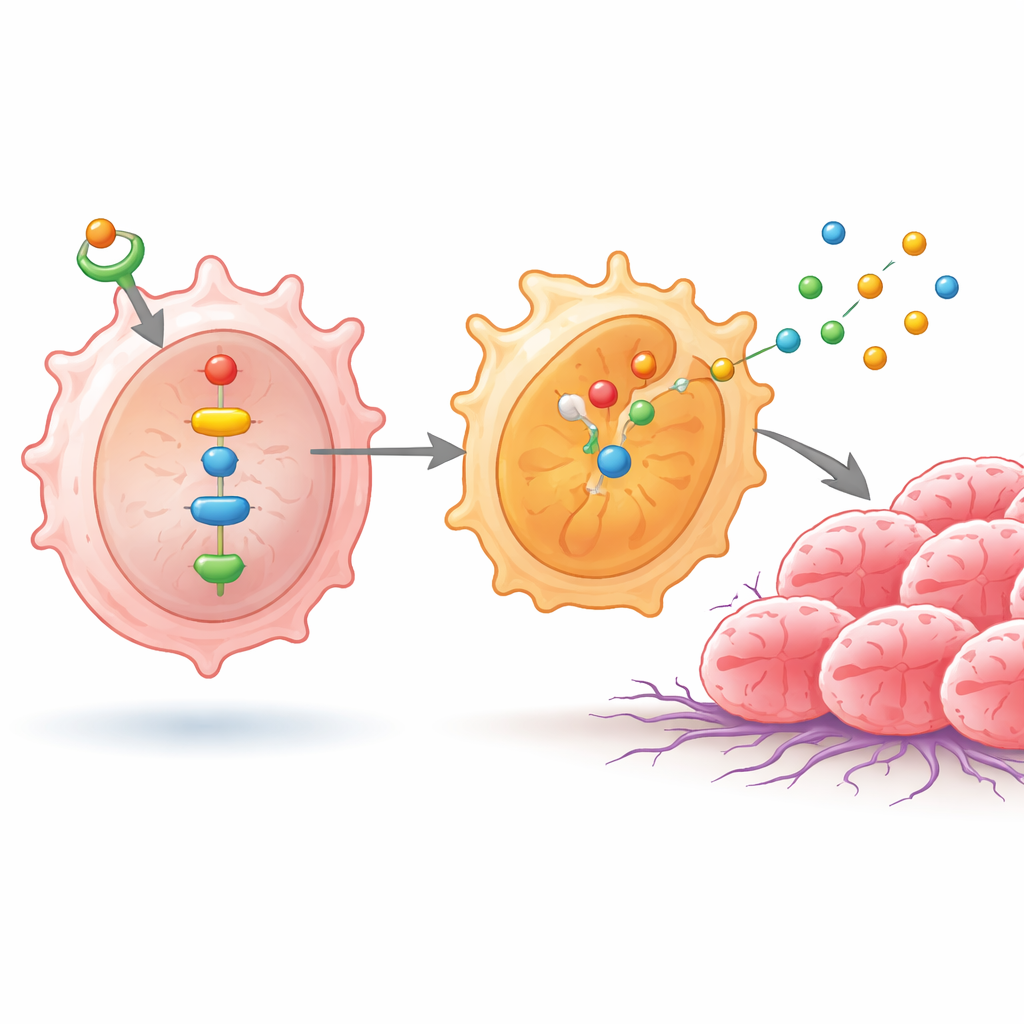
被重编程的巨噬细胞如何促进肿瘤生长
为观察这些免疫变化如何影响癌细胞,团队将经过不同处理的巨噬细胞与肺癌细胞系共同培养。当 ID1 水平较高且信号链完整时,癌细胞增殖更快,穿过人工屏障的迁移能力更强——这些都是与体内转移相关的行为。当阻断 NF‑κB 时,这些侵袭性特征减弱,但若强制激活 NPM1,侵袭性又会恢复,强调了该通路的重要性。研究人员随后在小鼠体内进行实验,将肺癌细胞与处理过的巨噬细胞混合皮下接种。伴随高 ID1、M2 样巨噬细胞的肿瘤体积和重量更大,而与通路被阻断的巨噬细胞共同接种的肿瘤则较小。对人类肺肿瘤样本的检测也显示,与相邻非癌组织相比,肿瘤中 ID1 和活化的 NF‑κB 水平更高,将实验室发现与真实患者状况联系起来。
这对未来肺癌治疗意味着什么
总体而言,这项研究将 ID1 描绘为一个重要的“主控开关”,它促使原本有益的免疫细胞成为肺癌的沉默同谋。通过经由 NF‑κB、NPM1 与 SHP1/SHP2 的事件链,ID1 将巨噬细胞推向抑制免疫攻击并释放促生长因子的 M2 样状态,从而加速肿瘤进展。对患者而言,结论带来希望:未来的治疗或许不只针对癌细胞本身,而可以切断这条信号链或将巨噬细胞重新调回抗癌模式。尽管这些发现仍需在临床环境中进一步验证与优化,但它们强调了一种有前景的策略——改变肿瘤周围“社区”的行为,以放慢甚至逆转肺癌的发展。
引用: Jiang, P., Chen, Z., Cui, L. et al. ID1 in TAMs promoted the progression of non-small-cell carcinoma via increasing NF-κB/NPM1/SHP1/SHP2 signaling induced M2 polarization. Sci Rep 16, 14222 (2026). https://doi.org/10.1038/s41598-026-44075-6
关键词: 非小细胞肺癌, 肿瘤相关巨噬细胞, 免疫微环境, 巨噬细胞极化, 癌症免疫治疗