Clear Sky Science · ru
ID1 в ТАМ способствует прогрессированию немелкоклеточной карциномы за счёт усиления сигнальной цепи NF-κB/NPM1/SHP1/SHP2, индуцирующей М2-поляризацию
Почему защитники организма могут превратиться в помощников рака лёгкого
Рак лёгкого остаётся одним из самых смертоносных видов рака в мире, отчасти потому, что многие опухоли научаются скрываться от иммунной системы и даже использовать её в своих интересах. В этом исследовании рассматривается особая группа иммунных клеток, собирающихся внутри опухолей лёгкого, и задаётся простой, но важный вопрос: что заставляет эти клетки переключаться с борьбы с раком на его содействие? Понимание этого переключения может открыть путь к новым методам лечения, которые перенастраивают иммунную систему, а не только атакуют опухоль напрямую.
Иммунные клетки, меняющие сторону
Внутри каждой опухоли действует оживлённый микрорайон нераковых клеток, называемый опухолевой микросредой. Среди её ключевых жителей — макрофаги, иммунные клетки, обычно отвечающие за фагоцитоз микробов и повреждённых тканей. В опухолях лёгкого многие из этих клеток, известные как опухоль-ассоциированные макрофаги, переходят в так называемое состояние «M2», которое подавляет воспаление, восстанавливает ткани и, к сожалению, поддерживает рост рака. У пациентов с немелкоклеточным раком лёгкого, наиболее распространённой формой заболевания, часто наблюдается большое количество макрофагов типа M2, что связано с быстрым ростом опухоли, метастазированием и плохим ответом на терапию.
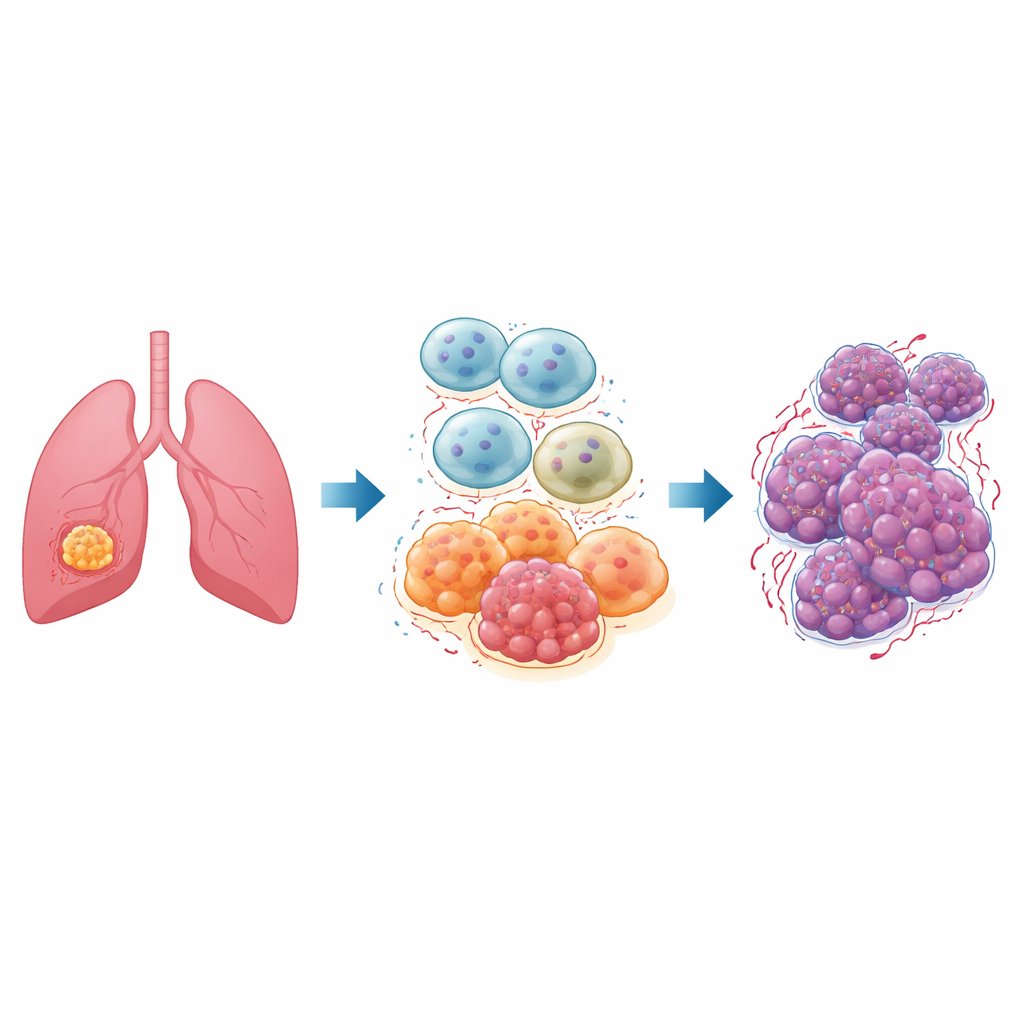
Главный переключатель под названием ID1
Исследователи сосредоточились на белке под названием ID1, уже известном способностью стимулировать более агрессивное поведение различных видов рака. Они предположили, что ID1 в опухоль-ассоциированных макрофагах помогает направлять эти клетки в их поддерживающее опухоль состояние M2. Используя публичные геномные базы данных, они сначала показали, что уровни ID1 повышаются совместно с ключевым регулятором NF-κB в образцах рака лёгкого, что намекает на их взаимодействие. Затем в лабораторных моделях человеческих макрофагов применяли генетические инструменты и препараты, чтобы либо повысить экспрессию ID1, либо заблокировать NF-κB, тщательно отслеживая изменения в других участниках той же сигнальной цепи.
Как ID1 перенастраивает макрофаги
В этих макрофагах повышенные уровни ID1 активировали NF-κB и другой белок — NPM1, которые вместе включали пару ферментов SHP1 и SHP2. Эта каскадная реакция способствовала перемещению субъединиц NF-κB в ядро клетки, где они включали гены, благоприятствующие M2-подобному состоянию. В результате макрофаги стали продуцировать больше таких веществ, как IL-4, IL-10, аргиназа-1, CD206 и несколько катепсинов — молекул, известных подавлением антитуморного иммунитета, ремоделированием тканей и облегчением миграции и инвазии раковых клеток. Когда учёные прерывали эту сигнализацию, либо блокируя NF-κB, либо изменяя активность NPM1, уровни SHP1, SHP2 и этих ассоциированных с M2 веществ снижались, и макрофаги выглядели менее «дружелюбными» к опухоли.
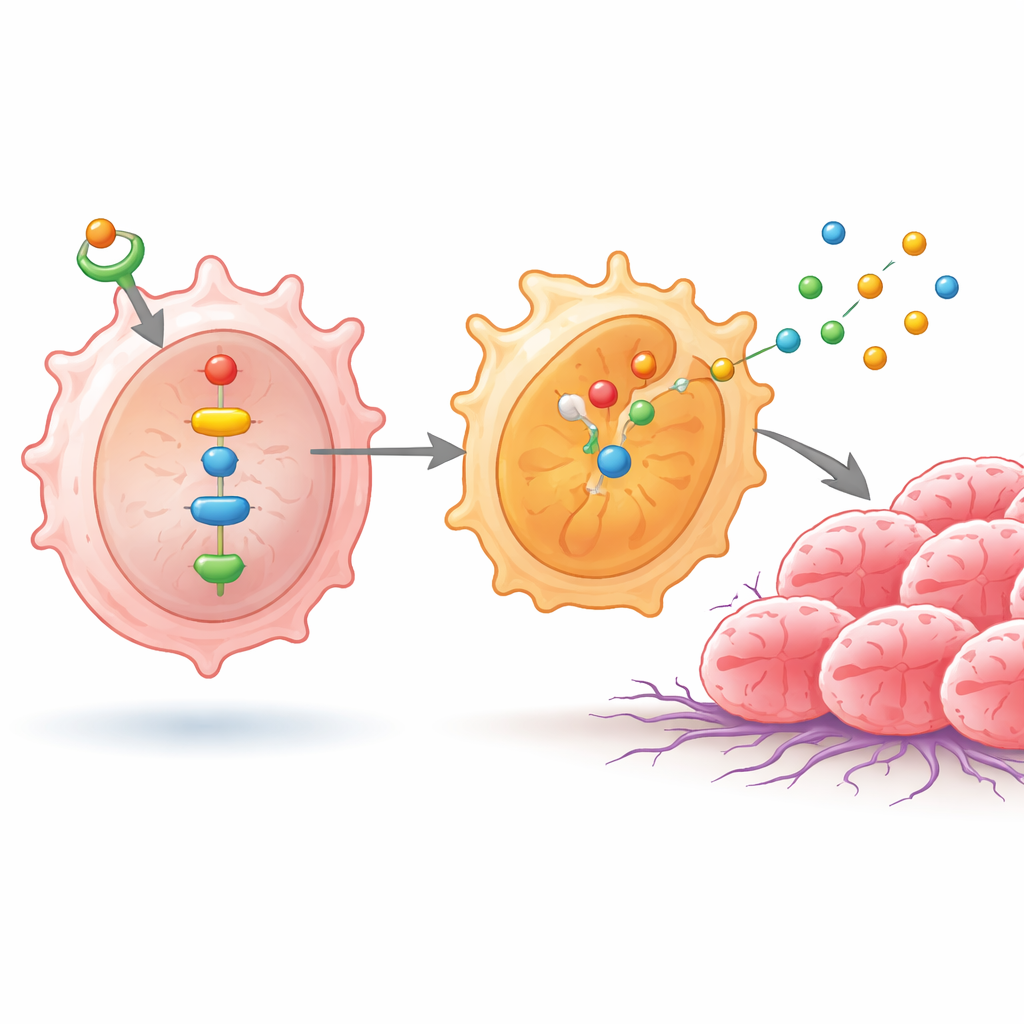
Как перепрограммированные макрофаги ускоряют рост опухоли
Чтобы выяснить, как эти иммунные изменения влияют на раковые клетки, команда выращивала линии клеток рака лёгкого совместно с макрофагами, подвергнутыми разным воздействиям. При высоком уровне ID1 и сохранённой сигнальной цепи раковые клетки делились активнее и лучше мигрировали через искусственные барьеры — поведение, связанное с метастазированием. При блокаде NF-κB агрессивные свойства ослабевали, но возвращались при принудительной активации NPM1, что подчёркивало важность этого пути. Затем исследователи перешли к опытам на мышах, имплантируя под кожу смеси раковых клеток лёгкого и обработанных макрофагов. Опухоли, сформированные в присутствии макрофагов с высоким уровнем ID1 и M2-подобным фенотипом, были крупнее и тяжелее, тогда как опухоли с макрофагами, у которых сигнальный путь был блокирован, оставались меньшими. Образцы человеческих опухолей лёгкого также продемонстрировали более высокие уровни ID1 и активированного NF-κB по сравнению с близлежащей ненарушенной тканью, связывая лабораторные находки с реальными пациентами.
Что это значит для будущего лечения рака лёгкого
В совокупности работа представила ID1 как важный «главный переключатель», способствующий превращению полезных иммунных клеток в молчаливых помощников рака лёгкого. Запуская цепь событий через NF-κB, NPM1 и SHP1/SHP2, ID1 подталкивает макрофаги к M2-подобному состоянию, которое успокаивает иммунный ответ и высвобождает факторы, способствующие росту, тем самым ускоряя прогрессирование опухоли. Для пациентов это даёт надежду: вместо того чтобы нацеливаться только на раковые клетки, будущие терапии могли бы разрывать эту сигнальную цепь или возвращать макрофагам противоопухолевую функцию. Хотя эти результаты ещё требуют проверок и доработки в клинических условиях, они подчёркивают перспективную стратегию — менять поведение «окрестностей» опухоли, чтобы замедлить или даже обратить развитие рака лёгкого.
Цитирование: Jiang, P., Chen, Z., Cui, L. et al. ID1 in TAMs promoted the progression of non-small-cell carcinoma via increasing NF-κB/NPM1/SHP1/SHP2 signaling induced M2 polarization. Sci Rep 16, 14222 (2026). https://doi.org/10.1038/s41598-026-44075-6
Ключевые слова: немелкоклеточный рак лёгкого, макрофаги, ассоциированные с опухолью, иммунная микросреда, поляризация макрофагов, иммунотерапия рака