Clear Sky Science · fr
ID1 dans les macrophages associés aux tumeurs favorise la progression du carcinome non à petites cellules en augmentant la signalisation NF-κB/NPM1/SHP1/SHP2 induisant la polarisation M2
Pourquoi les défenseurs du corps peuvent se transformer en alliés du cancer du poumon
Le cancer du poumon reste l’un des cancers les plus mortels dans le monde, en partie parce que de nombreuses tumeurs apprennent à se dissimuler à, et même à exploiter, le système immunitaire de l’organisme. Cette étude examine un groupe particulier de cellules immunitaires qui s’accumulent à l’intérieur des tumeurs pulmonaires et pose une question simple mais cruciale : qu’est-ce qui pousse ces cellules à passer de la lutte contre le cancer à son soutien ? Comprendre ce basculement pourrait ouvrir la voie à de nouveaux traitements qui réorientent le système immunitaire plutôt que de s’attaquer uniquement à la tumeur.
Des cellules immunitaires qui passent de camp
À l’intérieur de chaque tumeur se trouve un quartier animé de cellules non cancéreuses appelé microenvironnement tumoral. Parmi ses résidents les plus importants figurent les macrophages, des cellules immunitaires chargées normalement d’engloutir les germes et les tissus endommagés. Dans les tumeurs pulmonaires, bon nombre de ces cellules, connues sous le nom de macrophages associés aux tumeurs, adoptent un état dit « M2 » qui apaise l’inflammation, répare les tissus et, malheureusement, nourrit le cancer. Les patients atteints d’un cancer du poumon non à petites cellules, la forme la plus fréquente, présentent souvent une abondance de macrophages de type M2, associés à une croissance tumorale rapide, à la dissémination et à de faibles réponses aux traitements.
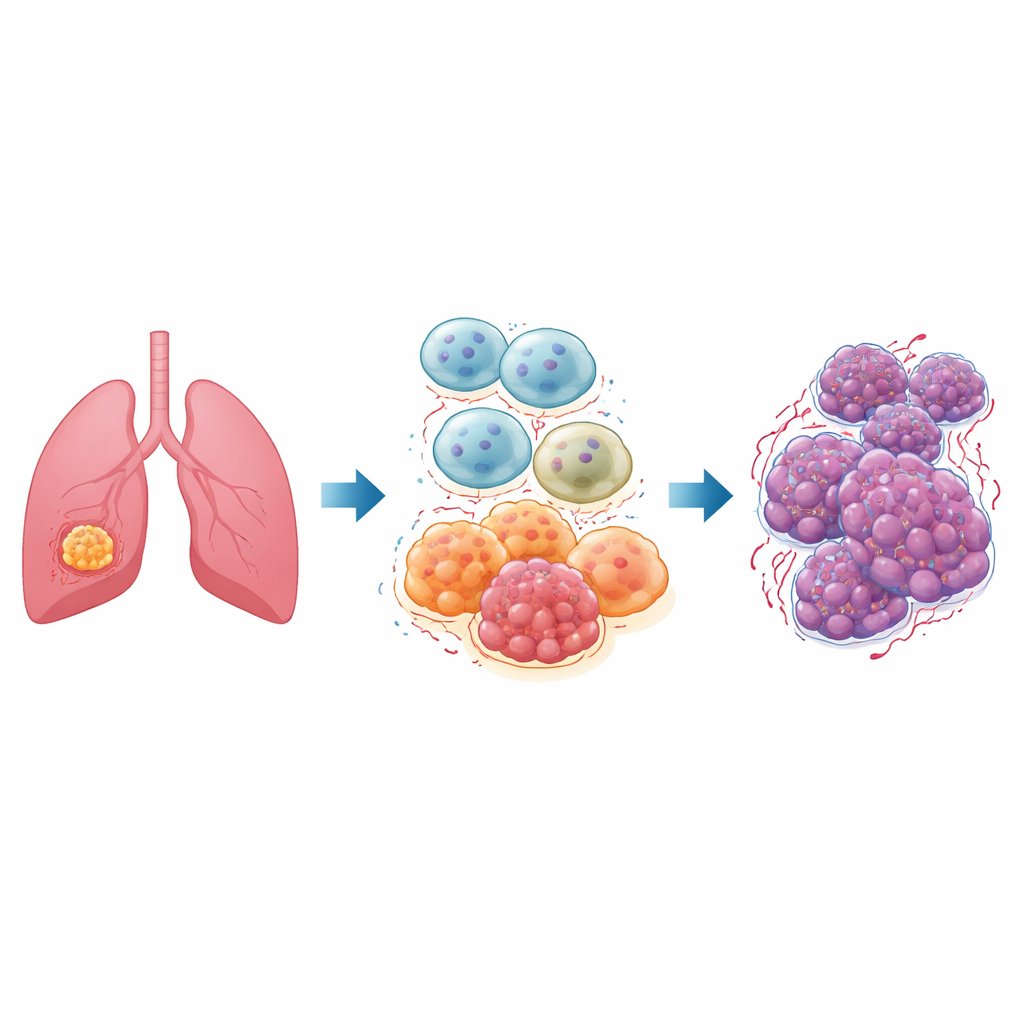
Un interrupteur maître nommé ID1
Les chercheurs se sont concentrés sur une protéine appelée ID1, déjà connue pour favoriser un comportement plus agressif de divers cancers. Ils ont émis l’hypothèse que ID1, dans les macrophages associés aux tumeurs, contribue à orienter ces cellules vers leur état pro‑tumoral M2. En utilisant des bases de données publiques de gènes, ils ont d’abord montré que les niveaux de ID1 augmentent en parallèle d’un facteur de contrôle clé appelé NF‑κB dans des échantillons de cancer du poumon, suggérant que ces molécules agissent de concert. Ils ont ensuite construit des modèles cellulaires de macrophages humains en laboratoire et utilisé des outils génétiques et des médicaments pour soit augmenter ID1, soit bloquer NF‑κB, en suivant attentivement comment cela modifiait d’autres molécules de cette même cascade.
Comment ID1 reprogramme les macrophages
Dans ces macrophages, une augmentation de ID1 a activé NF‑κB et une autre protéine, NPM1, qui ensemble ont activé une paire d’enzymes appelées SHP1 et SHP2. Cette réaction en chaîne a poussé des sous‑unités de NF‑κB dans le noyau cellulaire, où elles ont activé des gènes favorisant l’état de type M2. En conséquence, les macrophages ont commencé à produire davantage de substances telles que IL‑4, IL‑10, arginase‑1, CD206 et plusieurs cathépsines — des molécules connues pour atténuer l’immunité antitumorale, remodeler les tissus et faciliter la migration et l’invasion des cellules cancéreuses. Lorsque les scientifiques ont interrompu cette signalisation, soit en bloquant NF‑κB, soit en modulant NPM1, les niveaux de SHP1, SHP2 et de ces substances associées au phénotype M2 ont diminué, et les macrophages ont présenté un comportement moins favorable à la tumeur.
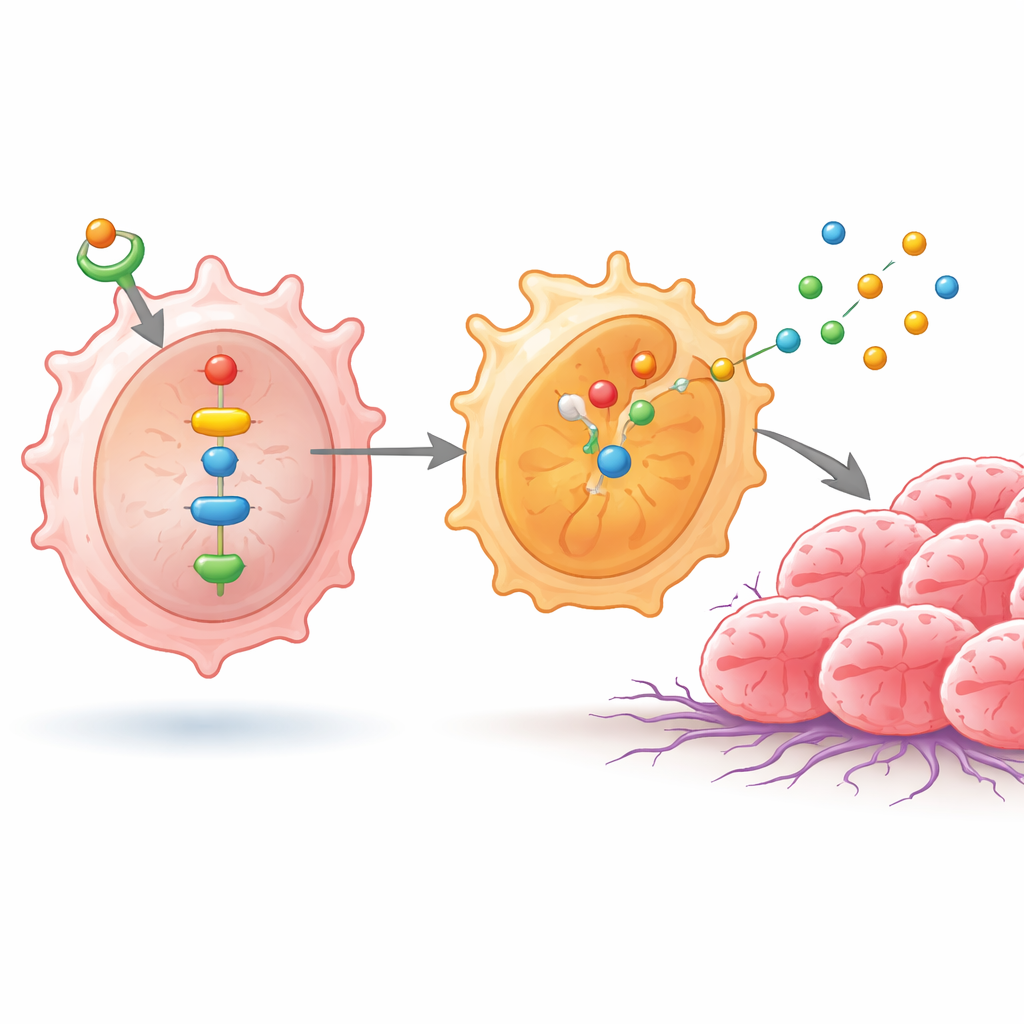
Comment des macrophages reprogrammés stimulent la croissance tumorale
Pour évaluer l’impact de ces changements immunitaires sur les cellules cancéreuses, l’équipe a cultivé des lignées de cancer du poumon en présence des macrophages traités de différentes manières. Lorsque ID1 était élevé et que la chaîne de signalisation était intacte, les cellules cancéreuses se multipliaient plus rapidement et migrèrent mieux à travers des barrières artificielles — des comportements liés à la dissémination dans l’organisme. Lorsque NF‑κB était bloqué, ces traits agressifs diminuaient, mais réapparaissaient si NPM1 était réactivé, soulignant l’importance de cette voie. Les chercheurs sont ensuite passés à des modèles murins, implantant sous la peau des mélanges de cellules cancéreuses pulmonaires et de macrophages traités. Les tumeurs formées en présence de macrophages riches en ID1 et de phénotype M2 ont grandi davantage et étaient plus volumineuses, tandis que les tumeurs associées à des macrophages avec la voie bloquée restaient plus petites. Des échantillons de tumeurs pulmonaires humaines ont également montré des niveaux plus élevés de ID1 et de NF‑κB activé par rapport aux tissus non cancéreux adjacents, reliant les découvertes de laboratoire aux patients réels.
Ce que cela signifie pour les futurs traitements du cancer du poumon
Dans l’ensemble, ce travail décrit ID1 comme un « interrupteur maître » important qui aide à transformer des cellules immunitaires utiles en partenaires silencieux du cancer du poumon. En déclenchant une cascade via NF‑κB, NPM1 et SHP1/SHP2, ID1 pousse les macrophages vers un état de type M2 qui calme les attaques immunitaires et libère des facteurs favorisant la croissance, accélérant ainsi la progression tumorale. Pour les patients, le message est porteur d’espoir : au lieu de cibler uniquement les cellules cancéreuses, des thérapies futures pourraient viser à couper cette chaîne de signalisation ou à reconvertir les macrophages vers un comportement anti‑tumoral. Bien que ces résultats doivent encore être testés et affinés en contexte clinique, ils mettent en lumière une stratégie prometteuse — modifier le comportement du microenvironnement tumoral pour ralentir, voire inverser, l’évolution du cancer du poumon.
Citation: Jiang, P., Chen, Z., Cui, L. et al. ID1 in TAMs promoted the progression of non-small-cell carcinoma via increasing NF-κB/NPM1/SHP1/SHP2 signaling induced M2 polarization. Sci Rep 16, 14222 (2026). https://doi.org/10.1038/s41598-026-44075-6
Mots-clés: cancer du poumon non à petites cellules, macrophages associés aux tumeurs, microenvironnement immunitaire, polarisation des macrophages, immunothérapie du cancer