Clear Sky Science · tr
TAM'lardaki ID1, NF-κB/NPM1/SHP1/SHP2 sinyallemesiyle indüklenen M2 polarizasyonunu artırarak küçük hücre dışı karsinom ilerlemesini destekledi
Vücudun savunucuları neden akciğer kanserinin yardımcılarına dönüşebiliyor
Akciğer kanseri, birçok tümörün vücudun kendi bağışıklık sisteminden saklanmayı ya da ondan yararlanmayı öğrenmesi nedeniyle hâlâ en ölümcül kanserlerden biridir. Bu çalışma, akciğer tümörleri içinde biriken özel bir bağışıklık hücresi grubunu inceliyor ve basit ama kritik bir soruyu soruyor: bu hücreleri kanserle savaşmaktan onu desteklemeye ne geçiriyor? Bu geçişi anlamak, tümöre doğrudan saldırmaktan ziyade bağışıklık sistemini yeniden eğiten yeni tedavilere kapı açabilir.
Taraf değiştiren bağışıklık hücreleri
Her tümörün içinde, tümör mikroçevresi adı verilen kanser dışı hücrelerden oluşan yoğun bir mahalle vardır. En önemli sakinlerinden biri makrofajlardır; bunlar normalde mikropları ve hasarlı dokuyu yutan bağışıklık hücreleridir. Akciğer tümörlerinde, tümör ilişkili makrofajlar olarak bilinen bu hücrelerin birçoğu iltihabı yatıştıran, doku onaran ve ne yazık ki kanseri besleyen “M2” adı verilen bir duruma geçer. En yaygın akciğer kanseri türü olan küçük hücre dışı akciğer kanseri hastalarında sıklıkla çok sayıda M2 tipi makrofaj bulunur; bunlar hızlı tümör büyümesi, yayılma ve kötü tedavi yanıtları ile ilişkilidir.
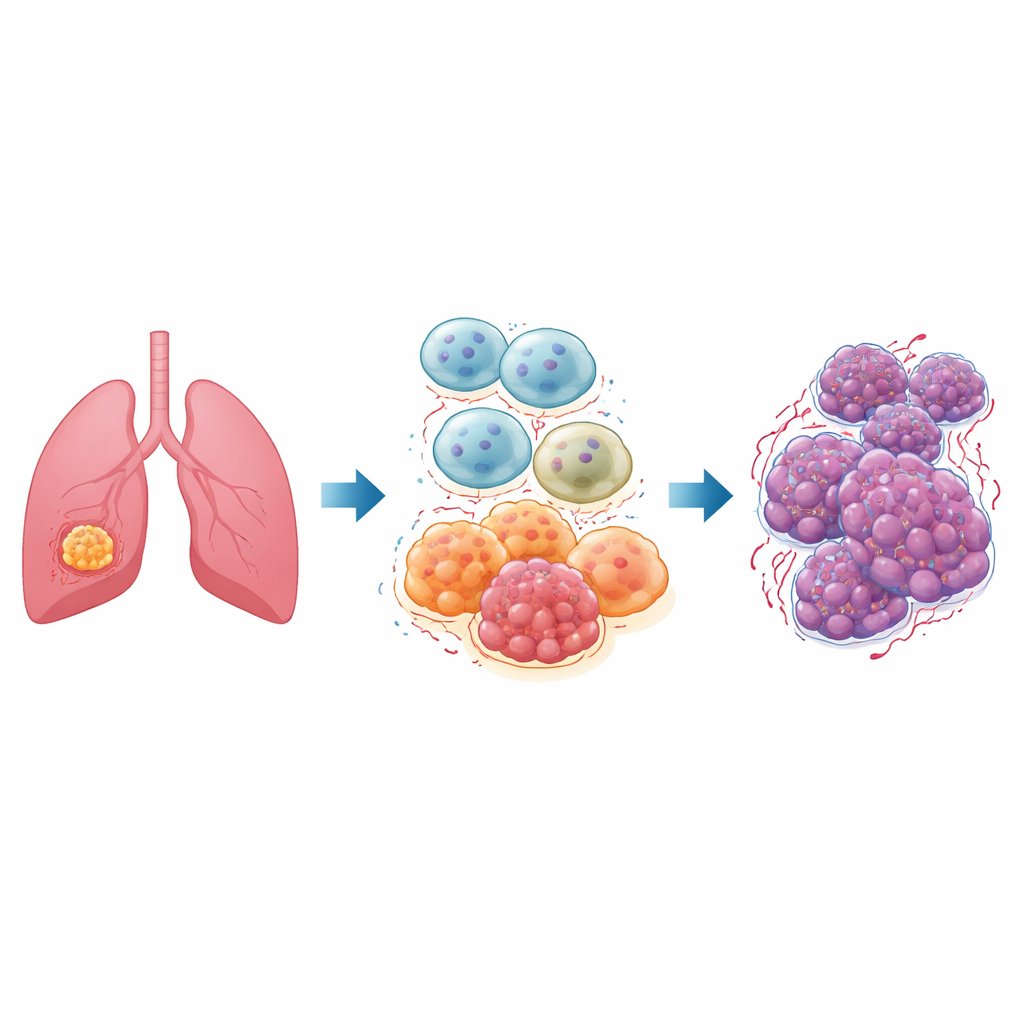
ID1 adlı bir anahtar anahtar
Araştırmacılar, çeşitli kanserleri daha agresif davranışa itmesiyle zaten bilinen ID1 adlı bir proteine odaklandı. ID1’in tümör ilişkili makrofajlarda bu hücreleri kanseri destekleyen M2 durumuna yönlendirmeye yardımcı olduğunu düşündüler. Önce kamuya açık gen veritabanlarını kullanarak ID1 düzeylerinin akciğer kanseri örneklerinde NF‑κB adı verilen önemli bir kontrol faktörü ile birlikte arttığını gösterdiler; bu da bu moleküllerin birlikte çalıştığına işaret etti. Ardından insan makrofajlarının laboratuvar modellerini kurdular ve genetik araçlar ile ilaçlar kullanarak ya ID1'i artırdılar ya da NF‑κB'yi engellediler ve aynı zincirdeki diğer moleküllerin nasıl değiştiğini dikkatle izlediler.
ID1 makrofajların devrelerini nasıl yeniden kuruyor
Bu makrofajlarda daha yüksek ID1 düzeyleri NF‑κB ve başka bir protein olan NPM1’i etkinleştirdi; bunlar birlikte SHP1 ve SHP2 adlı bir çift enzimi aktifleştirdi. Bu zincirleme reaksiyon, NF‑κB alt birimlerinin hücre çekirdeğine geçmesini sağladı ve orada M2 benzeri durumu destekleyen genleri açtı. Sonuç olarak makrofajlar IL‑4, IL‑10, arginaz‑1, CD206 ve birkaç katepsin gibi anti‑tümör bağışıklığını zayıflatan, dokuyu yeniden şekillendiren ve kanser hücrelerinin hareket ve invazyonunu kolaylaştıran maddeleri daha yüksek miktarlarda üretmeye başladı. Bilim insanları bu sinyallemeyi NF‑κB'yi bloke ederek veya NPM1'i dikkatlice ayarlayarak kesintiye uğrattığında, SHP1, SHP2 ve bu M2 ilişkili maddelerin düzeyleri düştü ve makrofajlar tümör dostu görünümünü kaybetti.
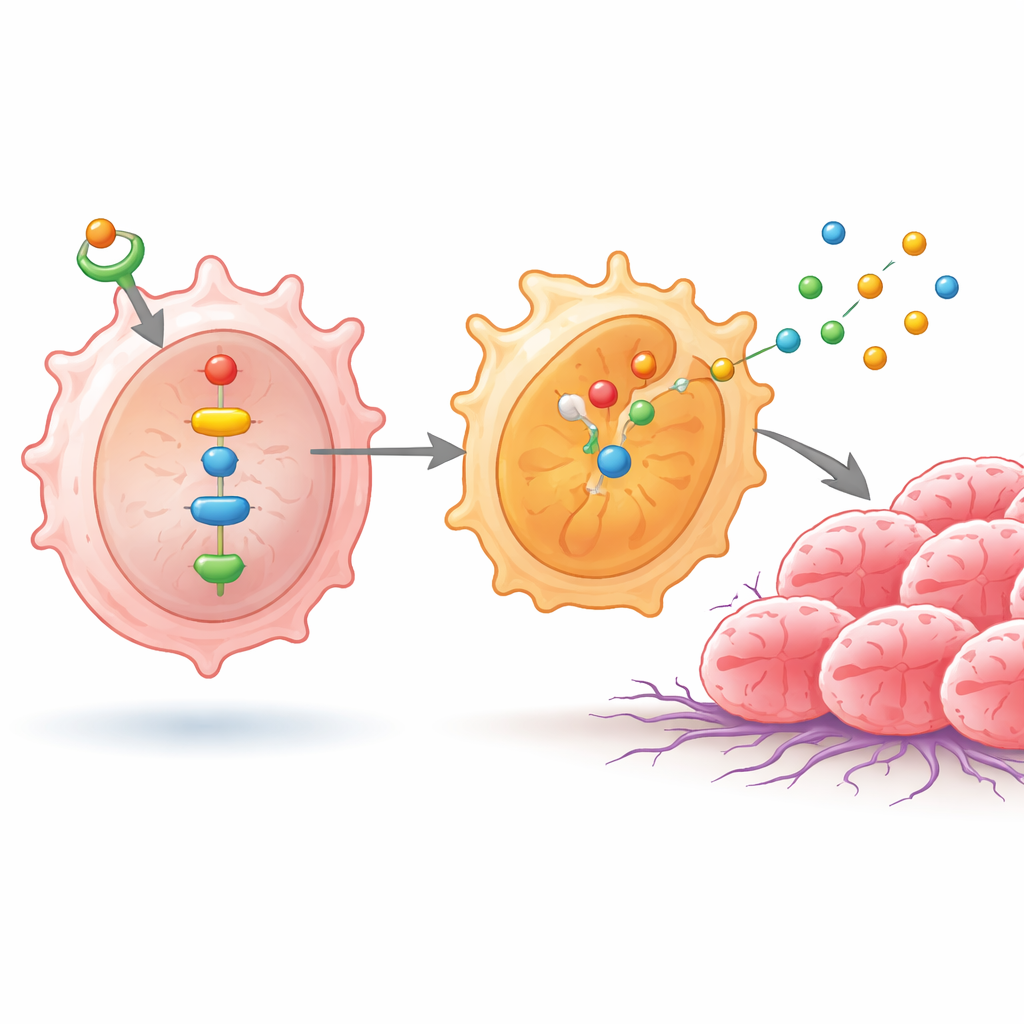
Yeniden programlanmış makrofajlar tümör büyümesini nasıl artırıyor
Bu bağışıklık değişikliklerinin kanser hücrelerini nasıl etkilediğini görmek için ekip, farklı şekilde muamele edilmiş makrofajlarla birlikte akciğer kanseri hücre hatlarını birlikte büyüttü. ID1 yüksek ve sinyal zinciri sağlam olduğunda, kanser hücreleri daha hızlı çoğaldı ve yapay bariyerlerden geçme konusunda daha yetenekli oldu—bu davranışlar vücutta yayılma ile ilişkilidir. NF‑κB bloke edildiğinde bu agresif özellikler azaldı; ancak NPM1 yeniden aktive edilirse özellikler geri geldi ve bu yolun önemini vurguladı. Araştırmacılar daha sonra farelerde, akciğer kanseri hücreleri ile muamele edilmiş makrofaj karışımlarını deri altına implante etti. ID1 açısından zengin, M2‑benzeri makrofajlarla birlikte oluşan tümörler daha büyük ve daha ağır olurken; yol bloke edilmiş makrofajlarla eşleştirilen tümörler daha küçük kaldı. İnsan akciğer tümörü örnekleri de çevrelerindeki kansersiz dokuya kıyasla daha yüksek ID1 ve aktive NF‑κB düzeyleri gösterdi; bu da laboratuvar bulgularını gerçek hastalarla ilişkilendirdi.
Gelecekteki akciğer kanseri tedavileri için anlamı
Bir araya getirildiğinde bu çalışma, ID1'i faydalı bağışıklık hücrelerini akciğer kanserinin sessiz ortağı haline getiren önemli bir “anahtar anahtar” olarak resmediyor. ID1, NF‑κB, NPM1 ve SHP1/SHP2 yoluyla bir dizi olayı tetikleyerek makrofajları bağışıklık saldırılarını yatıştıran ve büyümeyi destekleyen faktörler salan M2‑benzeri bir duruma yönlendiriyor; böylece tümör ilerlemesini hızlandırıyor. Hastalar için umut verici mesaj şudur: yalnızca kanser hücrelerini hedeflemek yerine, gelecekteki tedaviler bu sinyal zincirini kesmeyi veya makrofajları yeniden kanserle savaşan moda döndürmeyi amaçlayabilir. Bu bulgular klinik ortamlarda test edilip rafine edilmesi gereken aşamada olsa da, tümörün kendi mahallesinin davranışını değiştirme stratejisini öne çıkararak akciğer kanserinin seyrini yavaşlatma ya da tersine çevirme açısından umut vadediyor.
Atıf: Jiang, P., Chen, Z., Cui, L. et al. ID1 in TAMs promoted the progression of non-small-cell carcinoma via increasing NF-κB/NPM1/SHP1/SHP2 signaling induced M2 polarization. Sci Rep 16, 14222 (2026). https://doi.org/10.1038/s41598-026-44075-6
Anahtar kelimeler: küçük hücre dışı akciğer kanseri, tümör ilişkili makrofajlar, immün mikroçevre, makrofaj polarizasyonu, kanser immünoterapisi