Clear Sky Science · de
ID1 in TAMs förderte das Fortschreiten von non‑small‑cell-Karzinom durch Verstärkung von NF-κB/NPM1/SHP1/SHP2‑Signalwegen, die eine M2‑Polarisation induzieren
Warum die körpereigenen Verteidiger zu Helfern des Lungenkrebses werden können
Lungenkrebs bleibt eine der tödlichsten Krebsarten weltweit, zum Teil weil viele Tumoren lernen, sich vor dem Immunsystem zu verbergen oder es sogar auszunutzen. Diese Studie untersucht eine spezielle Gruppe von Immunzellen, die sich in Lungen-Tumoren ansammeln, und stellt eine einfache, aber entscheidende Frage: Was bringt diese Zellen dazu, vom Krebsbekämpfer zum Krebsunterstützer zu werden? Das Verständnis dieses Umschaltens könnte neue Behandlungsansätze eröffnen, die das Immunsystem umprogrammieren statt nur den Tumor direkt anzugreifen.
Immunzellen, die die Seiten wechseln
In jedem Tumor gibt es eine lebhafte Nachbarschaft nicht‑tumoraler Zellen, das so genannte Tumormikroumfeld. Zu seinen wichtigsten Bewohnern gehören Makrophagen, Immunzellen, die normalerweise dafür zuständig sind, Erreger und beschädigtes Gewebe zu beseitigen. In Lungen-Tumoren nehmen viele dieser Zellen, die als tumorassoziierte Makrophagen bezeichnet werden, einen sogenannten „M2“-Zustand ein, der Entzündungen dämpft, Gewebe repariert und leider auch den Krebs unterstützt. Patienten mit nicht‑kleinzelligem Lungenkrebs, der häufigsten Form von Lungenkrebs, weisen oft viele dieser M2‑Makrophagen auf, was mit schnellem Tumorwachstum, Metastasierung und schlechteren Therapieansprechen verbunden ist.
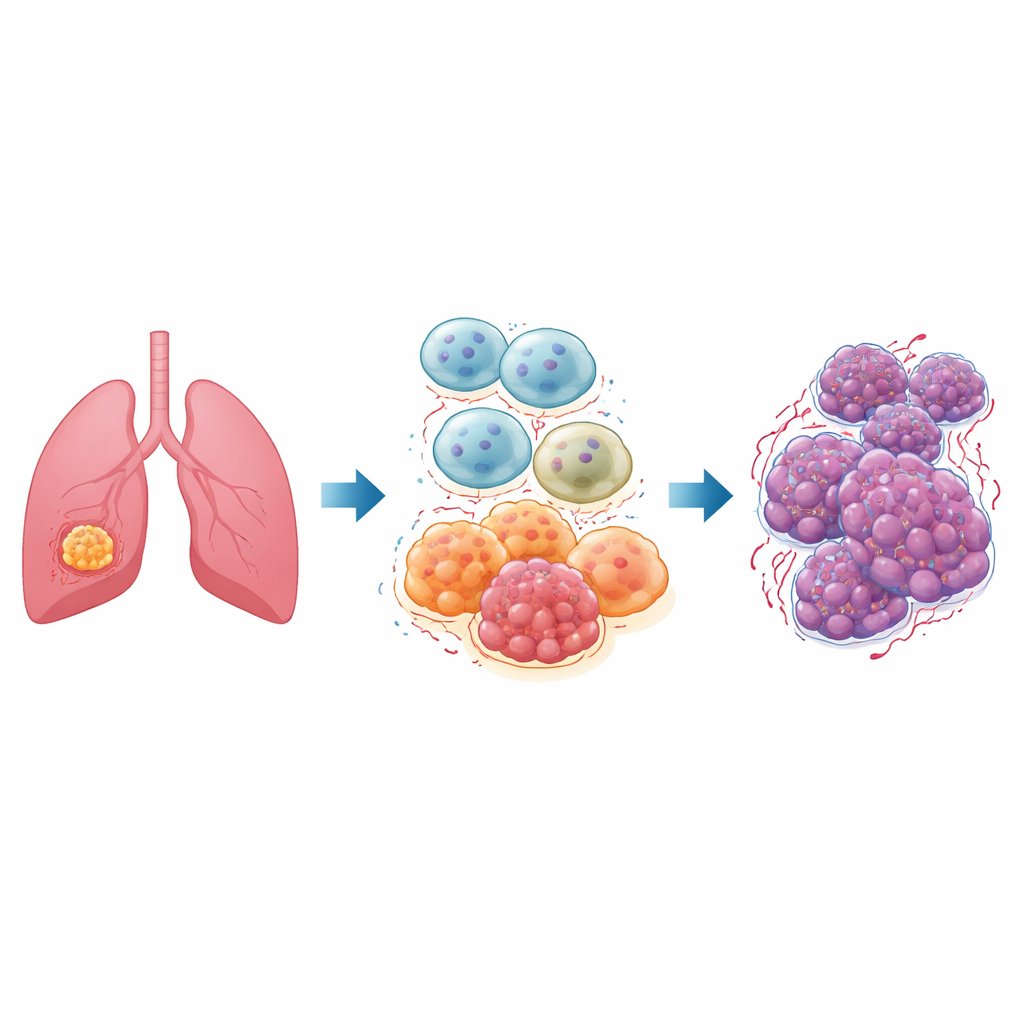
Ein Hauptschalter namens ID1
Die Forscher konzentrierten sich auf ein Protein namens ID1, das bereits dafür bekannt ist, verschiedene Krebsarten aggressiver zu machen. Sie vermuteten, dass ID1 in tumorassoziierten Makrophagen diese Zellen in den tumorfördernden M2‑Zustand lenkt. Mithilfe öffentlicher Gen-Datenbanken zeigten sie zunächst, dass ID1‑Spiegel in Lungenkrebsproben zusammen mit einem wichtigen Kontrollfaktor namens NF‑κB ansteigen, was darauf hindeutet, dass diese Moleküle zusammenarbeiten. Anschließend etablierten sie Labor‑Modelle menschlicher Makrophagen und nutzten genetische Werkzeuge sowie Wirkstoffe, um ID1 zu erhöhen oder NF‑κB zu blockieren, und verfolgten sorgfältig, wie sich dies auf weitere Moleküle der gleichen Signalkette auswirkte.
Wie ID1 Makrophagen umprogrammiert
In diesen Makrophagen aktivierte ein erhöhtes ID1‑Niveau NF‑κB und ein weiteres Protein, NPM1, die zusammen ein Paar Enzyme namens SHP1 und SHP2 in Gang setzten. Diese Kaskade förderte das Eindringen von NF‑κB‑Untereinheiten in den Zellkern, wo sie Gene anschalteten, die den M2‑ähnlichen Zustand begünstigen. Folglich begannen die Makrophagen, vermehrt Substanzen wie IL‑4, IL‑10, Arginase‑1, CD206 und mehrere Cathepsine zu produzieren — Moleküle, die bekannt dafür sind, die antitumorale Immunantwort zu dämpfen, Gewebe umzubauen und das Eindringen und die Wanderung von Krebszellen zu erleichtern. Wenn die Wissenschaftler diese Signalübertragung unterbrachen, entweder durch Blockade von NF‑κB oder durch gezielte Modulation von NPM1, sanken die Spiegel von SHP1, SHP2 und diesen M2‑assoziierten Substanzen, und die Makrophagen zeigten ein weniger tumorförderliches Profil.
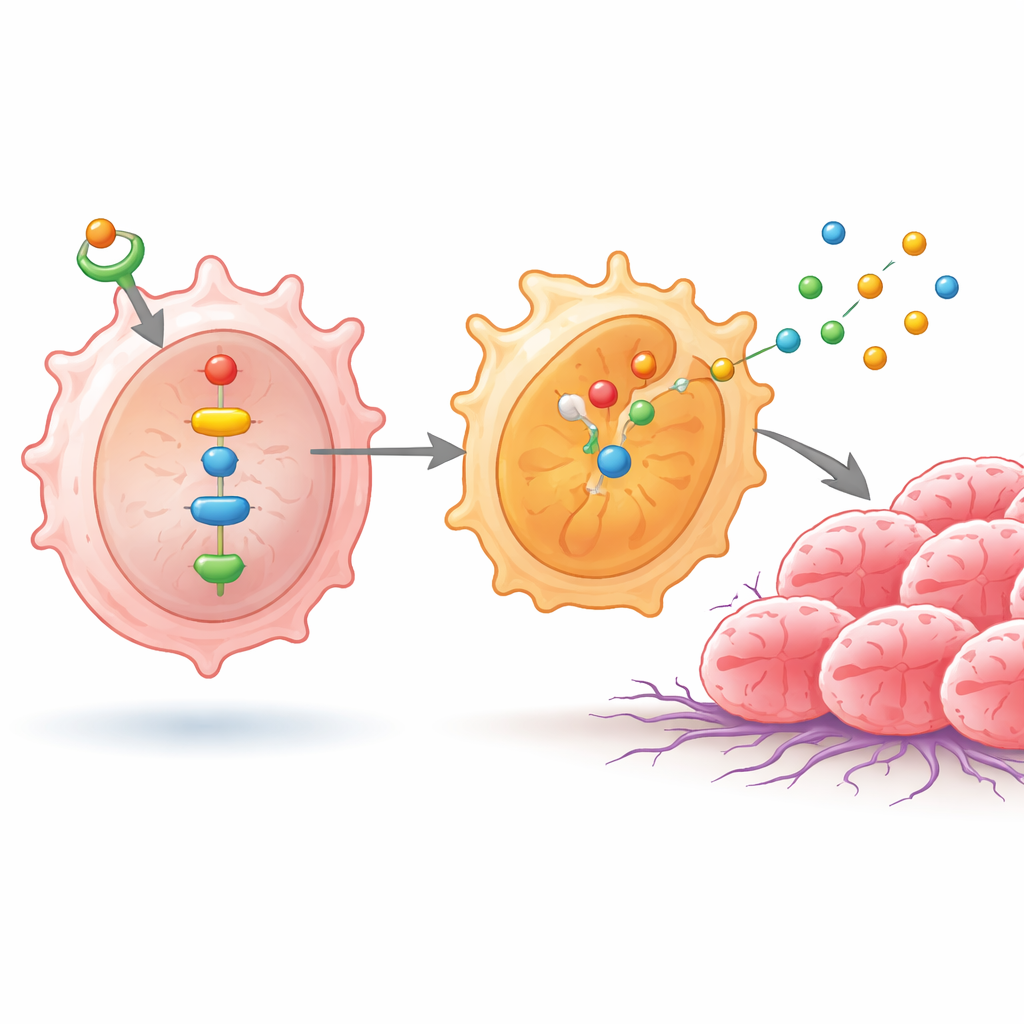
Wie umprogrammierte Makrophagen das Tumorwachstum fördern
Um zu prüfen, wie sich diese Immunveränderungen auf Krebszellen auswirken, züchtete das Team Lungenkrebszelllinien zusammen mit den unterschiedlich behandelten Makrophagen. Bei hohem ID1‑Spiegel und intakter Signalkette teilten sich die Krebszellen schneller und waren besser in der Lage, künstliche Barrieren zu durchwandern — Verhaltensweisen, die mit Metastasierung in Verbindung stehen. Wurde NF‑κB blockiert, gingen diese aggressiven Eigenschaften zurück, kehrten jedoch zurück, wenn NPM1 wieder aktiviert wurde, was die Bedeutung dieses Weges unterstreicht. Die Forscher trugen die Experimente in Mäuse weiter, indem sie Mischungen aus Lungenkrebszellen und behandelten Makrophagen unter die Haut implantierten. Tumoren, die neben ID1‑reichen, M2‑ähnlichen Makrophagen entstanden, wuchsen größer und schwerer, während Tumoren mit blockierten Signalwegen kleiner blieben. Auch menschliche Lungentumorproben zeigten höhere ID1‑ und aktiviertes NF‑κB‑Niveau im Vergleich zu benachbartem, nicht‑tumoralem Gewebe, wodurch die Laborbefunde mit Patientendaten in Verbindung gesetzt wurden.
Was das für zukünftige Lungenkrebs‑Behandlungen bedeutet
Insgesamt zeichnet die Arbeit ID1 als wichtigen „Hauptschalter“, der dabei hilft, nützliche Immunzellen in stille Partner des Lungenkrebses zu verwandeln. Indem ID1 eine Kaskade über NF‑κB, NPM1 und SHP1/SHP2 antreibt, schiebt es Makrophagen in einen M2‑ähnlichen Zustand, der Immunangriffe beruhigt und wachstumsfördernde Faktoren freisetzt und so das Tumorwachstum beschleunigt. Für Patientinnen und Patienten ist die Botschaft hoffnungsvoll: Statt nur die Krebszellen ins Visier zu nehmen, könnten künftige Therapien darauf abzielen, diese Signalkette zu unterbrechen oder Makrophagen wieder in einen krebsbekämpfenden Zustand zurückzuschalten. Während diese Ergebnisse noch in klinischen Studien geprüft und verfeinert werden müssen, heben sie eine vielversprechende Strategie hervor — das Verhalten der Tumornachbarschaft zu verändern, um das Fortschreiten des Lungenkrebses zu verlangsamen oder möglicherweise umzukehren.
Zitation: Jiang, P., Chen, Z., Cui, L. et al. ID1 in TAMs promoted the progression of non-small-cell carcinoma via increasing NF-κB/NPM1/SHP1/SHP2 signaling induced M2 polarization. Sci Rep 16, 14222 (2026). https://doi.org/10.1038/s41598-026-44075-6
Schlüsselwörter: nicht‑kleinzelliges Lungenkarzinom, tumorassoziierte Makrophagen, immunes Mikroumfeld, Makrophagenpolarisation, Krebsimmuntherapie