Clear Sky Science · nl
ID1 in TAM's bevorderde de progressie van niet-kleincellige longkanker door verhoging van NF-κB/NPM1/SHP1/SHP2-signaal dat M2-polarisatie induceert
Waarom de verdedigers van het lichaam helpers van longkanker kunnen worden
Longkanker blijft een van de dodelijkste vormen van kanker wereldwijd, deels omdat veel tumoren leren zich te verbergen voor en zelfs gebruik te maken van het eigen immuunsysteem. Deze studie onderzoekt een specifieke groep immuuncellen die zich in longtumoren ophopen en stelt een eenvoudige maar cruciale vraag: wat zorgt ervoor dat deze cellen overschakelen van het bestrijden van kanker naar het ondersteunen ervan? Begrijpen hoe die omschakeling plaatsvindt, kan de deur openen naar nieuwe behandelingen die het immuunsysteem hertrainen in plaats van alleen de tumor direct aan te vallen.
Immune cellen die van kant veranderen
In elke tumor bevindt zich een drukke buurt van niet-kankerachtige cellen, het tumor-micro-omgeving genoemd. Tot de belangrijkste bewoners behoren macrofagen, immuuncellen die normaal gesproken bacteriën en beschadigd weefsel opruimen. In longtumoren nemen veel van deze cellen, bekend als tumor-geassocieerde macrofagen, een zogenoemde “M2”-toestand aan die ontsteking kalmeert, weefsel repareert en, helaas, kanker ondersteunt. Patiënten met niet-kleincellige longkanker, de meest voorkomende vorm van longkanker, hebben vaak veel van deze M2-type macrofagen, die gekoppeld zijn aan snelle tumorgroei, uitzaaiing en slechte therapierespons.
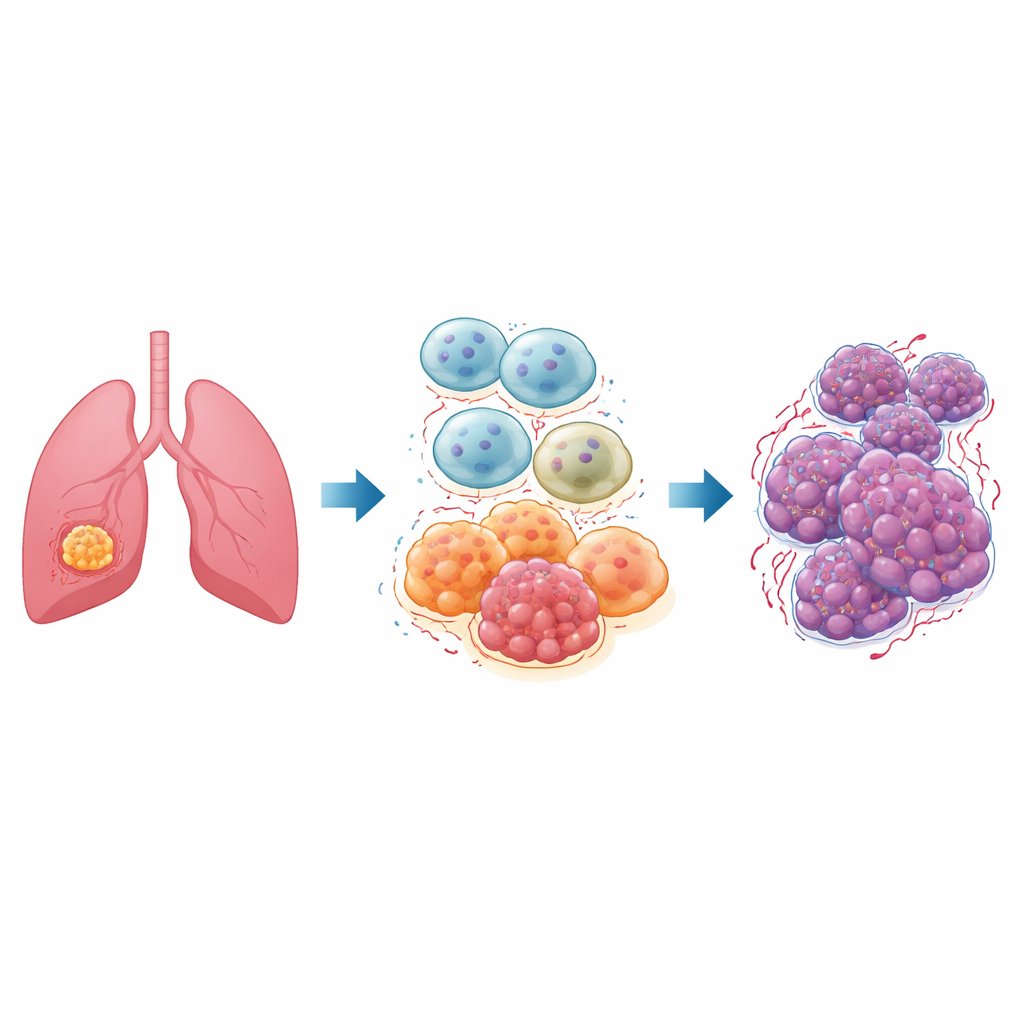
Een hoofdschakelaar genaamd ID1
De onderzoekers richtten zich op een eiwit met de naam ID1, dat al bekendstaat als bevorderaar van agressiever gedrag in verschillende kankers. Ze vermoedden dat ID1 in tumor-geassocieerde macrofagen helpt deze cellen naar hun kankervriendelijke M2-toestand te sturen. Met behulp van publieke genbanken toonden ze eerst aan dat ID1-niveaus samen stijgen met een belangrijke regelaar genaamd NF-κB in longkankermonsters, wat erop wijst dat deze moleculen als partners functioneren. Vervolgens bouwden ze laboratoriummodellen van humane macrofagen en gebruikten genetische middelen en geneesmiddelen om ID1 te verhogen of NF-κB te blokkeren, terwijl ze zorgvuldig volgden hoe dit andere moleculen in dezelfde keten veranderde.
Hoe ID1 macrofagen herbedraadt
In deze macrofagen zorgde een hogere ID1-expressie voor activatie van NF-κB en een ander eiwit, NPM1, die samen een paar enzymen activeerden genaamd SHP1 en SHP2. Deze kettingreactie duwde NF-κB-subunits de celkern in, waar ze genen aanzetten die de M2-achtige toestand bevorderen. Als gevolg begonnen de macrofagen grotere hoeveelheden stoffen te produceren zoals IL-4, IL-10, arginase-1, CD206 en verschillende cathepsines — moleculen die bekendstaan om het onderdrukken van anti-tumorimmuniteit, het herbouwen van weefsel en het vergemakkelijken van migratie en invasie van kankercellen. Wanneer de onderzoekers deze signaaloverdracht onderbraken, hetzij door NF-κB te blokkeren of door NPM1 zorgvuldig aan te passen, daalden de niveaus van SHP1, SHP2 en deze M2-geassocieerde stoffen, en gedroegen de macrofagen zich minder tumorvriendelijk.
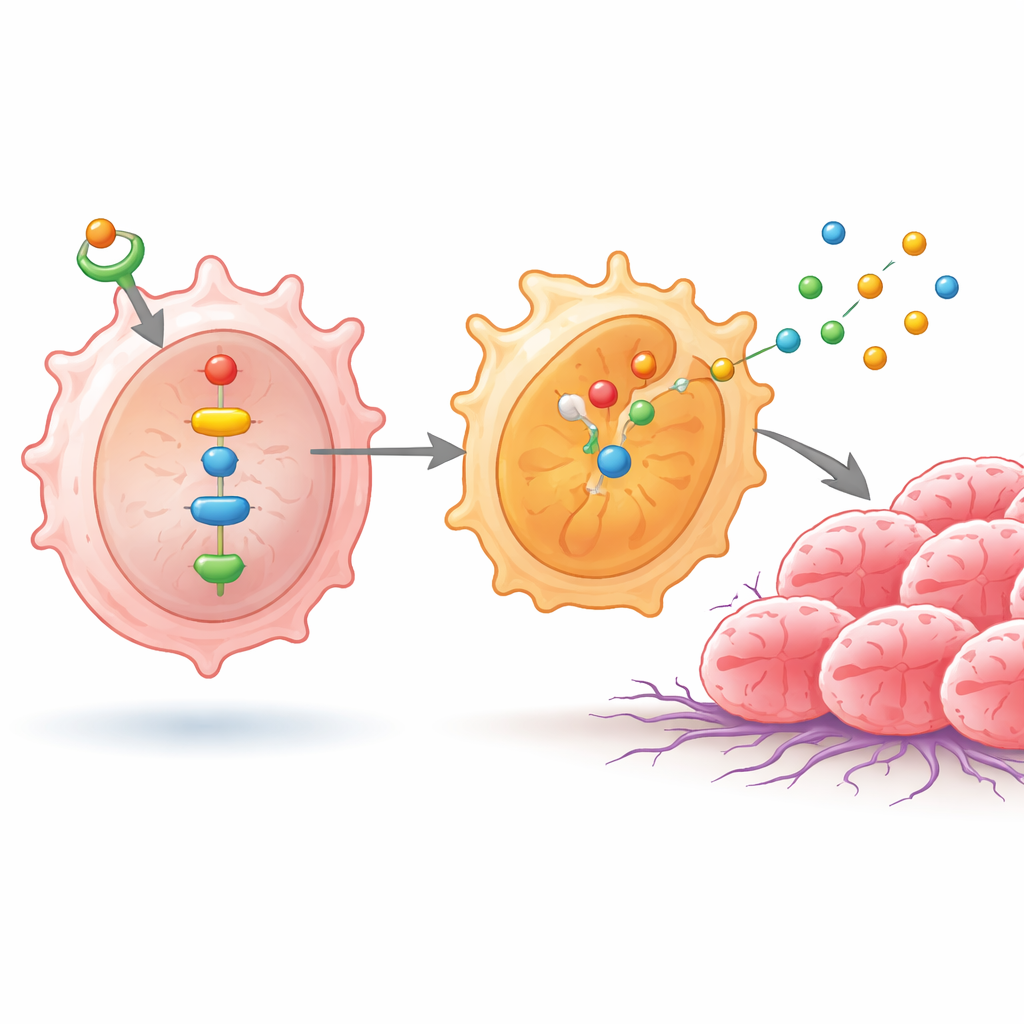
Hoe geherprogrammeerde macrofagen tumorgroei stimuleren
Om te zien hoe deze immuunveranderingen kankercellen beïnvloeden, kweekte het team longkankercellijnen samen met de verschillend behandelde macrofagen. Wanneer ID1 hoog was en de signaalketen intact bleef, vermenigvuldigden de kankercellen zich sneller en waren ze beter in staat door kunstmatige barrières te migreren — gedragingen die samenhangen met uitzaaiing in het lichaam. Wanneer NF-κB werd geblokkeerd, verdwenen deze agressieve eigenschappen, maar ze keerden terug als NPM1 weer gedwongen werd te activeren, wat het belang van deze route onderstreept. De onderzoekers gingen vervolgens naar muismodellen en implanteren mengsels van longkankercellen en behandelde macrofagen onder de huid. Tumoren die samen met ID1-rijke, M2-achtige macrofagen vormden, werden groter en zwaarder, terwijl tumoren die met pathway-geblokkeerde macrofagen werden gevormd kleiner bleven. Humane longtumormonsters toonden ook hogere niveaus van ID1 en geactiveerd NF-κB in vergelijking met nabijgelegen niet-kankerachtig weefsel, waarmee de laboratoriumbevindingen aan echte patiënten werden gekoppeld.
Wat dit betekent voor toekomstige behandelingen van longkanker
Gezamenlijk schetst het werk ID1 als een belangrijke “hoofdschakelaar” die helpt om behulpzame immuuncellen te veranderen in stille partners van longkanker. Door een keten van gebeurtenissen te sturen via NF-κB, NPM1 en SHP1/SHP2, duwt ID1 macrofagen in een M2-achtige toestand die immuunaanvallen dempt en groeibevorderende factoren vrijgeeft, waardoor de tumorprogressie versnelt. Voor patiënten is de boodschap hoopgevend: in plaats van alleen de kankercellen te richten, zouden toekomstige therapieën kunnen proberen deze signaalketen te onderbreken of macrofagen weer te draaien naar een kankervijandig profiel. Hoewel deze bevindingen nog in klinische settings getest en verfijnd moeten worden, benadrukken ze een veelbelovende strategie — het veranderen van het gedrag van de tumoromgeving om de voortgang van longkanker te vertragen of zelfs om te keren.
Bronvermelding: Jiang, P., Chen, Z., Cui, L. et al. ID1 in TAMs promoted the progression of non-small-cell carcinoma via increasing NF-κB/NPM1/SHP1/SHP2 signaling induced M2 polarization. Sci Rep 16, 14222 (2026). https://doi.org/10.1038/s41598-026-44075-6
Trefwoorden: niet-kleincellige longkanker, tumor-geassocieerde macrofagen, immuunmicro-omgeving, macrofagenpolarizatie, kankerimmunotherapie