Clear Sky Science · es
ID1 en los TAM promovió la progresión del carcinoma de células no pequeñas mediante el aumento de la señalización NF-κB/NPM1/SHP1/SHP2 inducida por la polarización M2
Por qué los defensores del cuerpo pueden convertirse en cómplices del cáncer de pulmón
El cáncer de pulmón sigue siendo uno de los tumores más letales a nivel mundial, en parte porque muchos cánceres aprenden a ocultarse e incluso a explotar el propio sistema inmunitario del organismo. Este estudio examina un grupo especial de células inmunitarias que se agrupan dentro de los tumores pulmonares y plantea una pregunta sencilla pero crucial: ¿qué hace que estas células cambien de combatir el cáncer a favorecer su crecimiento? Comprender ese cambio podría abrir la puerta a nuevos tratamientos que reprogramen el sistema inmunitario en lugar de atacar el tumor únicamente de forma directa.
Células inmunitarias que cambian de bando
En el interior de cada tumor hay un vecindario bullicioso de células no cancerosas llamado microambiente tumoral. Entre sus residentes más importantes están los macrófagos, células inmunitarias cuya función habitual es engullir gérmenes y tejido dañado. En los tumores pulmonares, muchas de estas células, conocidas como macrófagos asociados al tumor, adoptan un estado denominado “M2” que reduce la inflamación, repara tejidos y, desafortunadamente, nutre el cáncer. Los pacientes con cáncer de pulmón no microcítico, la forma más común de este cáncer, suelen presentar numerosos macrófagos de tipo M2, vinculados a un crecimiento tumoral rápido, diseminación y malas respuestas al tratamiento.
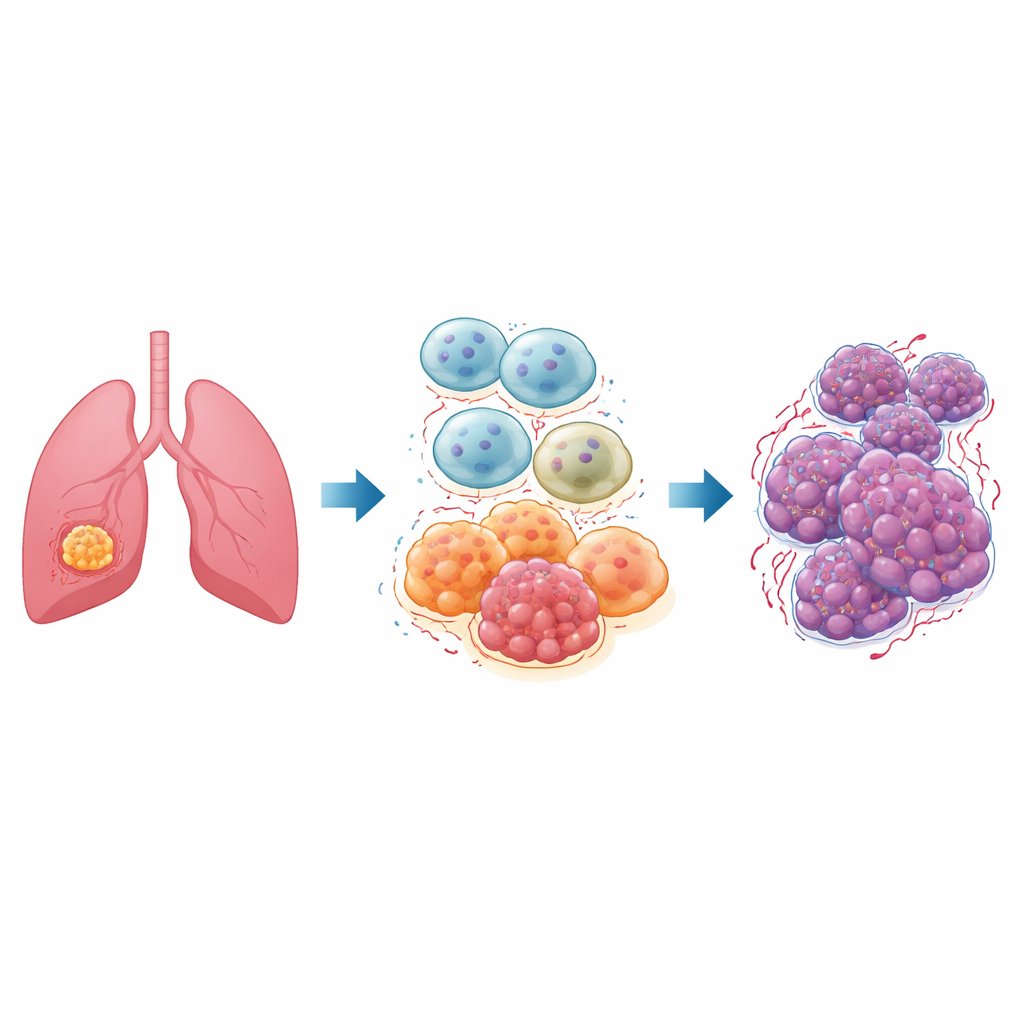
Un interruptor maestro llamado ID1
Los investigadores se centraron en una proteína llamada ID1, ya conocida por impulsar un comportamiento más agresivo en varios tipos de cáncer. Sospechaban que ID1 en los macrófagos asociados al tumor ayuda a orientar estas células hacia su estado M2, favorable al cáncer. Empleando bases de datos genómicas públicas, mostraron inicialmente que los niveles de ID1 aumentan junto con un factor clave de control llamado NF-κB en muestras de cáncer de pulmón, lo que sugiere que estas moléculas actúan en conjunto. A continuación, construyeron modelos de laboratorio con macrófagos humanos y utilizaron herramientas genéticas y fármacos para aumentar ID1 o bloquear NF-κB, monitorizando con detalle cómo esto alteraba otras moléculas de la misma vía.
Cómo ID1 reconecta los macrófagos
En estos macrófagos, niveles elevados de ID1 activaron NF-κB y otra proteína, NPM1, que a su vez activaron un par de enzimas denominadas SHP1 y SHP2. Esta reacción en cadena empujó subunidades de NF-κB al núcleo celular, donde encendieron genes que favorecen el estado similar a M2. Como resultado, los macrófagos comenzaron a producir mayores cantidades de sustancias como IL-4, IL-10, arginasa-1, CD206 y varias catepsinas: moléculas conocidas por atenuar la inmunidad antitumoral, remodelar el tejido y facilitar el movimiento e invasión de las células cancerosas. Cuando los científicos interrumpieron esta señalización, ya fuera bloqueando NF-κB o modulando cuidadosamente NPM1, bajaron los niveles de SHP1, SHP2 y de estos marcadores asociados a M2, y los macrófagos presentaron un perfil menos favorable al tumor.
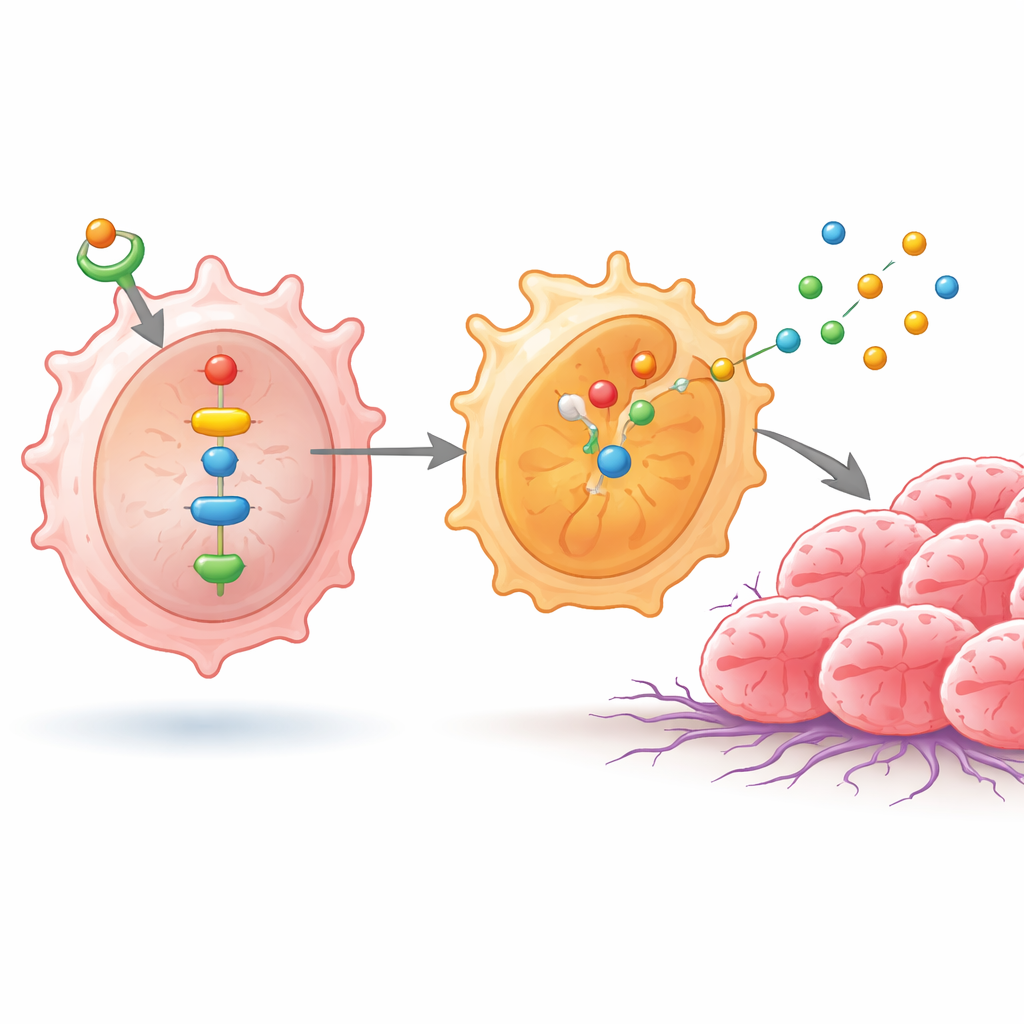
Cómo los macrófagos reprogramados potencian el crecimiento tumoral
Para ver cómo estos cambios inmunitarios afectan a las células cancerosas, el equipo cultivó líneas celulares de cáncer de pulmón junto con macrófagos tratados de forma distinta. Cuando ID1 era alto y la vía de señalización estaba intacta, las células cancerosas se multiplicaban más rápido y migraban mejor a través de barreras artificiales—comportamientos asociados a la diseminación en el organismo. Al bloquear NF-κB, estos rasgos agresivos disminuyeron, pero volvieron si se reactivaba NPM1, subrayando la importancia de esta vía. Los investigadores pasaron después a modelos murinos, implantando bajo la piel mezclas de células de cáncer de pulmón y macrófagos tratados. Los tumores formados junto a macrófagos ricos en ID1 y con perfil M2 crecieron más y pesaron más, mientras que los tumores asociados a macrófagos con la vía bloqueada permanecieron más pequeños. Muestras humanas de tumores pulmonares también mostraron niveles más altos de ID1 y NF-κB activado en comparación con tejido no canceroso circundante, vinculando los hallazgos de laboratorio con pacientes reales.
Qué significa esto para futuros tratamientos del cáncer de pulmón
En conjunto, el trabajo presenta a ID1 como un “interruptor maestro” importante que contribuye a convertir células inmunitarias útiles en cómplices silenciosos del cáncer de pulmón. Al impulsar una cadena de eventos a través de NF-κB, NPM1 y SHP1/SHP2, ID1 empuja a los macrófagos hacia un estado similar a M2 que calma los ataques inmunitarios y libera factores que promueven el crecimiento, acelerando así la progresión tumoral. Para los pacientes, el mensaje es esperanzador: en lugar de dirigir las terapias únicamente contra las células cancerosas, los tratamientos futuros podrían intentar interrumpir esta cadena de señalización o reincorporar a los macrófagos a un modo de lucha contra el cáncer. Aunque estos hallazgos aún deben probarse y refinase en entornos clínicos, destacan una estrategia prometedora: cambiar el comportamiento del propio vecindario tumoral para frenar, o incluso revertir, la evolución del cáncer de pulmón.
Cita: Jiang, P., Chen, Z., Cui, L. et al. ID1 in TAMs promoted the progression of non-small-cell carcinoma via increasing NF-κB/NPM1/SHP1/SHP2 signaling induced M2 polarization. Sci Rep 16, 14222 (2026). https://doi.org/10.1038/s41598-026-44075-6
Palabras clave: cáncer de pulmón no microcítico, macrófagos asociados al tumor, microambiente inmunitario, polarización de macrófagos, inmunoterapia contra el cáncer