Clear Sky Science · pl
ID1 w makrofagach związanych z nowotworem sprzyja progresji gruczolakoraka niedrobnokomórkowego poprzez zwiększenie sygnalizacji NF-κB/NPM1/SHP1/SHP2 wywołującej polaryzację do typu M2
Dlaczego obrońcy organizmu mogą stać się sprzymierzeńcami raka płuca
Rak płuca pozostaje jednym z najgroźniejszych nowotworów na świecie, częściowo dlatego, że wiele guzów uczy się ukrywać przed układem odpornościowym, a nawet wykorzystywać go na swoją korzyść. W tym badaniu przyglądamy się szczególnej grupie komórek odpornościowych gromadzących się w guzach płuca i stawiamy proste, ale kluczowe pytanie: co sprawia, że te komórki przełączają się z walki z nowotworem na wspieranie jego wzrostu? Zrozumienie tego przełączenia może otworzyć drogę do nowych terapii, które będą na nowo kształtować układ odpornościowy, zamiast jedynie bezpośrednio atakować guz.
Komórki odpornościowe, które zmieniają strony
W każdym guzie istnieje tętniąca życiem dzielnica komórek niebędących nowotworowymi, zwana mikrośrodowiskiem guza. Jednymi z najważniejszych mieszkańców są makrofagi — komórki odpornościowe zwykle odpowiedzialne za pochłanianie zarazków i uszkodzonej tkanki. W guzach płuca wiele z tych komórek, określanych jako makrofagi związane z guzem, przyjmuje tzw. stan „M2”, który tłumi stan zapalny, naprawia tkanki i niestety sprzyja nowotworowi. Pacjenci z niedrobnokomórkowym rakiem płuca, najczęstszą postacią raka płuca, często mają wiele makrofagów typu M2, co wiąże się z szybkim wzrostem guza, jego rozsiewem i słabymi odpowiedziami na leczenie.
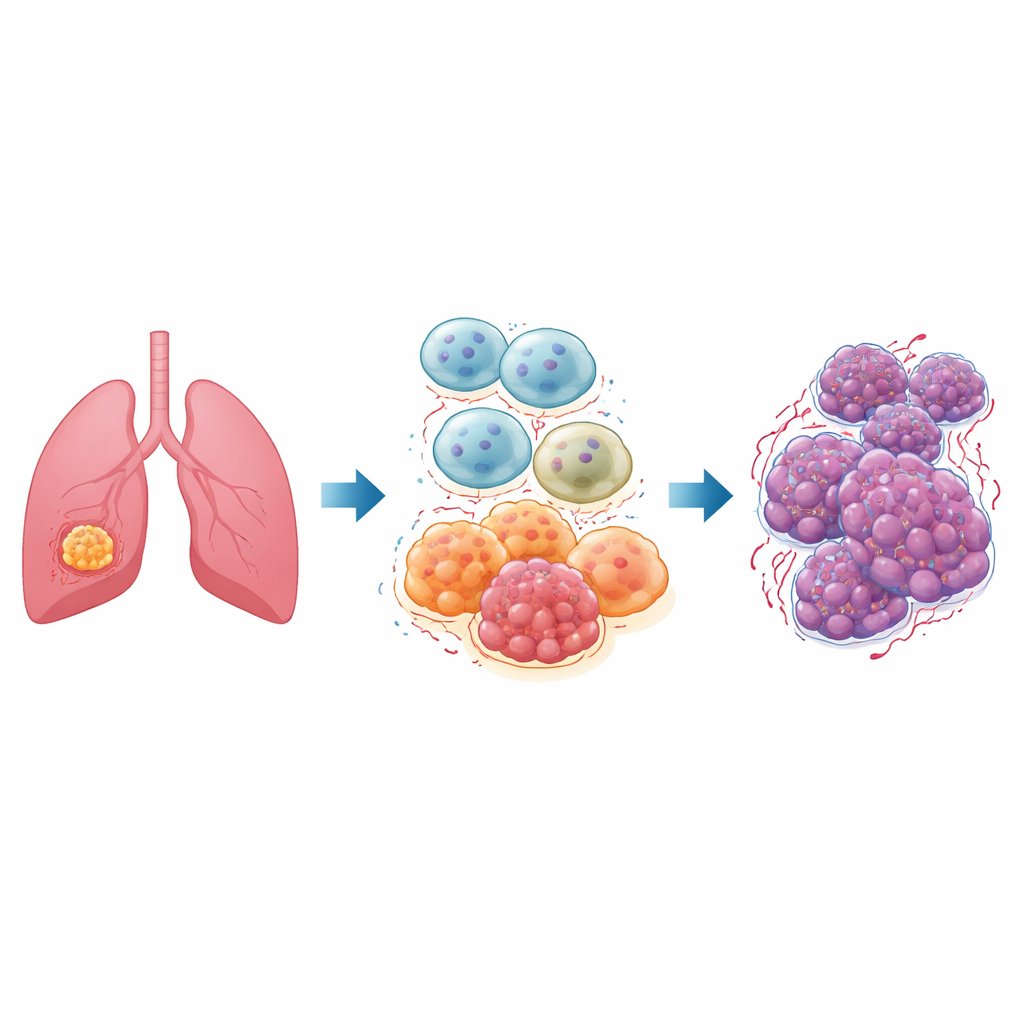
Przełącznik główny o nazwie ID1
Naukowcy skupili się na białku o nazwie ID1, już wcześniej znanym z tego, że wspiera bardziej agresywne zachowanie różnych nowotworów. Podejrzewali, że ID1 w makrofagach związanych z guzem pomaga skierować te komórki w stronę stanu M2 sprzyjającego nowotworowi. Korzystając z publicznych baz danych genowych, pokazali najpierw, że poziomy ID1 rosną równolegle z kluczowym czynnikiem kontroli, NF‑κB, w próbkach raka płuca, co sugeruje, że te molekuły działają wspólnie. Następnie stworzyli laboratoryjne modele ludzkich makrofagów i użyli narzędzi genetycznych oraz leków, aby albo zwiększyć ID1, albo zablokować NF‑κB, uważnie śledząc, jak to wpływa na inne molekuły w tym samym łańcuchu.
Jak ID1 przebudowuje makrofagi
W tych makrofagach wyższe poziomy ID1 uruchomiły NF‑κB oraz inne białko, NPM1, które razem aktywowały parę enzymów zwanych SHP1 i SHP2. Ta kaskada spowodowała przemieszczanie się podjednostek NF‑κB do jądra komórkowego, gdzie włączają one geny sprzyjające fenotypowi podobnemu do M2. W efekcie makrofagi zaczęły wytwarzać większe ilości substancji takich jak IL‑4, IL‑10, arginaza‑1, CD206 i kilka katepsyn — cząsteczek znanych z osłabiania odpowiedzi przeciwnowotworowej, przebudowy tkanki i ułatwiania migracji oraz inwazji komórek nowotworowych. Gdy naukowcy przerwali to sygnalizowanie, blokując NF‑κB lub precyzyjnie regulując NPM1, poziomy SHP1, SHP2 i tych substancji powiązanych z M2 spadły, a makrofagi wyglądały na mniej przyjazne guzowi.
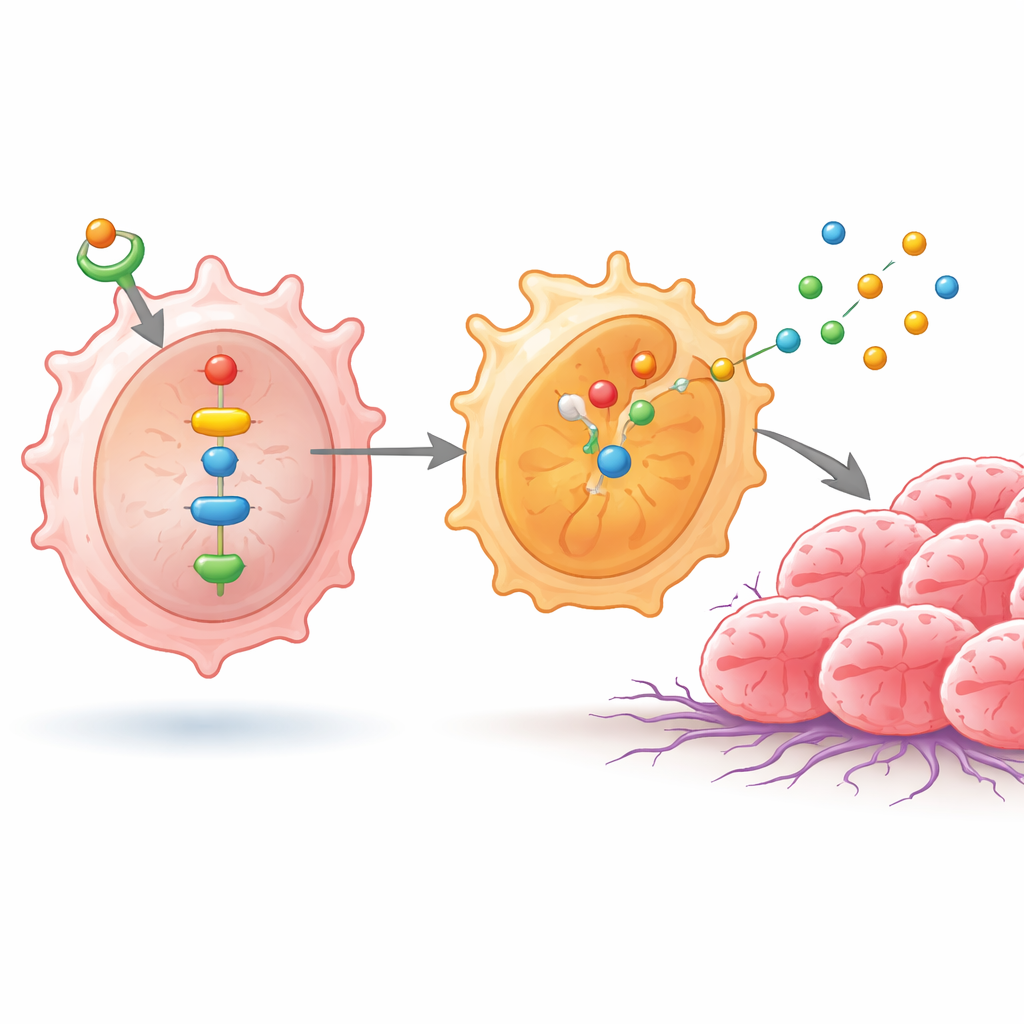
Jak przeprogramowane makrofagi przyspieszają wzrost guza
Aby sprawdzić, jak te zmiany immunologiczne wpływają na komórki nowotworowe, badacze hodowali linie komórek raka płuca razem z makrofagami poddanymi różnym manipulacjom. Gdy ID1 był wysoki, a łańcuch sygnalizacyjny nienaruszony, komórki nowotworowe rozmnażały się szybciej i lepiej migrowały przez sztuczne bariery — zachowania powiązane z rozsiewem w organizmie. Gdy NF‑κB został zablokowany, te agresywne cechy ustępowały, ale pojawiały się ponownie, jeśli NPM1 został na nowo aktywowany, co podkreśla znaczenie tej ścieżki. Następnie badacze przeszli do modelu mysiego, wszczepiając pod skórę mieszaniny komórek raka płuca i zmodyfikowanych makrofagów. Guzy rozwijające się w towarzystwie makrofagów bogatych w ID1 i o fenotypie M2 były większe i cięższe, podczas gdy guzy współtowarzyszące makrofagom zablokowanym w tej ścieżce pozostawały mniejsze. Próbki ludzkich guzów płuca również wykazały wyższe poziomy ID1 i aktywowanego NF‑κB w porównaniu z sąsiednią tkanką nie-nowotworową, co łączy wyniki laboratoryjne z przypadkami klinicznymi.
Co to oznacza dla przyszłych terapii raka płuca
W sumie praca ta przedstawia ID1 jako istotny „główny przełącznik”, który pomaga przekształcić pomocne komórki odpornościowe w cichych współpracowników raka płuca. Poprzez uruchamianie kaskady wydarzeń obejmującej NF‑κB, NPM1 i SHP1/SHP2, ID1 skłania makrofagi do fenotypu podobnego do M2, który tłumi ataki immunologiczne i uwalnia czynniki sprzyjające wzrostowi, przyspieszając w ten sposób progresję guza. Dla pacjentów przesłanie jest optymistyczne: zamiast atakować wyłącznie komórki nowotworowe, przyszłe terapie mogłyby celować w przerwanie tego łańcucha sygnałowego lub odwrócić polaryzację makrofagów z powrotem na antynowotworowy tryb. Chociaż odkrycia te wymagają jeszcze badań i walidacji w warunkach klinicznych, wskazują obiecującą strategię — zmianę zachowania mikrośrodowiska guza, by spowolnić lub nawet odwrócić przebieg raka płuca.
Cytowanie: Jiang, P., Chen, Z., Cui, L. et al. ID1 in TAMs promoted the progression of non-small-cell carcinoma via increasing NF-κB/NPM1/SHP1/SHP2 signaling induced M2 polarization. Sci Rep 16, 14222 (2026). https://doi.org/10.1038/s41598-026-44075-6
Słowa kluczowe: niedrobnokomórkowy rak płuca, makrofagi związane z guzem, mikrośrodowisko immunologiczne, polaryzacja makrofagów, immunoterapia nowotworów