Clear Sky Science · zh
开发和验证 gra1–bag1 RT-qPCR 检测作为替代小鼠生物测定以评估弓形虫(Toxoplasma gondii)活性
为什么这种微小寄生虫关系到你的餐桌
弓形虫(Toxoplasma gondii)是一种微小的寄生虫,在全球的农场动物、宠物和人类之间悄然循环。大多数感染不会有明显症状,但对孕妇和免疫力低下的人群,它可能导致流产、新生儿脑损伤和严重的眼部疾病。由于人类通常通过食用未熟或半熟的肉类而感染,食品安全研究人员需要可靠的方法来判断肉中寄生虫是否仍然存活且具有危险性。迄今为止,金标准检测需要感染活体小鼠并等待数周以观察疾病迹象——这种方法既慢又昂贵,而且与现代动物福利标准日益冲突。本研究提出了一种新的实验室检测方法,旨在在不大量依赖动物实验的情况下预测寄生虫的活性。
从农场动物到餐桌上的食物
猪、羊和山羊是将弓形虫从环境带入人类厨房链条中的关键环节。该寄生虫会在这些动物的肌肉和大脑中形成坚韧的包囊,若食用生肉或未煮熟的肉类,这些包囊可能仍具有感染性。传统基于DNA的检测擅长发现样本中是否存在寄生虫的遗传物质,但无法判断寄生虫是活着还是已经死亡——就像发现一辆损毁的车并不能证明它还能行驶。因此,监管机构和研究者仍然依赖小鼠生物测定,将家畜消化处理后的组织注入小鼠体内,并在一个多月的时间里监测其感染迹象。
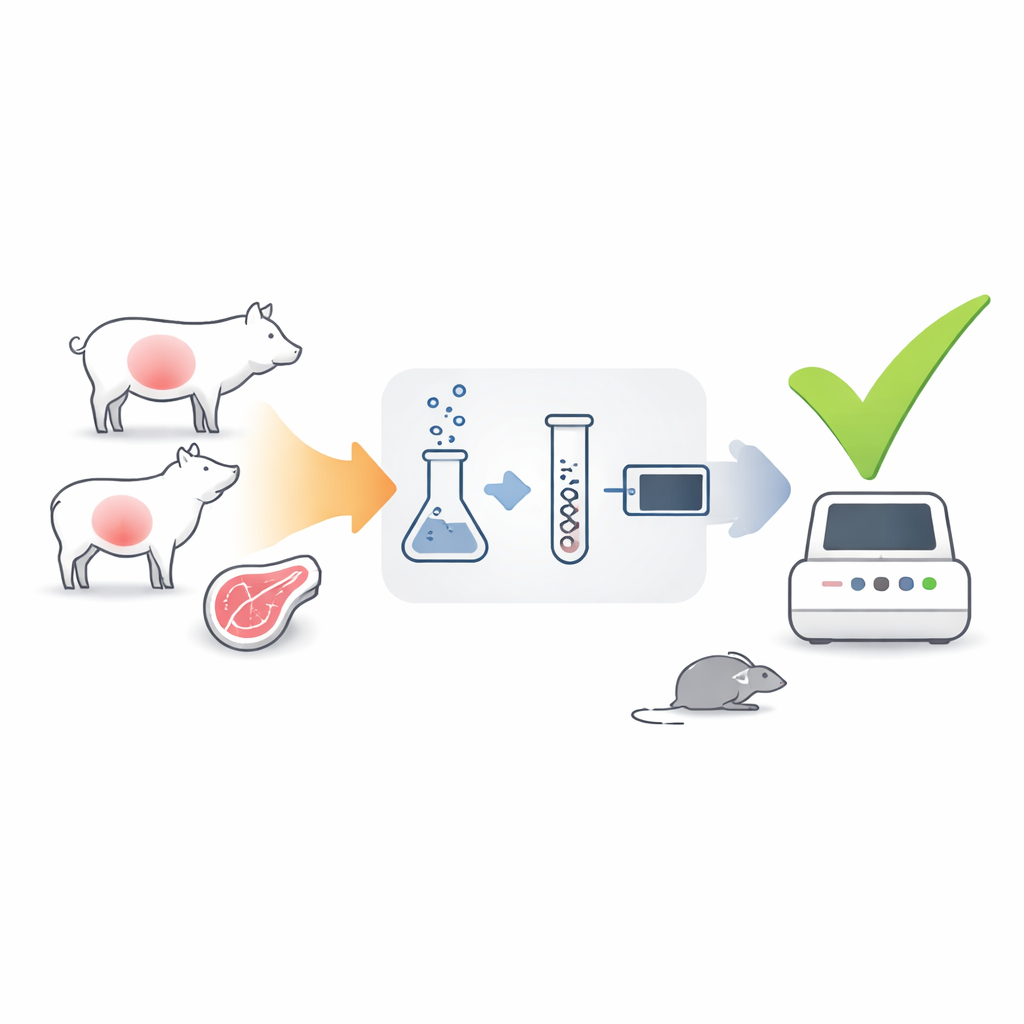
一种监听生命迹象的新方法
作者开发的检测并不侧重于寄生虫的DNA,而是其信使RNA(mRNA)——这些短寿命分子仅由具有活性的细胞产生。他们选择了两个寄生虫基因作为信号:gra1,当寄生虫快速繁殖时该基因高度表达;以及 bag1,当寄生虫进入长期存在的组织包囊时该基因被激活。利用名为 RT-qPCR 的技术,他们将组织样本中的寄生虫 mRNA 逆转录为 DNA 并放大,从而计数 gra1 和 bag1 的拷贝数。由于寄生虫一旦死亡 mRNA 会迅速降解,这些基因的强烈信号应当表明仍存在具有感染性的活寄生虫。
在实验室中检验该检测方法
为验证该思路是否可行,研究团队首先在细胞培养中培养弓形虫,并对寄生虫进行模拟肉类消化和加工过程中可能发生的处理。有些样本仅暴露于消化酶,而另一些则先加热至可杀死寄生虫的温度,再用能破坏残留 RNA 的酶处理。当他们应用 gra1–bag1 RT-qPCR 检测时,存活或仅经酶处理的寄生虫产生了强烈的 mRNA 信号,而经加热杀死的寄生虫几乎没有信号并且无法在新鲜细胞培养中生长。该检测能够可靠地检测到相当于少量寄生虫的水平,且测量结果在不同实验间一致,表明该方法既灵敏又在技术上稳健。
新检测与活体小鼠实验的比较
关键问题是实际动物组织中的 mRNA 水平是否与实际感染风险相匹配。研究者使用了来自已用已知数量弓形虫卵囊感染的仔猪和绵羊的存储肌肉和大脑样本。每个样本并行使用四种方法检测:经典的小鼠生物测定、广泛使用的基于 DNA 的 qPCR、额外的嵌套 PCR,以及新的 gra1–bag1 RT-qPCR。通过比较结果,他们表明 gra1 和 bag1 信号强的组织几乎总是会感染所有暴露的小鼠,而低于某一阈值的 mRNA 水平的样本从未导致感染。当将这些阈值用作判定标准时,mRNA 检测与小鼠生物测定之间的一致性与或优于传统的基于 DNA 的方法。重要的是,只有被预测含有足够多具有实际意义的活性寄生虫的样本才需要进一步进行小鼠检测。
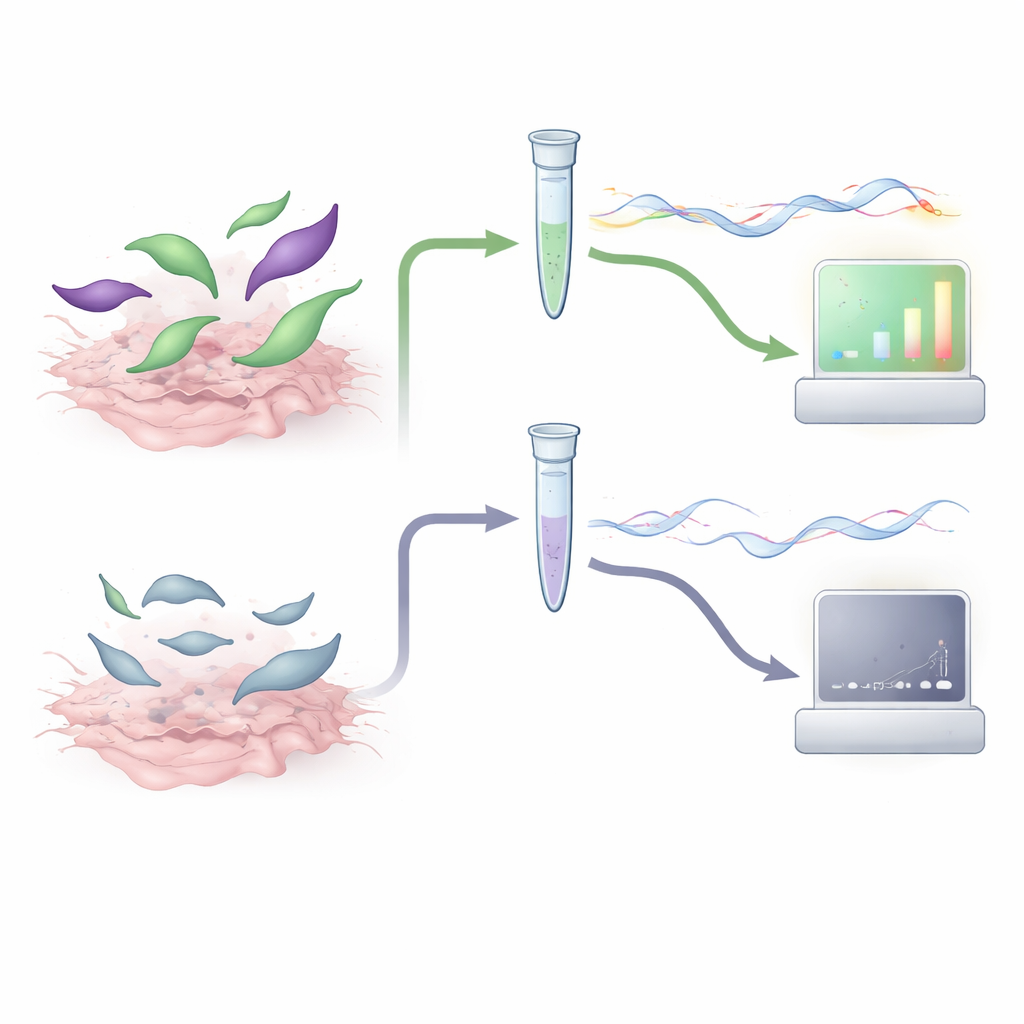
这对更安全的食品和更少的动物实验意味着什么
对非专业人士而言,主要结论是科学家正在接近一种快速且伦理的方法,用以判断肉类中是否含有活的、具有感染性的弓形虫。通过“监听”来自两个关键寄生虫基因的短寿命 mRNA 信号,gra1–bag1 RT-qPCR 检测能够作为预筛查:它能标记出明显含有危险水平活性寄生虫的组织,同时也能让其他样本在寄生虫角度上更有把握地被认为是安全的。尽管还需要在自然感染的动物和加工肉制品中进行更多研究,这一方法最终有望减少食品安全检测中使用的小鼠数量,并帮助监管机构和产业更好地评估哪些肉类对消费者构成真实的弓形虫病风险。
引用: Largo-de la Torre, A., Velasco-Jiménez, N., Ortega-Mora, L.M. et al. Development and validation of a gra1–bag1 RT-qPCR assay as an alternative to the mouse bioassay for assessing Toxoplasma gondii viability. Sci Rep 16, 14370 (2026). https://doi.org/10.1038/s41598-026-43786-0
关键词: 弓形虫病, 食源性寄生虫, PCR 检测, 肉类安全, 无动物检测