Clear Sky Science · de
Entwicklung und Validierung eines gra1–bag1 RT-qPCR-Tests als Alternative zum Maus-Bioassay zur Beurteilung der Lebensfähigkeit von Toxoplasma gondii
Warum dieser winzige Parasit für Ihren Esstisch wichtig ist
Toxoplasma gondii ist ein mikroskopischer Parasit, der weltweit unauffällig durch Nutztiere, Haustiere und Menschen zirkuliert. Die meisten Infektionen verlaufen unbemerkt, doch bei Schwangeren und Menschen mit geschwächtem Immunsystem kann er Fehlgeburten, Hirnschäden bei Neugeborenen und schwere Augenerkrankungen verursachen. Da Menschen sich oft durch den Verzehr von unzureichend gegartem Fleisch infizieren, benötigen Lebensmittelsicherheitsforscher verlässliche Methoden, um festzustellen, ob der Parasit im Fleisch noch lebensfähig und gefährlich ist. Bislang basierte der Goldstandard darauf, lebende Mäuse zu infizieren und Wochen auf Krankheitsanzeichen zu warten—ein Vorgehen, das langsam, teuer ist und zunehmend modernen Tierschutzstandards widerspricht. Diese Studie stellt einen neuen Labortest vor, der darauf abzielt, die Lebensfähigkeit des Parasiten vorherzusagen, ohne so stark auf Tierversuche angewiesen zu sein.
Von Nutztieren bis auf den Teller
Schweine, Schafe und Ziegen sind wichtige Glieder in der Kette, die T. gondii aus der Umwelt in die menschliche Küche bringt. Der Parasit bildet robuste Zysten in ihren Muskeln und im Gehirn, die infektiös bleiben können, wenn das Fleisch roh oder unzureichend gegart verzehrt wird. Herkömmliche DNA-basierte Tests sind gut darin, das Vorhandensein von parasitärer genetischer Substanz in einer Probe zu erkennen, können jedoch nicht unterscheiden, ob der Parasit lebendig oder tot ist—ähnlich wie das Auffinden eines verunglückten Autos nicht beweist, dass es noch fahrbereit ist. Aus diesem Grund verlassen sich Behörden und Forscher weiterhin auf den Maus-Bioassay, bei dem verdautes Gewebe von Nutztieren in Mäuse injiziert wird und die Tiere über mehr als einen Monat auf Infektionszeichen überwacht werden.
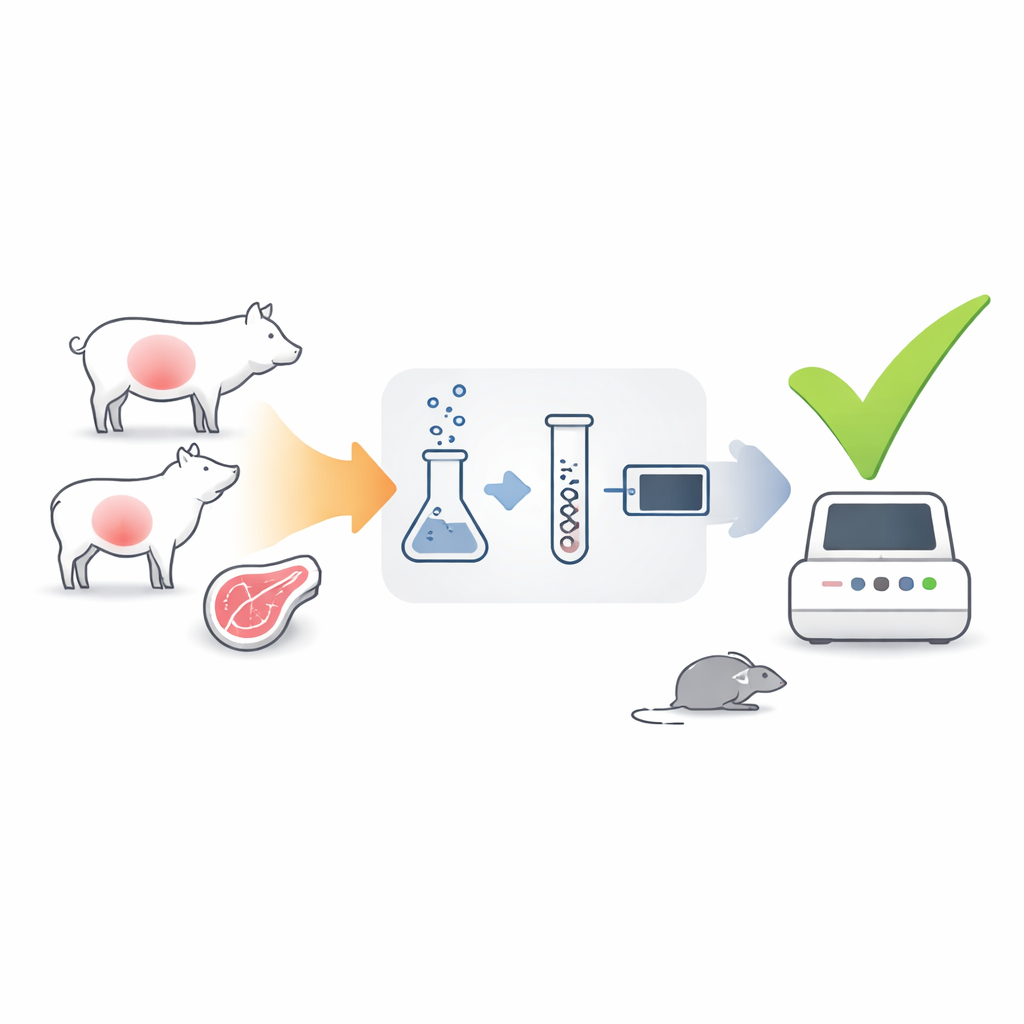
Eine neue Methode, um Lebenszeichen zu „hören”
Die Autorinnen und Autoren entwickelten einen Test, der sich nicht auf die DNA des Parasiten, sondern auf seine Boten-RNA (mRNA) konzentriert—kurzlebige Moleküle, die nur von aktiven, lebenden Zellen produziert werden. Sie wählten zwei Parasiten-Gene als Signale: gra1, das bei rascher Vermehrung des Parasiten stark aktiv ist, und bag1, das hochreguliert wird, wenn der Parasit in langlebigen Gewebszysten verharrt. Mit einer Technik namens RT-qPCR wandelten sie parasitäre mRNA aus Gewebeproben in DNA um und amplifizierten diese anschließend, so dass sie zählen konnten, wie viele Kopien von gra1 und bag1 vorhanden waren. Da mRNA nach dem Absterben eines Parasiten schnell abgebaut wird, sollten starke Signale dieser Gene anzeigen, dass noch infektiöse Parasiten vorhanden sind.
Erprobung des Tests im Labor
Um zu prüfen, ob diese Idee funktioniert, züchtete das Team zunächst T. gondii in Zellkultur und unterzog die Parasiten Behandlungen, die dem Vorgehen bei der Fleischverdauung und -verarbeitung ähneln. Einige Proben wurden einfach Verdauungsenzymen ausgesetzt, andere wurden auf Temperaturen erhitzt, die den Parasiten abtöten, und dann mit Enzymen behandelt, die verbliebene RNA zerstören. Als sie ihren gra1–bag1 RT-qPCR-Test anwandten, zeigten lebende oder nur enzymatisch behandelte Parasiten starke mRNA-Signale, während hitzegetötete Parasiten nahezu keine Signale erzeugten und sich in frischen Zellkulturen nicht vermehrten. Der Test konnte zuverlässig bereits die Entsprechung von nur wenigen Parasiten nachweisen, und die Messungen waren von Durchgang zu Durchgang konsistent, was darauf hindeutet, dass der Assay sowohl empfindlich als auch technisch robust ist.
Wie der neue Test im Vergleich zu Versuchen an lebenden Mäusen abschneidet
Die entscheidende Frage war, ob die mRNA-Spiegel in echten Tiergeweben dem tatsächlichen Infektionsrisiko entsprechen. Die Forschenden verwendeten gelagerte Muskel- und Gehirnproben von Ferkeln und Schafen, die experimentell mit bekannten Mengen T. gondii-Oozysten infiziert worden waren. Jede Probe wurde parallel mit vier Methoden getestet: dem klassischen Maus-Bioassay, einer weit verbreiteten DNA-basierten qPCR, einer zusätzlichen Nested-PCR und der neuen gra1–bag1 RT-qPCR. Durch Vergleich der Ergebnisse zeigten sie, dass Gewebe mit hohen gra1- und bag1-Signalen fast immer alle exponierten Mäuse infizierten, während Proben mit mRNA-Werten unterhalb einer bestimmten Schwelle niemals eine Infektion verursachten. Wenn sie diese Schwellen als Cutoffs verwendeten, war die Übereinstimmung zwischen dem mRNA-Test und dem Maus-Bioassay vergleichbar mit oder besser als bei traditionellen DNA-basierten Methoden. Wichtig ist, dass nur Proben, bei denen vorhergesagt wurde, dass sie genügend lebensfähige Parasiten enthalten, um relevant zu sein, weiterhin einer Maus-Testung unterzogen werden müssten.
Was das für sicherere Lebensmittel und weniger Tierversuche bedeutet
Für Nichtfachleute lautet die Kernbotschaft, dass Forschende einer schnellen, ethischen Methode näherkommen, um zu entscheiden, ob Fleisch lebendige, infektiöse T. gondii enthält. Indem der Test kurzlebige mRNA-Signale von zwei Schlüsselgenen des Parasiten „abhört“, kann der gra1–bag1 RT-qPCR-Assay als Vorscreening dienen: Er markiert Gewebe, die eindeutig gefährliche Mengen lebensfähiger Parasiten beherbergen, und gibt die Sicherheit, dass andere Proben aus Sicht des Parasiten effektiv unbedenklich sind. Zwar ist weitere Arbeit an natürlich infizierten Tieren und verarbeiteten Fleischprodukten erforderlich, doch könnte dieser Ansatz langfristig die Anzahl der für die Lebensmittelsicherheit eingesetzten Mäuse reduzieren und Behörden sowie der Industrie helfen, besser einzuschätzen, welche Fleischprodukte für Verbraucher ein reales Risiko einer Toxoplasmose darstellen.
Zitation: Largo-de la Torre, A., Velasco-Jiménez, N., Ortega-Mora, L.M. et al. Development and validation of a gra1–bag1 RT-qPCR assay as an alternative to the mouse bioassay for assessing Toxoplasma gondii viability. Sci Rep 16, 14370 (2026). https://doi.org/10.1038/s41598-026-43786-0
Schlüsselwörter: Toxoplasmose, lebensmittelübertragene Parasiten, PCR-Tests, Fleischsicherheit, tierfreie Tests