Clear Sky Science · ja
マウス生体試験の代替としてのgra1–bag1 RT-qPCRアッセイの開発と検証:Toxoplasma gondiiの生存性評価
なぜこの小さな寄生虫が食卓に関係するのか
Toxoplasma gondii(トキソプラズマ・ゴンディイ)は、世界中の家畜、ペット、人を静かに循環する微小な寄生虫です。ほとんどの感染は気づかれませんが、妊婦や免疫が低下している人では流産、新生児の脳損傷、重篤な眼疾患を引き起こすことがあります。人はしばしば加熱不十分な肉を食べることで感染するため、食品安全の専門家は肉中の寄生虫がまだ生きていて危険かどうかを判断する信頼できる方法が必要です。これまでのゴールドスタンダードは生きたマウスに感染させ、数週間にわたって病徴を待つという方法で—遅く、費用がかかり、動物福祉の観点から問題が増しているアプローチでした。本研究は、動物実験に大きく依存せずに寄生虫の生存性を予測することを目指した新しい検査法を提示します。
家畜から皿の上の食べ物へ
ブタ、羊、ヤギは環境中のT. gondiiを人間の食卓へつなぐ重要な中継点です。寄生虫は筋肉や脳に耐久性のある嚢胞を形成し、生肉や加熱不十分な肉を食べると感染性を保ったままでいることがあります。従来のDNAベースの検査は試料中に寄生虫の遺伝物質が存在するかを検出するのに優れていますが、それが生きているか死んでいるかは判別できません—壊れた車が見つかっても走れるかどうかは分からないのと同じです。そのため、規制当局や研究者は、家畜組織を消化してからマウスに注射し、1か月以上にわたって感染の有無を観察するというマウス生体試験に依然依存してきました。
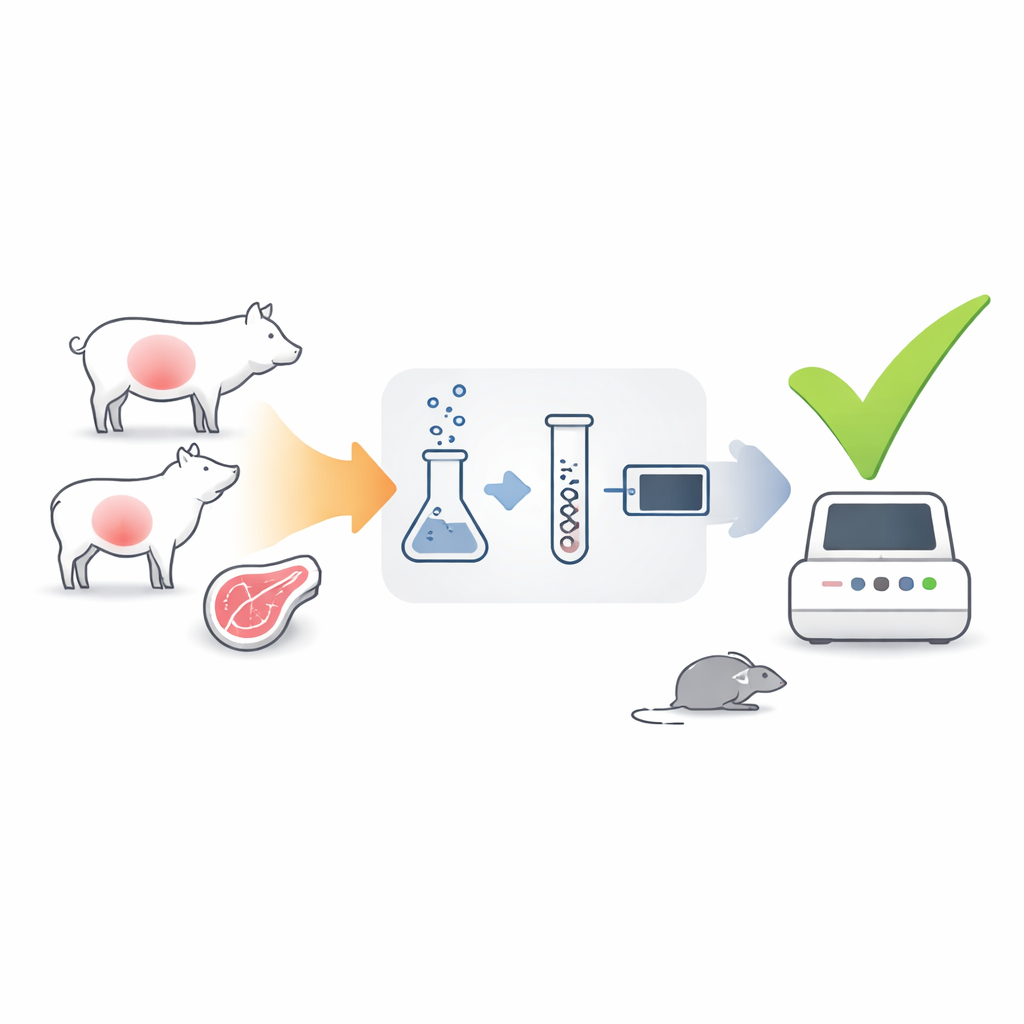
生命の兆候を聞き分ける新しい方法
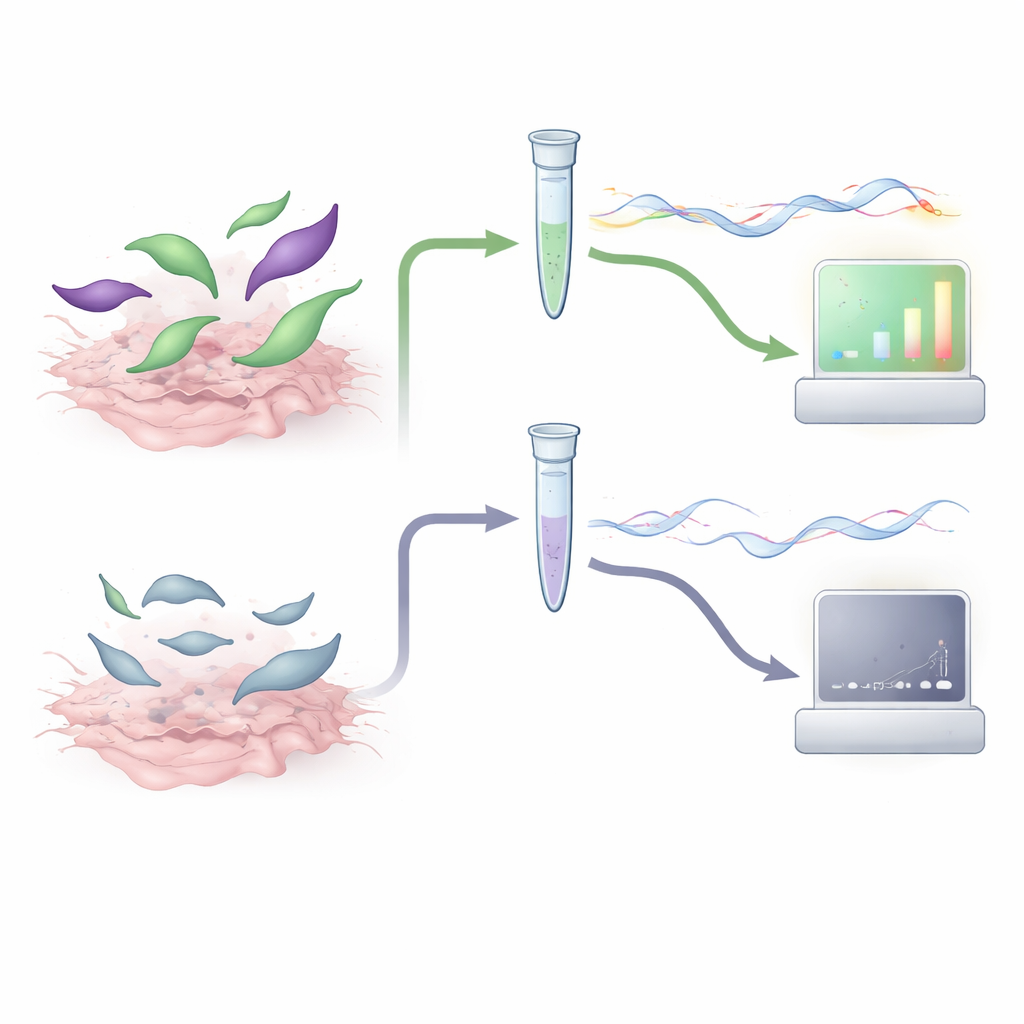
著者らは寄生虫のDNAではなく、メッセンジャーRNA(mRNA)に着目した検査を開発しました。mRNAは短寿命であり、活動中の生細胞だけが産生します。彼らは寄生虫の2つの遺伝子を指標として選びました。gra1は寄生虫が急速に増殖しているときに強く発現し、bag1は長期にわたる組織嚢胞の状態にあるときにオンになる遺伝子です。RT-qPCRという手法を用いて、組織試料から寄生虫mRNAを逆転写してDNAに変換し、それを増幅してgra1とbag1のコピー数を算出しました。mRNAは寄生虫が死ぬと急速に分解されるため、これらの遺伝子の強いシグナルは感染性のある寄生虫が存在することを示すはずです。
実験室での徹底的な検証
この方法が機能するかを確かめるために、研究チームはまず培養細胞でT. gondiiを増やし、肉の消化や加熱処理を模した処理を行いました。ある試料は消化酵素にさらされ、別の試料は寄生虫を殺すレベルまで加熱され、その後残存するRNAを破壊する酵素処理を受けました。gra1–bag1 RT-qPCRを適用したところ、生存または酵素処理のみの寄生虫は強いmRNAシグナルを示したのに対し、加熱で死滅させた寄生虫はほとんどシグナルを示さず、新しい培養でも増殖しませんでした。このアッセイはほんの数個の寄生虫に相当する量を確実に検出でき、測定は繰り返し間で一貫しており、感度が高く技術的に頑健であることが示唆されました。
新しい検査はマウス実験とどう比べられるか
重要な問いは、実際の動物組織におけるmRNAレベルが感染の実際のリスクと一致するかどうかでした。研究者らは既知数のT. gondiiオーシストで実験感染させた子ブタと羊の保存されている筋肉および脳試料を用いました。各試料は古典的なマウス生体試験、広く用いられるDNAベースのqPCR、追加のネスティッドPCR、および新しいgra1–bag1 RT-qPCRの四つの方法で並行して検査されました。比較の結果、高いgra1およびbag1シグナルを示す組織は、暴露されたマウスのすべてにほぼ確実に感染を引き起こし、一方でmRNAレベルがある閾値以下の試料は感染を引き起こしませんでした。これらの閾値をカットオフとして用いると、mRNA検査とマウス生体試験の一致度は従来のDNAベースの方法と同等かそれ以上でした。重要なのは、実際に問題となる十分な生存寄生虫を含むと予測される試料だけがマウス検査に回されればよい、という点です。
より安全な食品と動物実験の削減に向けて
専門外の人向けの結論としては、科学者たちは肉に生きた感染性のT. gondiiが含まれているかを迅速かつ倫理的に判断する手段に近づいているということです。二つの主要な寄生虫遺伝子からの短命なmRNAシグナルを“聞き取る”ことで、gra1–bag1 RT-qPCRアッセイはプレスクリーニングとして機能します。危険なレベルの生存寄生虫を明確に含む組織を特定し、その他の試料は寄生虫の観点から実質的に安全であることを示します。自然感染動物や加工肉製品でのさらなる検証が必要ですが、この手法は将来、食品安全検査で使用されるマウスの数を減らし、規制当局や業界が消費者にとって実際にトキソプラズマ症のリスクがある肉をより適切に評価するのに役立つ可能性があります。
引用: Largo-de la Torre, A., Velasco-Jiménez, N., Ortega-Mora, L.M. et al. Development and validation of a gra1–bag1 RT-qPCR assay as an alternative to the mouse bioassay for assessing Toxoplasma gondii viability. Sci Rep 16, 14370 (2026). https://doi.org/10.1038/s41598-026-43786-0
キーワード: トキソプラズマ症, 食品由来寄生虫, PCR検査, 肉の安全性, 動物を使わないアッセイ