Clear Sky Science · fr
Développement et validation d’un test RT-qPCR gra1–bag1 comme alternative au bioessai sur souris pour évaluer la viabilité de Toxoplasma gondii
Pourquoi ce minuscule parasite a de l’importance pour votre assiette
Toxoplasma gondii est un parasite microscopique qui circule discrètement chez les animaux d’élevage, les animaux de compagnie et les humains dans le monde entier. La plupart des infections passent inaperçues, mais chez les femmes enceintes et les personnes immunodéprimées il peut provoquer des fausses couches, des lésions cérébrales chez les nouveau‑nés et des atteintes oculaires graves. Comme l’homme est souvent infecté en consommant de la viande insuffisamment cuite, les spécialistes de la sécurité alimentaire ont besoin de méthodes fiables pour savoir si le parasite présent dans la viande est encore vivant et dangereux. Jusqu’à présent, le test de référence consistait à infecter des souris vivantes et à attendre des semaines l’apparition de signes de maladie — une approche lente, coûteuse et de plus en plus en désaccord avec les normes modernes de bien‑être animal. Cette étude présente un nouveau test de laboratoire qui vise à prédire la viabilité du parasite sans dépendre autant des expériences sur animaux.
Des animaux d’élevage à l’assiette
Les porcs, les moutons et les chèvres sont des maillons clés dans la chaîne qui transporte T. gondii de l’environnement vers les cuisines humaines. Le parasite forme des kystes résistants dans leurs muscles et leurs cerveaux, qui peuvent rester infectieux si la viande est consommée crue ou insuffisamment cuite. Les tests classiques basés sur l’ADN sont efficaces pour détecter la présence de matériel génétique du parasite dans un échantillon, mais ils ne peuvent pas dire si le parasite est vivant ou mort — comme trouver une voiture accidentée ne prouve pas qu’elle peut encore rouler. Pour cette raison, les autorités et les chercheurs ont continué à s’appuyer sur le bioessai sur souris, dans lequel un tissu digéré provenant d’animaux d’élevage est injecté à des souris qui sont ensuite surveillées pendant plus d’un mois pour détecter une infection.
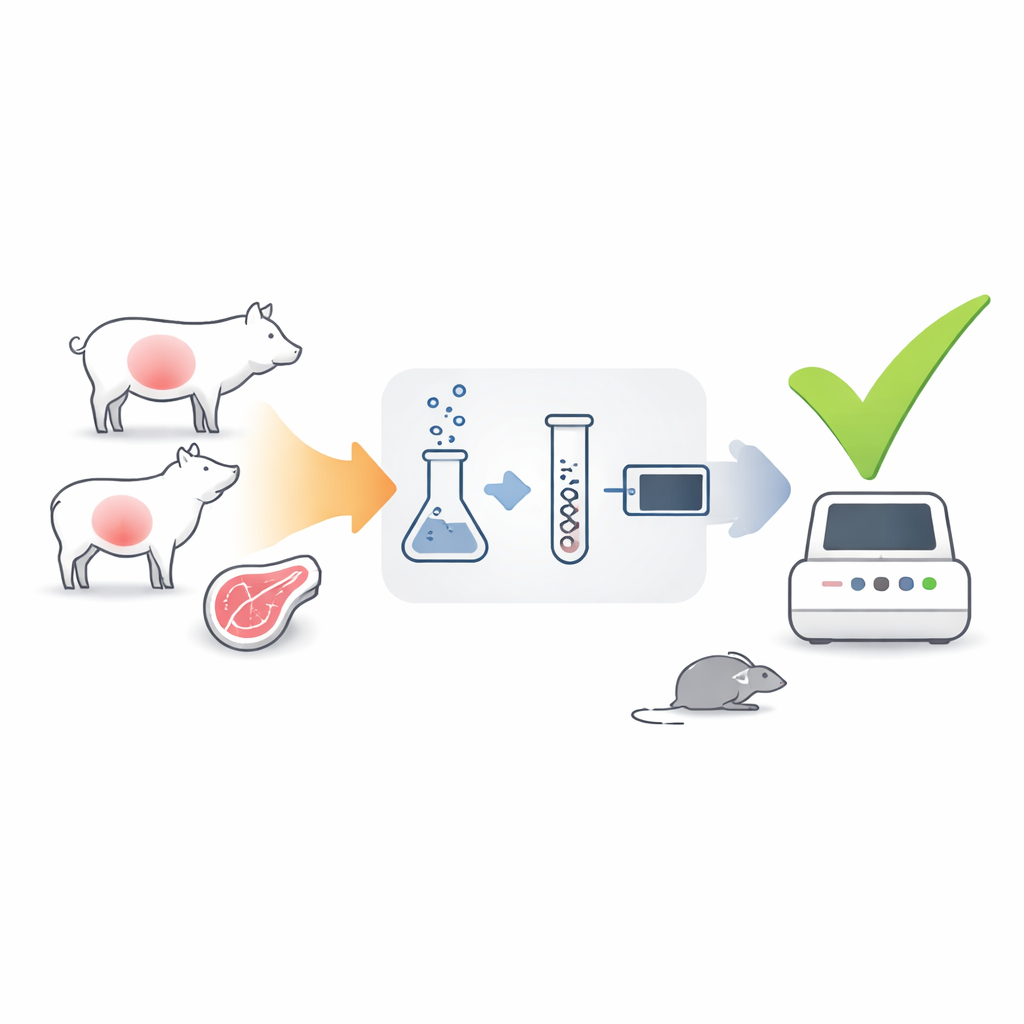
Une nouvelle façon d’écouter les signes de vie
Les auteurs ont développé un test qui se concentre non pas sur l’ADN du parasite, mais sur son ARN messager (ARNm) — des molécules transitoires produites uniquement par des cellules actives et vivantes. Ils ont choisi deux gènes du parasite comme témoins : gra1, fortement exprimé quand le parasite se multiplie rapidement, et bag1, activé lorsqu’il se met en dormance dans des kystes tissulaires de longue durée. À l’aide d’une technique appelée RT‑qPCR, ils ont converti l’ARNm parasitaire des échantillons tissulaires en ADN puis l’ont amplifié, ce qui leur a permis de compter le nombre de copies de gra1 et bag1 présentes. Parce que l’ARNm se dégrade rapidement après la mort du parasite, des signaux forts provenant de ces gènes devraient indiquer la présence de parasites infectieux.
Éprouver le test en laboratoire
Pour vérifier si l’idée fonctionnait, l’équipe a d’abord cultivé T. gondii en culture cellulaire et soumis les parasites à des traitements mimant ce qui se produit lors de la digestion et du traitement de la viande. Certains échantillons ont simplement été exposés à des enzymes digestives, d’autres chauffés à des températures létales pour le parasite puis traités avec des enzymes détruisant l’ARN résiduel. Lorsqu’ils ont appliqué leur test RT‑qPCR gra1–bag1, les parasites vivants ou traités aux enzymes ont donné des signaux d’ARNm forts, tandis que les parasites tués par la chaleur en ont produit presque aucun et n’ont pas pu croître dans des cultures cellulaires fraîches. Le test pouvait détecter de manière fiable l’équivalent d’une poignée de parasites, et les mesures étaient cohérentes d’une série à l’autre, ce qui suggère que l’essai est à la fois sensible et techniquement robuste.
Comment le nouveau test se compare aux expériences sur souris vivantes
La question cruciale était de savoir si les niveaux d’ARNm dans de vrais tissus animaux reflétaient le risque réel d’infection. Les chercheurs ont utilisé des échantillons musculaires et cérébraux conservés de porcelets et de moutons qui avaient été infectés expérimentalement avec des nombres connus d’oocystes de T. gondii. Chaque échantillon a été testé en parallèle par quatre méthodes : le classique bioessai sur souris, une qPCR basée sur l’ADN largement utilisée, une PCR nichée supplémentaire et la nouvelle RT‑qPCR gra1–bag1. En comparant les résultats, ils ont montré que les tissus présentant des signaux élevés de gra1 et bag1 infectaient presque toujours toutes les souris exposées, tandis que les échantillons avec des niveaux d’ARNm en dessous d’un certain seuil ne causaient jamais d’infection. En utilisant ces seuils comme valeurs de coupure, la concordance entre le test d’ARNm et le bioessai sur souris était comparable ou supérieure à celle des méthodes traditionnelles basées sur l’ADN. Fait important, seuls les échantillons prédits comme contenant suffisamment de parasites viables pour être significatifs auraient besoin d’être soumis à un test sur souris.
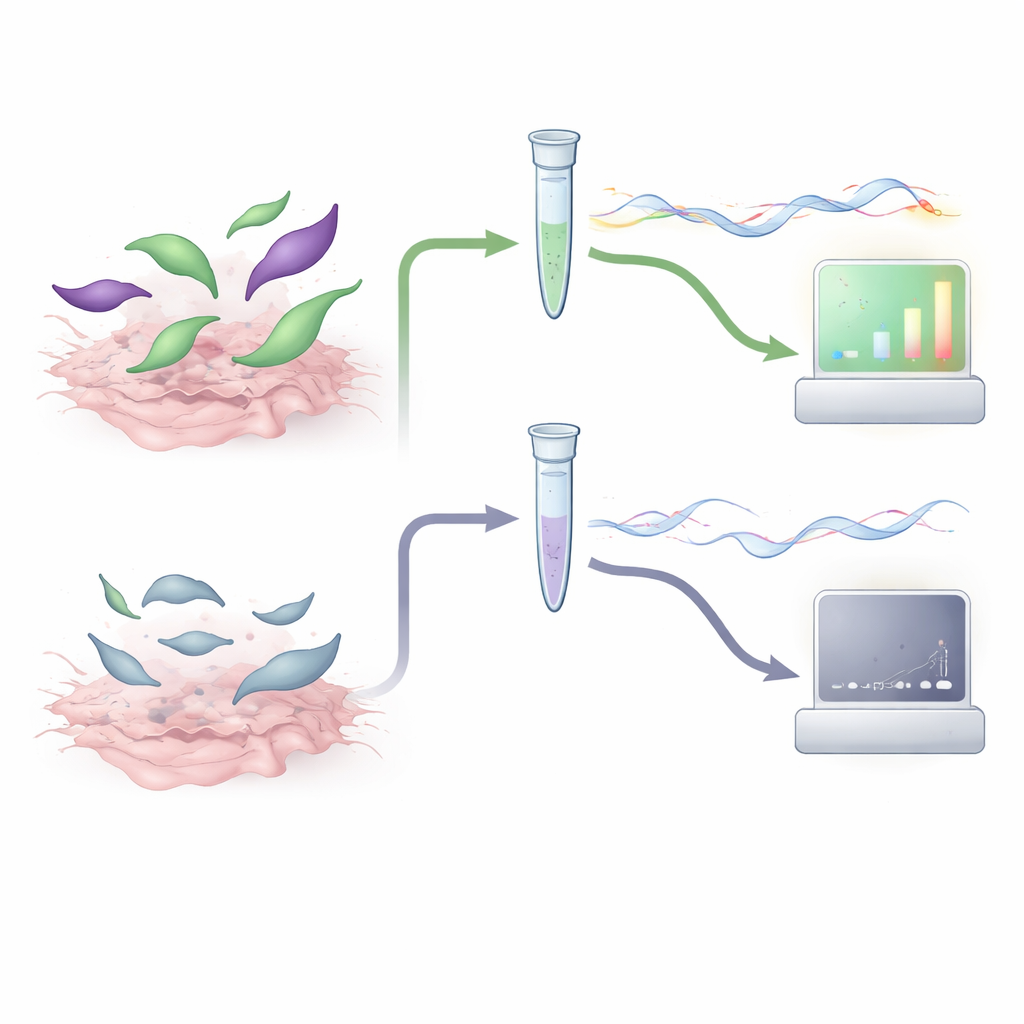
Ce que cela signifie pour une alimentation plus sûre et moins d’expérimentations animales
Pour le non‑spécialiste, le message essentiel est que les scientifiques se rapprochent d’une méthode rapide et éthique pour déterminer si la viande contient des T. gondii vivants et infectieux. En « écoutant » des signaux d’ARNm de courte durée issus de deux gènes clés du parasite, le test RT‑qPCR gra1–bag1 peut servir de présélection : il identifie les tissus qui abritent clairement des niveaux dangereux de parasites viables, et il rassure sur le fait que d’autres sont effectivement sûrs du point de vue du parasite. Bien que des travaux supplémentaires soient nécessaires sur des animaux infectés naturellement et sur des produits carnés transformés, cette approche pourrait à terme réduire le nombre de souris utilisées dans les tests de sécurité alimentaire et aider les autorités et l’industrie à mieux évaluer quelles viandes présentent un risque réel de toxoplasmose pour les consommateurs.
Citation: Largo-de la Torre, A., Velasco-Jiménez, N., Ortega-Mora, L.M. et al. Development and validation of a gra1–bag1 RT-qPCR assay as an alternative to the mouse bioassay for assessing Toxoplasma gondii viability. Sci Rep 16, 14370 (2026). https://doi.org/10.1038/s41598-026-43786-0
Mots-clés: toxoplasmose, parasites d’origine alimentaire, tests PCR, sûreté de la viande, tests sans animaux