Clear Sky Science · nl
Ontwikkeling en validatie van een gra1–bag1 RT-qPCR-test als alternatief voor de muizen-bioassay om de levensvatbaarheid van Toxoplasma gondii te beoordelen
Waarom deze kleine parasiet ertoe doet aan uw eettafel
Toxoplasma gondii is een microscopische parasiet die wereldwijd geruisloos circuleert tussen landbouwdieren, huisdieren en mensen. De meeste infecties blijven onopgemerkt, maar bij zwangere vrouwen en mensen met een verzwakt immuunsysteem kan de parasiet een miskraam, hersenbeschadiging bij pasgeborenen en ernstige oogziekten veroorzaken. Omdat mensen vaak besmet raken door het eten van onvoldoende verhit vlees, hebben voedselveiligheidswetenschappers betrouwbare methoden nodig om te bepalen of de parasiet in vlees nog leeft en gevaarlijk is. Tot nu toe bestond de gouden standaard uit het infecteren van levende muizen en het wekenlang afwachten op ziektesymptomen — een aanpak die traag, duur en steeds minder verenigbaar is met moderne dierenwelzijnsnormen. Deze studie presenteert een nieuwe laboratoriumtest die gericht is op het voorspellen van parasietlevensvatbaarheid zonder zo zwaar te steunen op dierexperimenten.
Van boerderijdieren naar voedsel op het bord
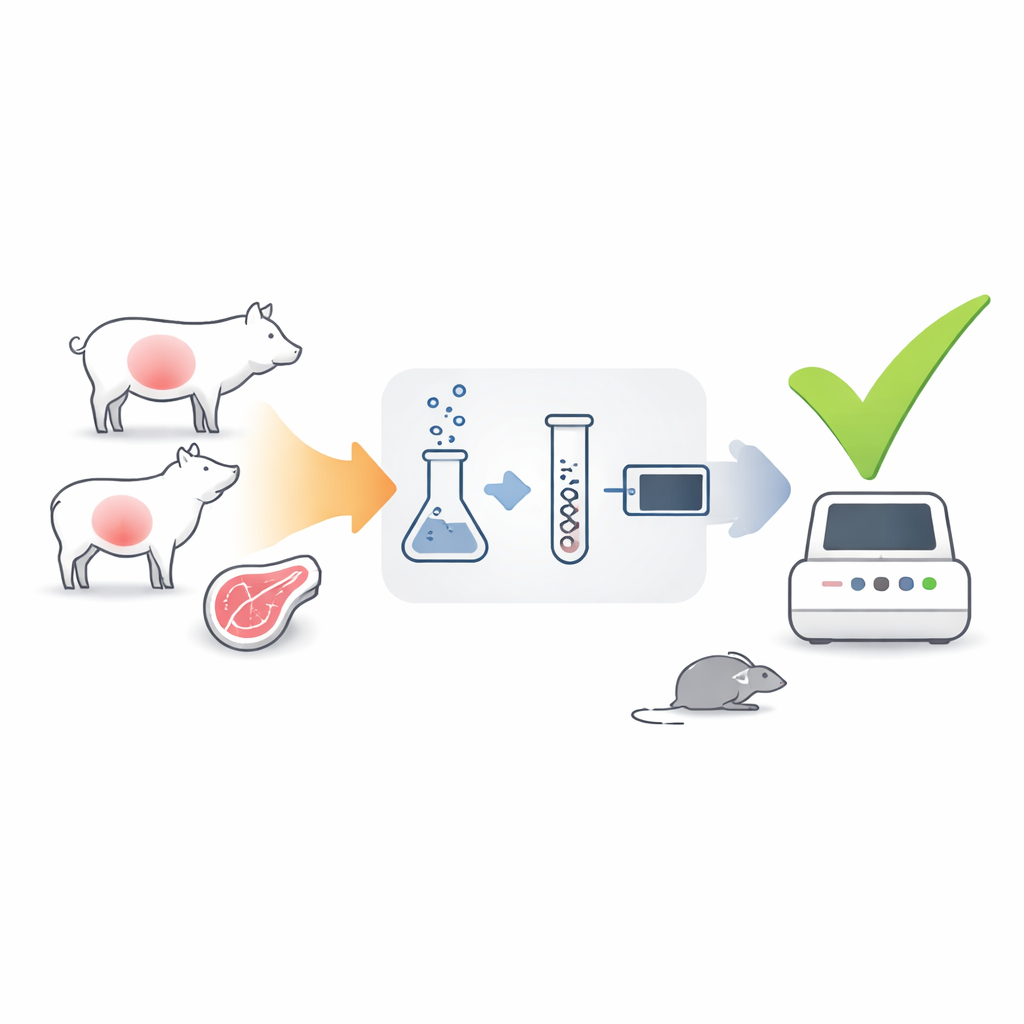
Varkens, schapen en geiten vormen belangrijke schakels in de keten die T. gondii van de omgeving naar menselijke keukens brengt. De parasiet vormt hardnekkige cysten in hun spieren en hersenen, die besmettelijk kunnen blijven als het vlees rauw of onvoldoende verhit wordt gegeten. Traditionele DNA-gebaseerde tests zijn goed in het opsporen van parasietmateriaal in een monster, maar ze kunnen niet aantonen of die parasiet levend of dood is — net zoals het vinden van een verongelukte auto niet bewijst dat die nog kan rijden. Om die reden bleven toezichthouders en onderzoekers vertrouwen op de muizen-bioassay, waarbij verteerd weefsel van vee in muizen wordt geïnjecteerd en de dieren meer dan een maand worden bewaakt op tekenen van infectie.
Een nieuwe manier om naar levenssignalen te luisteren
De auteurs ontwikkelden een test die zich niet richt op het DNA van de parasiet, maar op zijn boodschapper-RNA (mRNA) — kortlevende moleculen die alleen door actieve, levende cellen worden geproduceerd. Ze kozen twee parasietgenen als signaalgevers: gra1, dat sterk actief is wanneer de parasiet zich snel vermenigvuldigt, en bag1, dat wordt aangeschakeld wanneer de parasiet zich opsluit in langlevende weefselcysten. Met een techniek genaamd RT-qPCR zetten ze parasiet-mRNA uit weefselmonsters om in DNA en versterkten dat vervolgens, waardoor ze konden tellen hoeveel kopieën van gra1 en bag1 aanwezig waren. Omdat mRNA snel afbreekt zodra een parasiet sterft, zouden sterke signalen van deze genen moeten aangeven dat er nog infectieuze parasieten aanwezig zijn.
De test op de proef stellen in het laboratorium
Om te beoordelen of dit idee werkte, kweekte het team eerst T. gondii in celculturen en bracht de parasieten aan behandelingen die nabootsen wat er gebeurt tijdens vertering en verwerking van vlees. Sommige monsters werden simpelweg blootgesteld aan spijsverteringsenzymen, terwijl andere werden verhit tot temperaturen die de parasiet doden en vervolgens werden behandeld met enzymen die achtergebleven RNA vernietigen. Toen ze hun gra1–bag1 RT-qPCR-test toepasten, gaven levende of enzymbehandelde parasieten sterke mRNA-signalen, terwijl verhitte, gedode parasieten vrijwel geen signaal produceerden en niet konden uitgroeien in verse celculturen. De test kon betrouwbaar het equivalent van slechts een handvol parasieten detecteren, en de metingen waren consistent van run tot run, wat suggereert dat de assay zowel gevoelig als technisch robuust is.
Hoe de nieuwe test zich verhoudt tot experimenten met levende muizen
De cruciale vraag was of mRNA-niveaus in echte dierweefsels overeenkomen met het werkelijke infectierisico. De onderzoekers gebruikten opgeslagen spier- en hersenmonsters van biggen en schapen die experimenteel waren geïnfecteerd met bekende aantallen T. gondii-oöcysten. Elk monster werd parallel getest met vier methoden: de klassieke muizen-bioassay, een veelgebruikte DNA-gebaseerde qPCR, een aanvullende geneste PCR en de nieuwe gra1–bag1 RT-qPCR. Door de resultaten te vergelijken, toonden ze aan dat weefsels met hoge gra1- en bag1-signalen bijna altijd alle muizen die eraan werden blootgesteld, infecteerden, terwijl monsters met mRNA-niveaus onder een bepaalde drempel nooit infectie veroorzaakten. Wanneer ze deze drempels als afkapwaarden gebruikten, was de overeenstemming tussen de mRNA-test en de muizen-bioassay vergelijkbaar met of beter dan traditionele DNA-gebaseerde methoden. Belangrijk is dat alleen monsters die voorspeld werden voldoende levensvatbare parasieten te bevatten om relevant te zijn, door zouden hoeven naar muizentests.
Wat dit betekent voor veiliger voedsel en minder dierproeven
Voor niet-specialisten komt de hoofdboodschap neer op het feit dat wetenschappers dichter bij een snelle, ethische manier komen om te bepalen of vlees levende, infectieuze T. gondii bevat. Door te “luisteren” naar kortlevende mRNA-signalen van twee sleutelgenen van de parasiet, kan de gra1–bag1 RT-qPCR-assay fungeren als een voorselectie: ze geeft aan welke weefsels duidelijk gevaarlijke niveaus van levensvatbare parasieten herbergen, en ze biedt zekerheid dat andere weefsels vanuit het perspectief van de parasiet effectief veilig zijn. Hoewel er meer werk nodig is bij natuurlijk geïnfecteerde dieren en verwerkte vleesproducten, zou deze benadering uiteindelijk het aantal gebruikte muizen in voedselveiligheidstests kunnen verminderen en toezichthouders en de industrie kunnen helpen beter in te schatten welke vleessoorten een reëel risico op toxoplasmose voor consumenten vormen.
Bronvermelding: Largo-de la Torre, A., Velasco-Jiménez, N., Ortega-Mora, L.M. et al. Development and validation of a gra1–bag1 RT-qPCR assay as an alternative to the mouse bioassay for assessing Toxoplasma gondii viability. Sci Rep 16, 14370 (2026). https://doi.org/10.1038/s41598-026-43786-0
Trefwoorden: toxoplasmose, voedselovergedragen parasieten, PCR-testen, vleesveiligheid, dierloze assays