Clear Sky Science · sv
Utveckling och validering av ett gra1–bag1 RT-qPCR-test som alternativ till mus-bioassayet för att bedöma Toxoplasma gondii‑viabilitet
Varför denna lilla parasit spelar roll vid middagsbordet
Toxoplasma gondii är en mikroskopisk parasit som tyst cirkulerar bland lantbruksdjur, sällskapsdjur och människor världen över. De flesta infektioner passerar obemärkt, men hos gravida kvinnor och personer med försvagat immunförsvar kan parasiten orsaka missfall, hjärnskador hos nyfödda och allvarlig ögonsjukdom. Eftersom människor ofta smittas genom att äta otillräckligt tillagat kött behöver livsmedelssäkerhetsforskare tillförlitliga metoder för att avgöra om parasiten i köttet fortfarande är levande och farlig. Hittills har guldstandarden varit ett test som involverar att smitta levande möss och vänta veckor på sjukdomssymptom—en metod som är långsam, kostsam och i allt större utsträckning strider mot moderna djurvälfärdsprinciper. Denna studie presenterar ett nytt laboratorietest som syftar till att förutsäga parasitens viabilitet utan att så starkt förlita sig på djurförsök.
Från lantbruk till tallriken
Grisar, får och getter är viktiga länkar i kedjan som för T. gondii från miljön till människors kök. Parasiten bildar tåliga cystor i deras muskler och hjärnor, vilka kan förbli infektiösa om köttet äts rått eller otillräckligt tillagat. Traditionella DNA‑baserade tester är bra på att upptäcka om parasitens genetiska material finns i ett prov, men de kan inte avgöra om parasiten är levande eller död—ungefär som att hitta en kraschad bil inte bevisar att den fortfarande kan köra. Av den anledningen har reglerande myndigheter och forskare fortsatt att förlita sig på mus‑bioassayet, där nedbrutet vävnadsmaterial från produktionsdjur injiceras i möss som sedan övervakas för smittsymptom under mer än en månad.
Ett nytt sätt att lyssna efter livstecken
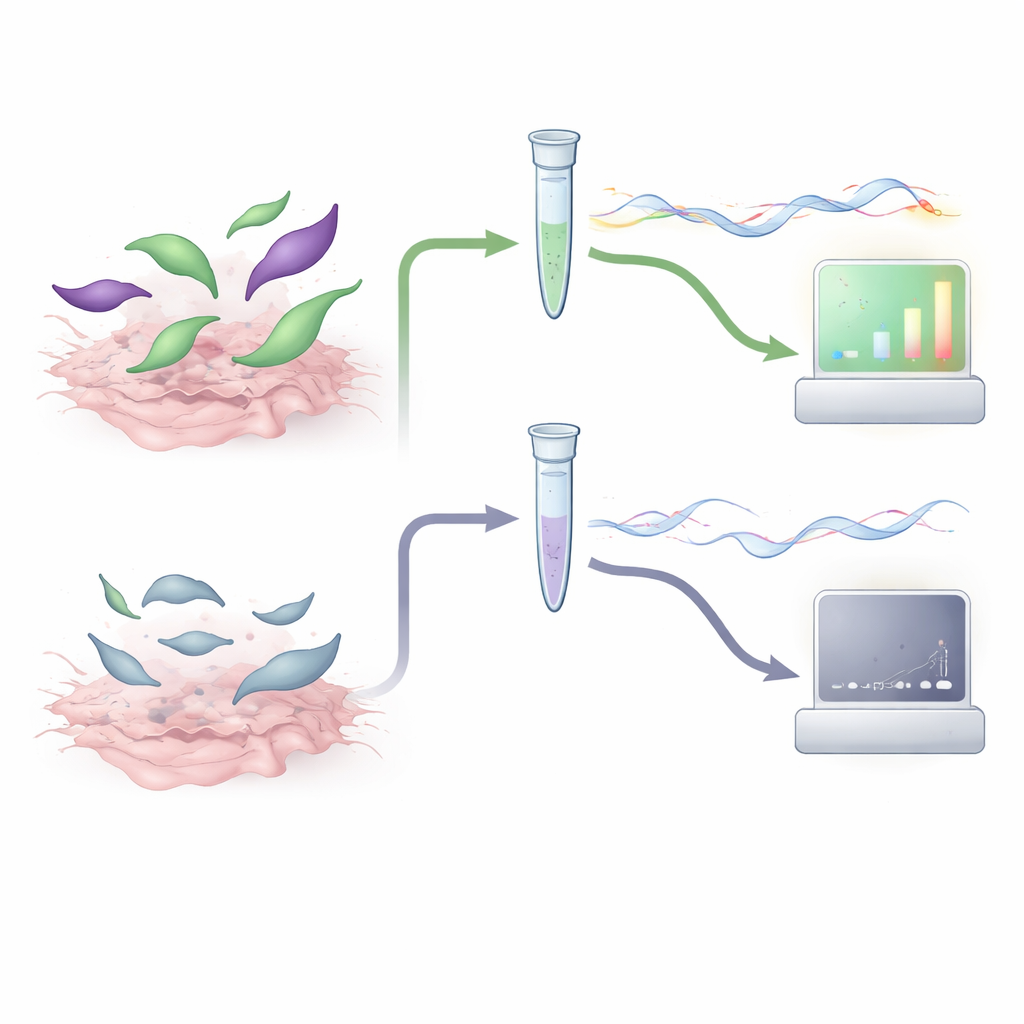
Forskarnas test fokuserar inte på parasitens DNA utan på dess budbärar‑RNA (mRNA)—kortlivade molekyler som endast produceras av aktiva, levande celler. De valde två parasitgener som signaler: gra1, som är mycket aktiv när parasiten snabbt förökar sig, och bag1, som slås på när den går in i långlivade vävnadscystformer. Med hjälp av en teknik kallad RT‑qPCR omvandlade de parasitens mRNA från vävnadsprov till DNA och amplifierade det, vilket gjorde det möjligt att räkna hur många kopior av gra1 och bag1 som fanns. Eftersom mRNA bryts ner snabbt när en parasit dör bör starka signaler från dessa gener tyda på att infektiösa parasiter fortfarande förekommer.
Att pröva testet i laboratoriet
För att undersöka om idén fungerade odlade teamet först T. gondii i cellkulturer och utsatte parasiterna för behandlingar som efterliknar vad som händer vid matsmältning och köttbearbetning. Vissa prover exponerades enbart för matsmältningsenzymer, medan andra värmebehandlades till nivåer som dödar parasiten och sedan behandlades med enzymer som förstör kvarvarande RNA. När de tillämpade sitt gra1–bag1 RT‑qPCR‑test gav levande eller enzymbehandlade parasiter starka mRNA‑signaler, medan värmedödade parasiter producerade nästan inga och inte kunde växa i friska cellkulturer. Testet kunde pålitligt detektera motsvarigheten till bara ett fåtal parasiter, och mätningarna var konsekventa mellan körningar, vilket tyder på att analysen både är känslig och tekniskt robust.
Hur det nya testet står sig mot försök med levande möss
Den avgörande frågan var om mRNA‑nivåerna i verkliga djurvävnader speglar den faktiska infektionsrisken. Forskarna använde lagrade muskel‑ och hjärnprover från kultingar och får som experimentellt infekterats med kända antal T. gondii‑oocyster. Varje prov testades parallellt med fyra metoder: det klassiska mus‑bioassayet, en mycket använd DNA‑baserad qPCR, en ytterligare nested PCR och den nya gra1–bag1 RT‑qPCR. Genom att jämföra resultaten visade de att vävnader med höga gra1‑ och bag1‑signaler nästan alltid smittade alla exponerade möss, medan prover med mRNA‑nivåer under en viss tröskel aldrig orsakade infektion. När dessa tröskelvärden användes som utfallsgränser var överensstämmelsen mellan mRNA‑testet och mus‑bioassayet i paritet med, eller bättre än, traditionella DNA‑baserade metoder. Viktigt är att endast prover som förutspås innehålla tillräckligt många levande parasiter för att vara relevanta skulle behöva gå vidare till musprovning.
Vad detta betyder för säkrare mat och färre djurtester
För icke‑specialisten är huvudbudskapet att forskarna närmar sig ett snabbt, etiskt sätt att avgöra om kött innehåller levande, infektiös T. gondii. Genom att "lyssna" efter kortlivade mRNA‑signaler från två nyckelparasitgener kan gra1–bag1 RT‑qPCR‑analysen fungera som ett prescreen: den markerar vävnader som tydligt hyser farliga nivåer av livskraftiga parasiter och ger trygghet att andra prover ur parasitens synvinkel är i praktiken säkra. Även om mer arbete krävs på naturligt infekterade djur och bearbetade köttprodukter kan detta tillvägagångssätt så småningom minska antalet möss som används i livsmedelssäkerhetstester och hjälpa tillsynsmyndigheter och industrin att bättre bedöma vilka köttprodukter som utgör en verklig risk för toxoplasmos hos konsumenter.
Citering: Largo-de la Torre, A., Velasco-Jiménez, N., Ortega-Mora, L.M. et al. Development and validation of a gra1–bag1 RT-qPCR assay as an alternative to the mouse bioassay for assessing Toxoplasma gondii viability. Sci Rep 16, 14370 (2026). https://doi.org/10.1038/s41598-026-43786-0
Nyckelord: toxoplasmos, födoämnesburna parasiter, PCR‑testning, köttsäkerhet, djurfria tester