Clear Sky Science · pl
Opracowanie i walidacja testu RT-qPCR gra1–bag1 jako alternatywy dla bioasejsu na myszach do oceny żywotności Toxoplasma gondii
Dlaczego ten maleńki pasożyt ma znaczenie przy Twoim stole
Toxoplasma gondii to mikroskopijny pasożyt, który cicho krąży wśród zwierząt hodowlanych, zwierząt domowych i ludzi na całym świecie. Większość infekcji przebiega bezobjawowo, ale u kobiet w ciąży i osób z osłabionym układem odpornościowym może powodować poronienia, uszkodzenia mózgu u noworodków oraz poważne choroby oczu. Ponieważ ludzie często zakażają się przez spożycie niedogotowanego mięsa, naukowcy zajmujący się bezpieczeństwem żywności potrzebują wiarygodnych metod, które pozwolą stwierdzić, czy pasożyt w mięsie jest nadal żywy i niebezpieczny. Do tej pory złotym standardem był test polegający na infekowaniu żywych myszy i oczekiwaniu tygodni na objawy choroby — podejście powolne, kosztowne i coraz bardziej niezgodne ze współczesnymi standardami dobrostanu zwierząt. W tym badaniu przedstawiono nowy test laboratoryjny, który ma na celu przewidywanie żywotności pasożyta bez tak silnego polegania na eksperymentach na zwierzętach.
Od zwierząt hodowlanych do jedzenia na talerzu
Świnie, owce i kozy są kluczowymi ogniwami w łańcuchu przenoszącym T. gondii ze środowiska do ludzkich kuchni. Pasożyt tworzy trwałe cysty w ich mięśniach i mózgach, które mogą pozostać zakaźne, jeśli mięso jest spożywane surowe lub niedogotowane. Tradycyjne testy oparte na DNA dobrze wykrywają materiał genetyczny pasożyta w próbce, ale nie potrafią powiedzieć, czy pasożyt jest żywy czy martwy — podobnie jak znalezienie rozbitego samochodu nie dowodzi, że potrafi on jeszcze jeździć. Z tego powodu regulatorzy i badacze wciąż polegają na bioasejsie na myszach, w którym trawione tkanki zwierząt są wstrzykiwane myszom, a zwierzęta obserwuje się pod kątem objawów infekcji przez ponad miesiąc.
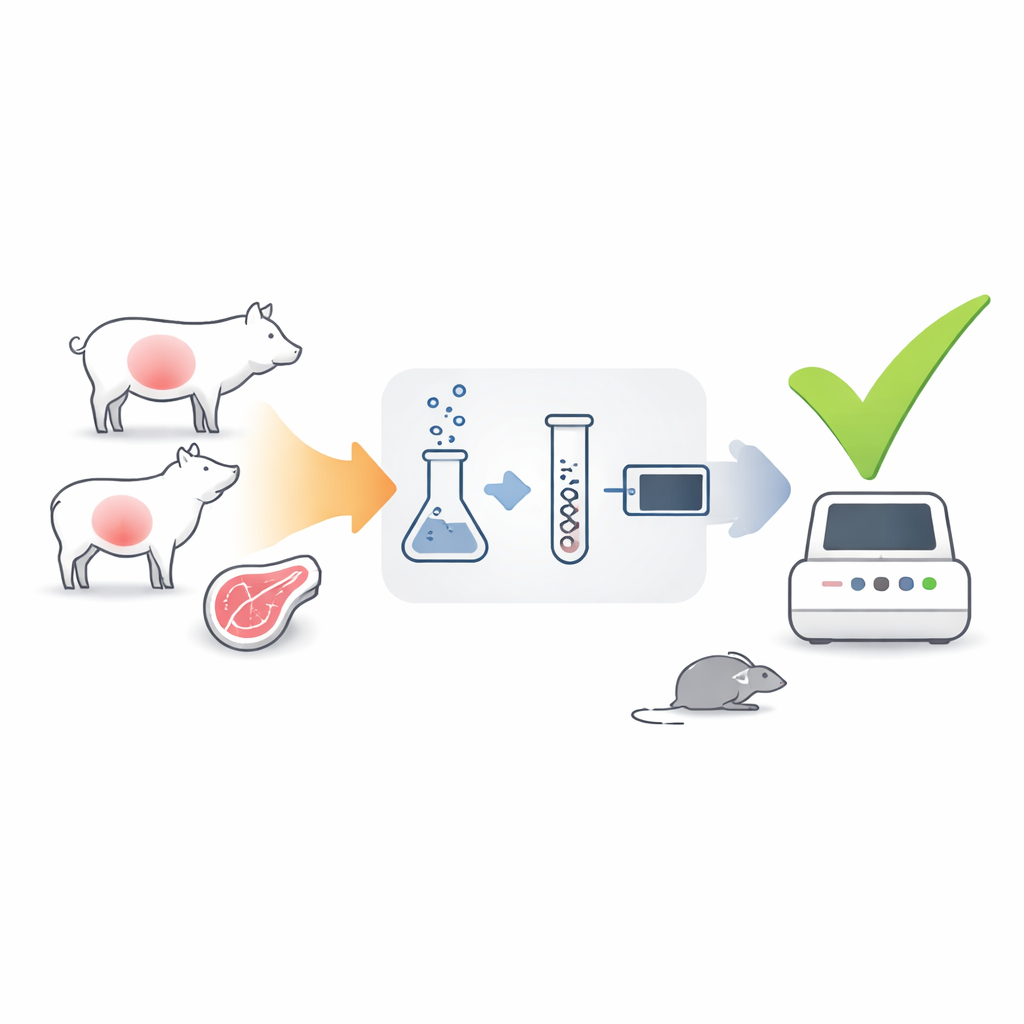
Nowy sposób nasłuchiwania oznak życia
Autorzy opracowali test, który koncentruje się nie na DNA pasożyta, lecz na jego informacyjnym RNA (mRNA) — krótkotrwałych cząsteczkach produkowanych wyłącznie przez aktywne, żywe komórki. Wybrali dwa geny pasożyta jako sygnały: gra1, który jest silnie aktywny, gdy pasożyt szybko się mnoży, oraz bag1, który jest włączany, gdy pasożyt przechodzi w formę przetrwałą w długowiecznych cystach tkankowych. Zastosowali technikę RT-qPCR, w której mRNA pasożyta z próbek tkankowych konwertowano na DNA, a następnie amplifikowano, co pozwoliło policzyć, ile kopii gra1 i bag1 występuje. Ponieważ mRNA szybko ulega rozpadowi po śmierci pasożyta, silne sygnały z tych genów powinny wskazywać na obecność zakaźnych, żywych pasożytów.
Test w akcji w warunkach laboratoryjnych
Aby sprawdzić, czy pomysł działa, zespół najpierw hodował T. gondii w hodowlach komórkowych i poddawał pasożyty zabiegom naśladującym to, co dzieje się podczas trawienia i przetwarzania mięsa. Niektóre próbki były tylko wystawione na działanie enzymów trawiennych, inne były podgrzewane do temperatur zabijających pasożyta, a następnie traktowane enzymami niszczącymi pozostałe RNA. Po zastosowaniu testu RT-qPCR gra1–bag1 żywe lub enzymatycznie traktowane próbki dały silne sygnały mRNA, podczas gdy pasożyty zabite ciepłem prawie nie wykazywały sygnału i nie namnażały się w świeżych hodowlach komórkowych. Test mógł niezawodnie wykryć równowartość zaledwie kilku pasożytów, a pomiary były spójne między powtórzeniami, co sugeruje, że metoda jest zarówno czuła, jak i technicznie odporna.
Jak nowy test wypada względem eksperymentów na żywych myszach
Kluczowe pytanie brzmiało, czy poziomy mRNA w rzeczywistych tkankach zwierzęcych odpowiadają rzeczywistemu ryzyku zakażenia. Badacze użyli przechowywanych próbek mięśni i mózgów od prosiąt i owiec, które zostały eksperymentalnie zakażone znanymi liczbami oocyst T. gondii. Każdą próbkę testowano równolegle czterema metodami: klasycznym bioasejsem na myszach, powszechnie stosowanym qPCR opartym na DNA, dodatkowym PCR nested oraz nowym testem RT-qPCR gra1–bag1. Porównując wyniki, wykazali, że tkanki z wysokimi sygnałami gra1 i bag1 niemal zawsze zakażały wszystkie eksponowane myszy, podczas gdy próbki z poziomami mRNA poniżej określonego progu nigdy nie powodowały zakażenia. Po zastosowaniu tych progów jako punktów odcięcia zgodność między testem mRNA a bioasejsem na myszach była porównywalna lub lepsza niż w przypadku tradycyjnych metod opartych na DNA. Co ważne, tylko próbki przewidywane jako zawierające wystarczającą liczbę żywotnych pasożytów wymagałyby dalszych testów na myszach.
Co to oznacza dla bezpieczniejszej żywności i mniejszej liczby testów na zwierzętach
Dla osoby niebędącej specjalistą kluczowy wniosek jest taki, że naukowcy zbliżają się do szybkiej, etycznej metody decydowania, czy mięso zawiera żywe, zakaźne T. gondii. „Nasłuchując” krótkotrwałych sygnałów mRNA z dwóch kluczowych genów pasożyta, test RT-qPCR gra1–bag1 może pełnić funkcję preselekcji: oznacza tkanki, które wyraźnie zawierają niebezpieczny poziom żywotnych pasożytów, i daje pewność, że inne próbki są z punktu widzenia pasożyta skutecznie bezpieczne. Chociaż potrzebne są dalsze badania na naturalnie zakażonych zwierzętach i w przetworzonych produktach mięsnych, podejście to w przyszłości może zmniejszyć liczbę myszy używanych w badaniach bezpieczeństwa żywności i pomóc regulatorom oraz przemysłowi lepiej ocenić, które mięsa stanowią realne ryzyko toxoplazmozy dla konsumentów.
Cytowanie: Largo-de la Torre, A., Velasco-Jiménez, N., Ortega-Mora, L.M. et al. Development and validation of a gra1–bag1 RT-qPCR assay as an alternative to the mouse bioassay for assessing Toxoplasma gondii viability. Sci Rep 16, 14370 (2026). https://doi.org/10.1038/s41598-026-43786-0
Słowa kluczowe: toxoplazmoza, pasożyty przenoszone przez żywność, testy PCR, bezpieczeństwo mięsa, testy bez użycia zwierząt