Clear Sky Science · pt
Desenvolvimento e validação de um ensaio RT-qPCR gra1–bag1 como alternativa ao bioensaio em camundongos para avaliar a viabilidade de Toxoplasma gondii
Por que esse parasita minúsculo importa para a sua mesa
Toxoplasma gondii é um parasita microscópico que circula discretamente entre animais de fazenda, animais de estimação e pessoas em todo o mundo. A maioria das infecções passa despercebida, mas em gestantes e em pessoas com o sistema imunológico comprometido pode provocar aborto, lesões cerebrais em recém-nascidos e doença ocular grave. Como os humanos frequentemente são infectados ao comer carne malpassada, cientistas de segurança alimentar precisam de métodos confiáveis para determinar se o parasita presente na carne ainda está vivo e representa perigo. Até agora, o padrão-ouro envolvia infectar camundongos vivos e aguardar semanas por sinais de doença — uma abordagem lenta, cara e cada vez mais incompatível com os padrões modernos de bem-estar animal. Este estudo apresenta um novo teste laboratorial que visa predizer a viabilidade do parasita sem depender tanto de experimentos com animais.
Dos animais de criação ao prato
Porcos, ovelhas e cabras são elos-chave na cadeia que leva T. gondii do ambiente às cozinhas humanas. O parasita forma cistos resistentes nos músculos e no cérebro desses animais, que podem permanecer infectantes se a carne for consumida crua ou malcozida. Testes tradicionais baseados em DNA detectam bem a presença de material genético do parasita em uma amostra, mas não conseguem dizer se o parasita está vivo ou morto — como encontrar um carro batido não prova que ele ainda dirige. Por essa razão, reguladores e pesquisadores continuam a depender do bioensaio em camundongo, no qual tecido digerido de animais de criação é injetado em camundongos e os animais são monitorados por sinais de infecção ao longo de mais de um mês.
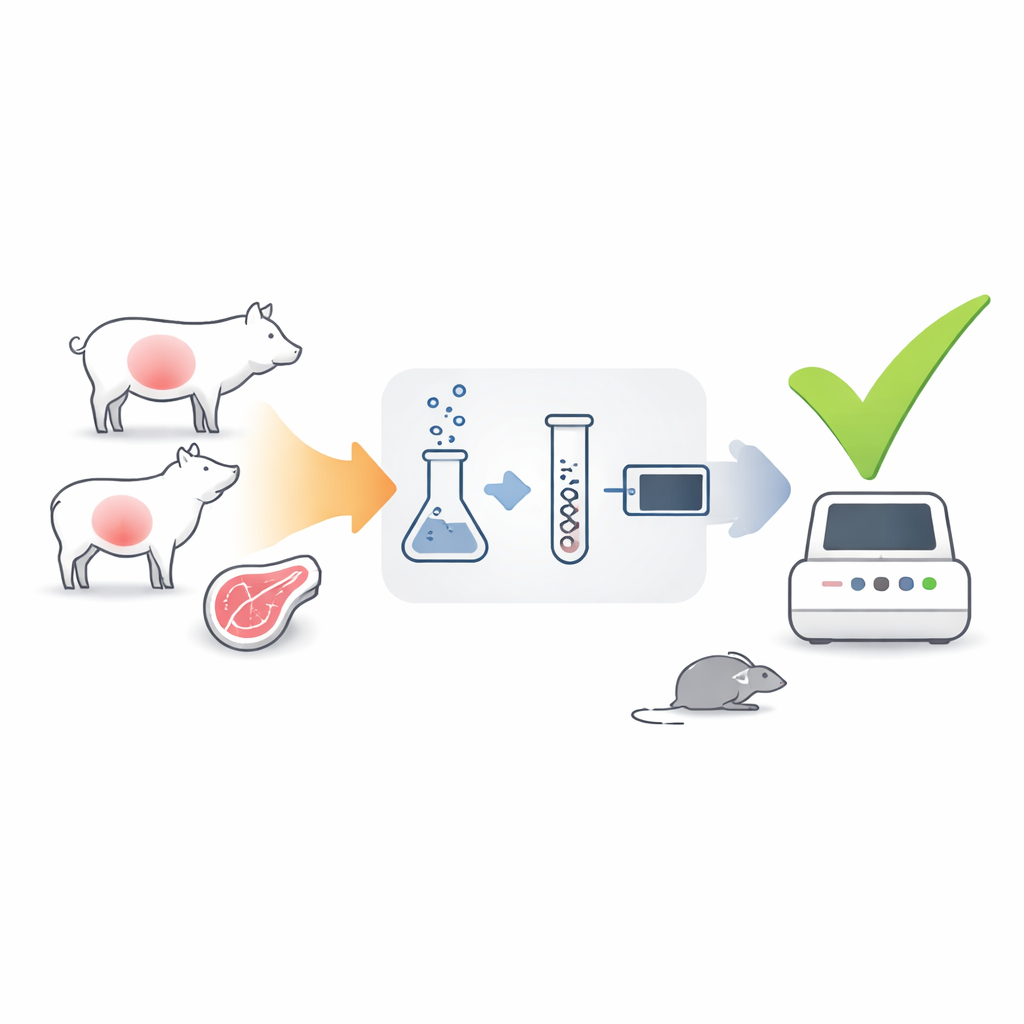
Uma nova maneira de escutar sinais de vida
Os autores desenvolveram um teste que se concentra não no DNA do parasita, mas em seu RNA mensageiro (mRNA) — moléculas de curta duração produzidas apenas por células ativas e vivas. Eles escolheram dois genes do parasita como sinais: gra1, fortemente ativo quando o parasita multiplica-se rapidamente, e bag1, ativado quando ele entra em cistos de longa duração nos tecidos. Usando uma técnica chamada RT-qPCR, converteram o mRNA do parasita presente em amostras de tecido em DNA e o amplificaram, permitindo contar quantas cópias de gra1 e bag1 estavam presentes. Como o mRNA se degrada rapidamente após a morte do parasita, sinais fortes desses genes devem indicar que parasitas infectantes ainda estão presentes.
Testando o ensaio em laboratório
Para avaliar se a ideia funcionava, a equipe primeiro cultivou T. gondii em cultura celular e submeteu os parasitas a tratamentos que imitam o que ocorre durante a digestão e o processamento da carne. Algumas amostras foram apenas expostas a enzimas digestivas, enquanto outras foram aquecidas a temperaturas letais para o parasita e depois tratadas com enzimas que destroem RNA residual. Ao aplicar o ensaio RT-qPCR gra1–bag1, parasitas vivos ou apenas expostos a enzimas mostraram sinais fortes de mRNA, enquanto parasitas mortos pelo calor produziram quase nenhum sinal e não cresceram em culturas celulares frescas. O teste conseguiu detectar de forma confiável o equivalente a apenas alguns parasitas, e as medidas foram consistentes de uma corrida para outra, sugerindo que o ensaio é sensível e tecnicamente robusto.
Como o novo teste se compara aos experimentos com camundongos vivos
A questão crucial era saber se os níveis de mRNA em tecidos animais reais corresponderiam ao risco efetivo de infecção. Os pesquisadores usaram amostras armazenadas de músculo e cérebro de leitões e cordeiros que haviam sido infectados experimentalmente com números conhecidos de oocistos de T. gondii. Cada amostra foi testada em paralelo por quatro métodos: o clássico bioensaio em camundongo, uma qPCR baseada em DNA amplamente utilizada, uma PCR aninhada adicional e a nova RT-qPCR gra1–bag1. Ao comparar os resultados, mostraram que tecidos com sinais altos de gra1 e bag1 quase sempre infectaram todos os camundongos expostos, enquanto amostras com níveis de mRNA abaixo de determinado limiar nunca causaram infecção. Ao usar esses limiares como pontos de corte, a concordância entre o teste de mRNA e o bioensaio em camundongo ficou equivalente ou superior à dos métodos tradicionais baseados em DNA. Importante: somente amostras previstas como contendo parasitas viáveis em quantidade suficiente para ser relevante precisariam seguir para o teste em camundongos.
O que isso significa para alimentos mais seguros e menos testes em animais
Para o público em geral, a conclusão é que os cientistas estão mais próximos de um método rápido e ético para decidir se a carne contém T. gondii vivo e infectante. Ao “escutar” sinais de mRNA de curta vida de dois genes-chave do parasita, o ensaio RT-qPCR gra1–bag1 pode funcionar como pré-triagem: ele identifica tecidos que claramente abrigam níveis perigosos de parasitas viáveis e dá segurança de que outros estão efetivamente seguros do ponto de vista do parasita. Embora sejam necessários mais estudos em animais naturalmente infectados e em produtos cárneos processados, essa abordagem poderia reduzir eventualmente o número de camundongos usados em testes de segurança alimentar e ajudar reguladores e a indústria a avaliar melhor quais carnes representam um risco real de toxoplasmose para os consumidores.
Citação: Largo-de la Torre, A., Velasco-Jiménez, N., Ortega-Mora, L.M. et al. Development and validation of a gra1–bag1 RT-qPCR assay as an alternative to the mouse bioassay for assessing Toxoplasma gondii viability. Sci Rep 16, 14370 (2026). https://doi.org/10.1038/s41598-026-43786-0
Palavras-chave: toxoplasmose, parasitas transmitidos por alimentos, testes por PCR, segurança da carne, ensaios sem animais