Clear Sky Science · es
Desarrollo y validación de un ensayo RT-qPCR gra1–bag1 como alternativa al bioensayo en ratón para evaluar la viabilidad de Toxoplasma gondii
Por qué este diminuto parásito importa en tu mesa
Toxoplasma gondii es un parásito microscópico que circula de forma silenciosa entre animales de granja, mascotas y personas en todo el mundo. La mayoría de las infecciones pasan desapercibidas, pero en mujeres embarazadas y en personas con el sistema inmunitario debilitado puede provocar aborto, daño cerebral en recién nacidos y enfermedades oculares graves. Dado que los humanos suelen infectarse al comer carne poco hecha, los científicos de seguridad alimentaria necesitan métodos fiables para determinar si el parásito presente en la carne sigue vivo y es peligroso. Hasta ahora, la prueba de referencia consistía en infectar ratones vivos y esperar semanas a que apareciesen signos de enfermedad: un enfoque lento, costoso y cada vez más incompatibilizado con las normas modernas de bienestar animal. Este estudio presenta una nueva prueba de laboratorio que pretende predecir la viabilidad del parásito sin depender tanto de experimentos con animales.
De los animales de granja a la comida en el plato
Los cerdos, las ovejas y las cabras son eslabones clave en la cadena que lleva a T. gondii del entorno a las cocinas humanas. El parásito forma quistes resistentes en sus músculos y cerebros, que pueden seguir siendo infecciosos si la carne se consume cruda o poco hecha. Las pruebas tradicionales basadas en ADN son buenas para detectar si hay material genético del parásito en una muestra, pero no pueden decir si ese parásito está vivo o muerto —como encontrar un coche destrozado no prueba que todavía pueda conducir. Por esa razón, reguladores e investigadores han seguido dependiendo del bioensayo en ratón, en el que el tejido digerido de animales de granja se inyecta en ratones y se monitoriza a los animales durante más de un mes en busca de signos de infección.
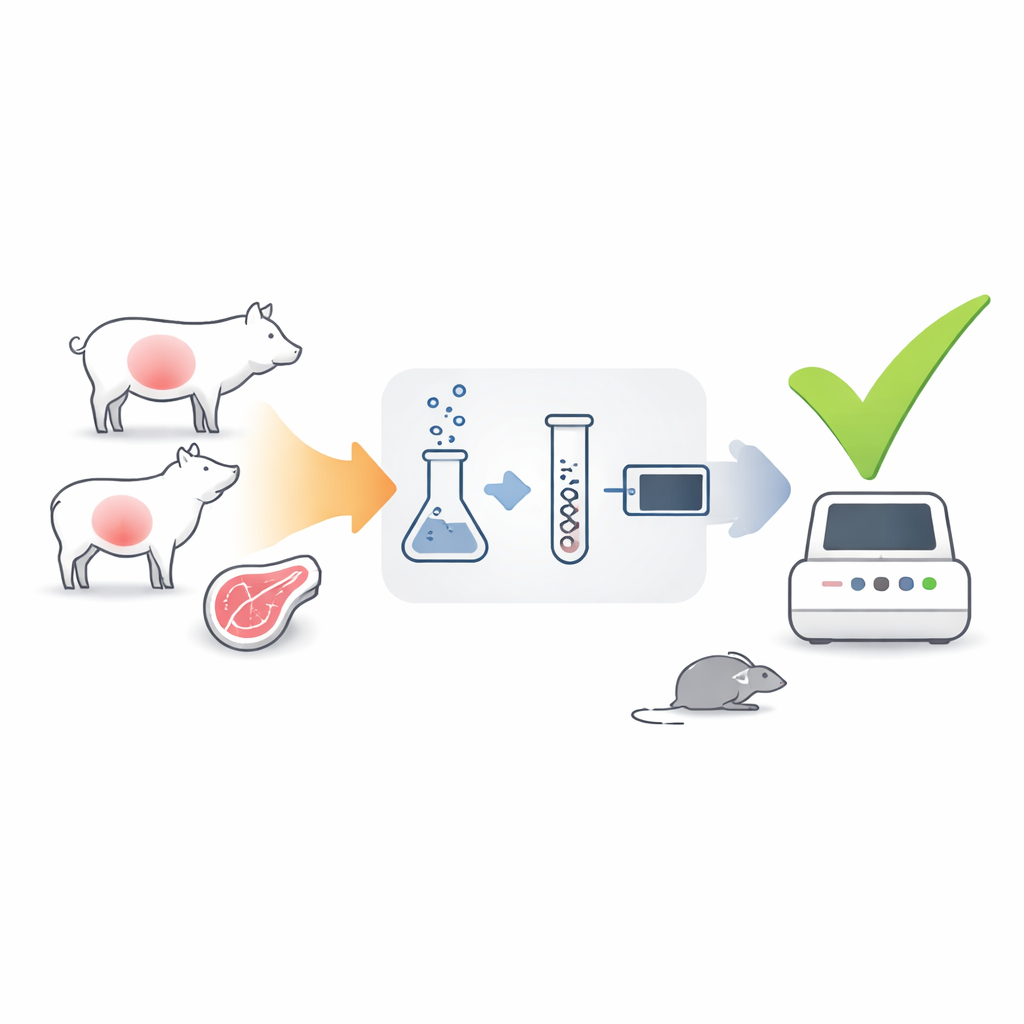
Una nueva forma de escuchar señales de vida
Los autores desarrollaron una prueba que se centra no en el ADN del parásito, sino en su ARN mensajero (ARNm): moléculas de vida corta que solo producen las células activas y vivas. Eligieron dos genes del parásito como señales: gra1, que está fuertemente activo cuando el parásito se multiplica rápidamente, y bag1, que se activa cuando se instala en quistes tisulares de larga duración. Usando una técnica llamada RT-qPCR, convirtieron el ARNm parasitario de muestras de tejido en ADN y luego lo amplificaron, lo que les permitió contar cuántas copias de gra1 y bag1 estaban presentes. Dado que el ARNm se degrada rápidamente una vez que el parásito muere, señales intensas de estos genes deberían indicar que aún hay parásitos infecciosos.
Poner la prueba a prueba en el laboratorio
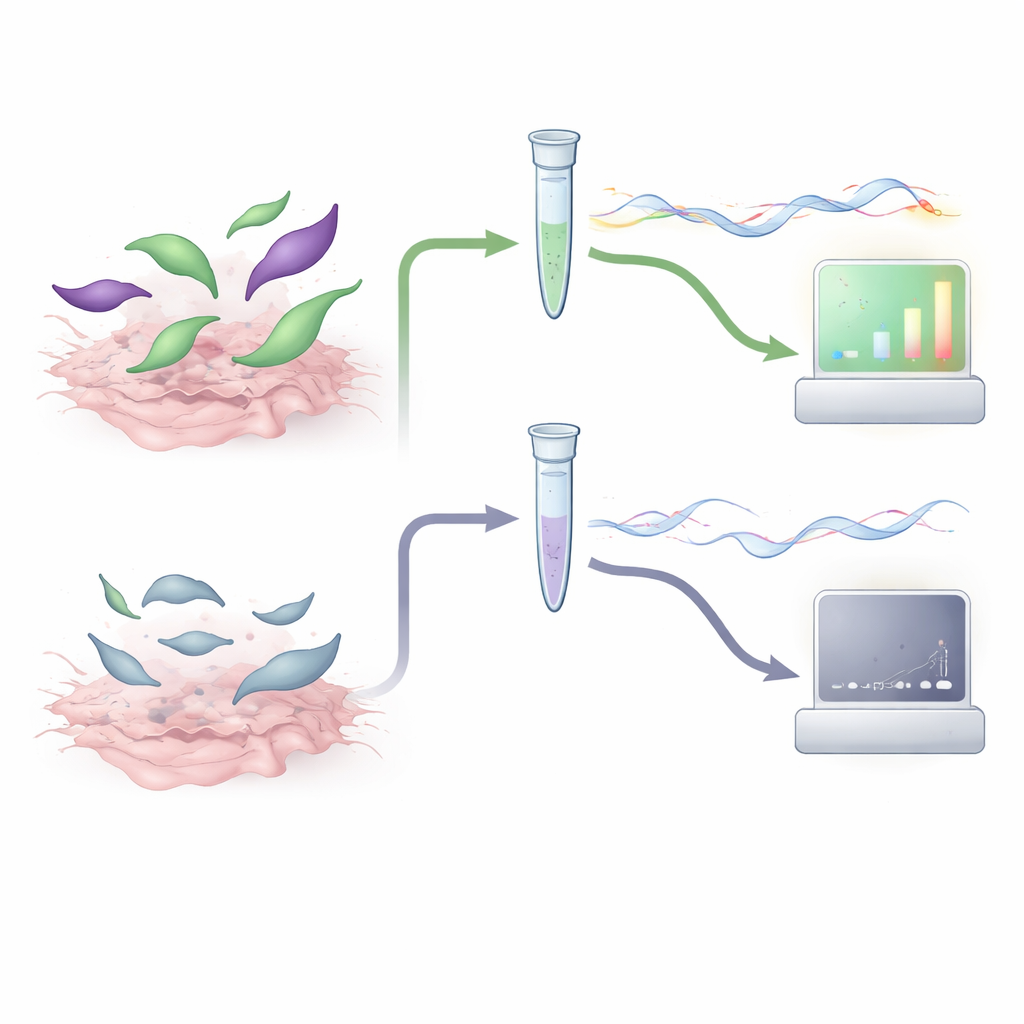
Para comprobar si la idea funcionaba, el equipo cultivó primero T. gondii en cultivo celular y sometió a los parásitos a tratamientos que imitan lo que ocurre durante la digestión y el procesado de la carne. Algunas muestras se expusieron simplemente a enzimas digestivas, mientras que otras se calentaron a niveles que matan al parásito y después se trataron con enzimas que destruyen el ARN residual. Cuando aplicaron su ensayo RT-qPCR gra1–bag1, los parásitos vivos o tratados solo con enzimas dieron señales intensas de ARNm, mientras que los parásitos muertos por calor produjeron casi ninguna señal y no crecieron en cultivos celulares frescos. La prueba pudo detectar de forma fiable el equivalente a apenas unas pocas unidades del parásito, y las mediciones fueron consistentes entre corridas, lo que sugiere que el ensayo es tanto sensible como técnicamente robusto.
Cómo se compara la nueva prueba con los experimentos en ratones vivos
La cuestión crucial era si los niveles de ARNm en tejidos animales reales se correspondían con el riesgo real de infección. Los investigadores usaron muestras almacenadas de músculo y cerebro de lechones y ovejas que habían sido infectados experimentalmente con números conocidos de ooquistes de T. gondii. Cada muestra se analizó en paralelo por cuatro métodos: el clásico bioensayo en ratón, una qPCR ampliamente usada basada en ADN, una PCR anidada adicional y la nueva RT-qPCR gra1–bag1. Al comparar los resultados, demostraron que los tejidos con señales altas de gra1 y bag1 casi siempre infectaban a todos los ratones expuestos, mientras que las muestras con niveles de ARNm por debajo de cierto umbral nunca causaron infección. Al usar estos umbrales como puntos de corte, la concordancia entre la prueba de ARNm y el bioensayo en ratón fue comparable o mejor que la de los métodos tradicionales basados en ADN. Importante: solo las muestras que se predecía contenían suficientes parásitos viables como para ser relevantes necesitarían pasar posteriormente a la prueba en ratones.
Qué significa esto para una comida más segura y menos ensayos con animales
Para un público no especializado, la conclusión es que los científicos están más cerca de disponer de una forma rápida y ética de decidir si la carne contiene T. gondii vivo e infeccioso. Al “escuchar” señales de ARNm de vida corta de dos genes parasitarios clave, el ensayo RT-qPCR gra1–bag1 puede actuar como una preselección: identifica los tejidos que claramente albergan niveles peligrosos de parásitos viables y confirma que otros están, desde el punto de vista del parásito, efectivamente seguros. Aunque se necesita más trabajo en animales infectados de forma natural y en productos cárnicos procesados, este enfoque podría eventualmente reducir el número de ratones usados en las pruebas de seguridad alimentaria y ayudar a reguladores e industria a evaluar mejor qué carnes representan un riesgo real de toxoplasmosis para los consumidores.
Cita: Largo-de la Torre, A., Velasco-Jiménez, N., Ortega-Mora, L.M. et al. Development and validation of a gra1–bag1 RT-qPCR assay as an alternative to the mouse bioassay for assessing Toxoplasma gondii viability. Sci Rep 16, 14370 (2026). https://doi.org/10.1038/s41598-026-43786-0
Palabras clave: toxoplasmosis, parásitos transmitidos por alimentos, pruebas PCR, seguridad de la carne, ensayos sin animales