Clear Sky Science · ar
تطوير والتحقق من اختبار RT-qPCR لجينات gra1–bag1 كبديل لاختبار الأحياء في الفئران لتقييم حيوية Toxoplasma gondii
لماذا هذا الطفيلي الصغير مهم على مائدتك
Toxoplasma gondii هو طفيلي مجهري يتنقل بهدوء عبر الحيوانات الأليفة والمزارع والبشر في جميع أنحاء العالم. تمر معظم الإصابات دون أن يلاحظها أحد، لكن لدى الحوامل والأشخاص ذوي المناعة الضعيفة يمكن أن يتسبب في إجهاض، وإصابة دماغ المواليد الجدد، وأمراض عينية خطيرة. ونظراً لأن العدوى البشرية غالباً ما تحدث بتناول لحوم غير مطهية جيداً، يحتاج علماء سلامة الغذاء إلى طرق موثوقة لمعرفة ما إذا كان الطفيلي في اللحوم لا يزال حياً وخطيراً. حتى الآن، كان الاختبار المعياري الذهبي يتطلب إصابة فئران حية والانتظار أسابيع لعلامات المرض—وهي مقاربة بطيئة ومكلفة وتتعارض متزايداً مع معايير رفاهية الحيوان الحديثة. تعرض هذه الدراسة اختباراً مخبرياً جديداً يهدف إلى التنبؤ بحيوية الطفيلي دون الاعتماد الكبير على التجارب الحيوانية.
من حيوانات المزرعة إلى الطعام على الطبق
الخنازير والأغنام والماعز تشكل حلقة رئيسية في السلسلة التي تنقل T. gondii من البيئة إلى المطابخ البشرية. يشكل الطفيلي أكياساً متينة في عضلاتها وأدمغتها، والتي قد تظل معدية إذا أُكلت اللحوم نيئة أو غير مطهوة جيداً. الاختبارات التقليدية القائمة على الحمض النووي جيدة في اكتشاف وجود المادة الجينية للطفيلي في عينة، لكنها لا تستطيع أن تخبر ما إذا كان الطفيلي حيّاً أم ميتاً—على غرار العثور على سيارة محطمة لا يثبت أنها لا تزال قادرة على القيادة. لهذا السبب، استمر المنظمون والباحثون في الاعتماد على اختبار الأحياء في الفئران، حيث تُحقن أنسجة مهضومة من الماشية في فئران وتُراقب الحيوانات لعلامات العدوى لأكثر من شهر.
طريقة جديدة للاستماع إلى إشارات الحياة
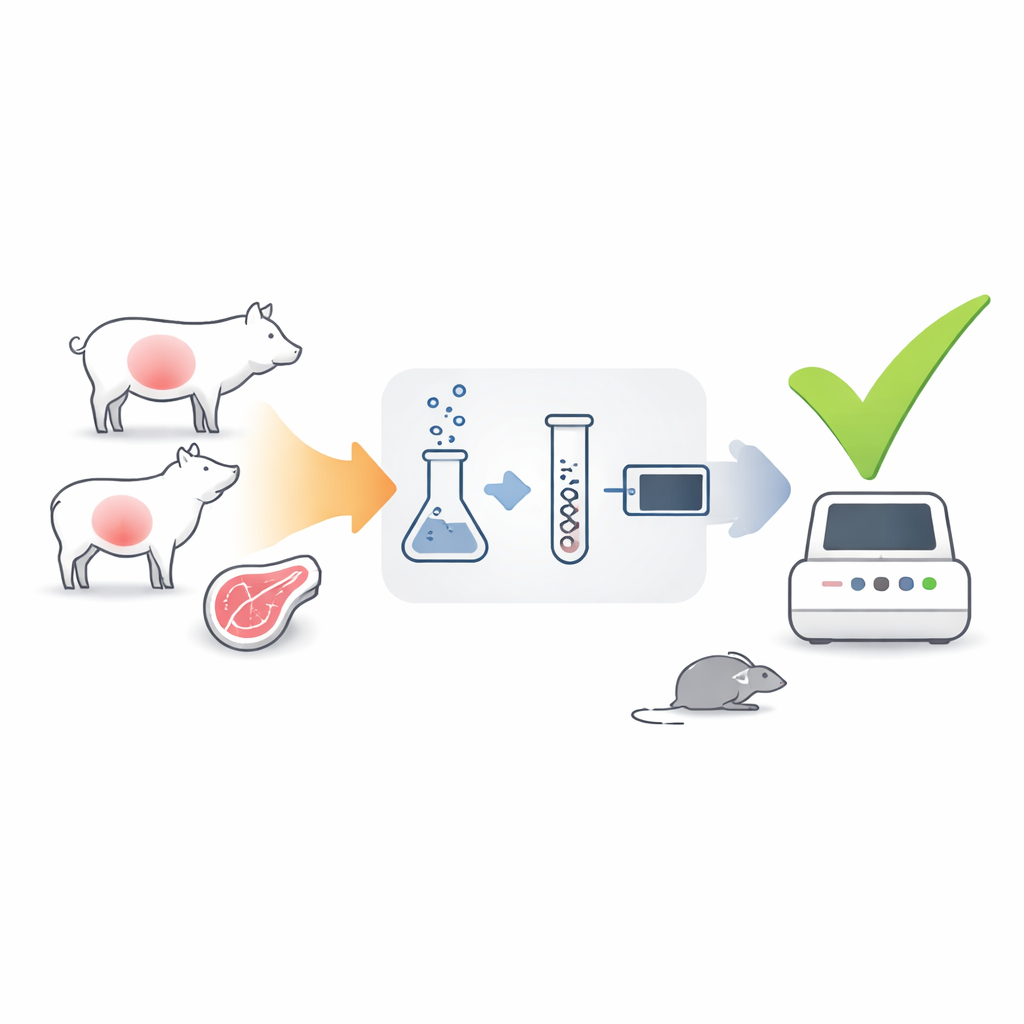
طور المؤلفون اختباراً يركز ليس على حمض الطفيلي النووي (DNA)، بل على الرنا الرسول (mRNA)—جزيئات قصيرة الأمد تُنتَج فقط بواسطة الخلايا النشطة والحية. اختاروا جينات طفيلية اثنتين كإشارات: gra1، النشطة بقوة عندما يتكاثر الطفيلي بسرعة، وbag1، التي تُشغّل عندما ينكمش الطفيلي في أكياس نسيجية طويلة العمر. باستخدام تقنية تُدعى RT-qPCR، حوّلوا رنا الرسول من عينات الأنسجة إلى DNA ثم ضخموا المادة، مما أتاح لهم عدّ نسخ gra1 وbag1 الموجودة. لأن الرنا الرسول يتحلل بسرعة عند موت الطفيلي، فالإشارات القوية من هاتين الجينتين يجب أن تشير إلى أن الطفيليات المعدية لا تزال موجودة.
اختبار المنهج في المختبر
لمعرفة ما إذا كانت الفكرة تعمل، نما الفريق أولاً T. gondii في زراعة خلوية وعرض الطفيليات لمعالجات تحاكي ما يحدث أثناء هضم ومعالجة اللحوم. بعض العينات تعرضت فقط لإنزيمات هاضمة، بينما عولجت عينات أخرى بالحرارة إلى مستويات تقتل الطفيلي ثم عوملت بإنزيمات تدمر الرنا المتبقّي. عند تطبيق اختبار gra1–bag1 RT-qPCR، أعطت الطفيليات الحية أو المعالجة بالإنزيمات إشارات قوية للرنا الرسول، بينما أنتجت الطفيليات الميتة بالحرارة إشارات ضئيلة تقريباً وفشلت في النمو في زراعات خلوية طازجة. استطاع الاختبار اكتشاف ما يعادل بضعة طفيليات فقط بشكل موثوق، وكانت القياسات متسقة من تشغيل إلى آخر، مما يشير إلى أن المقياس حساس ومتجانس فنياً.
كيف يقارن الاختبار الجديد بتجارب الفئران الحية
السؤال الحاسم كان ما إذا كانت مستويات الرنا الرسول في أنسجة حيوانية حقيقية تطابق خطر العدوى الفعلي. استخدم الباحثون عينات عضلية ودماغية مخزنة من خنازير صغيرة وأغنام أُصيبت تجريبياً بعدد معروف من الأكياس البيضية (oocysts) لـT. gondii. اختُبرت كل عينة بالتوازي بأربع طرق: اختبار الأحياء الكلاسيكي في الفئران، وqPCR القائم على الحمض النووي المستخدم على نطاق واسع، وPCR متداخل إضافي، واختبار gra1–bag1 RT-qPCR الجديد. بمقارنة النتائج، أظهروا أن الأنسجة ذات إشارات gra1 وbag1 العالية أصابت تقريباً دائماً كل الفئران المعرضة، بينما العينات ذات مستويات الرنا الرسول تحت عتبة معينة لم تسبب عدوى أبداً. عند استخدام هذه العتبات كفواصل، كان التوافق بين اختبار الرنا الرسول واختبار الأحياء في الفئران مماثلاً أو أفضل من الأساليب التقليدية القائمة على الحمض النووي. ومن المهم أن العينات التي يُتوقع أن تحتوي على طفيليات حية بكمية كافية لتكون مهمة فقط هي التي ستحتاج إلى الانتقال لاختبار الفئران.
ماذا يعني هذا لسلامة الغذاء وتقليل تجارب الحيوانات
بالنسبة لغير المتخصص، الخلاصة هي أن العلماء يقتربون من طريقة سريعة وأخلاقية لتقرير ما إذا كانت اللحوم تحتوي على T. gondii حي ومعدٍ. من خلال "الاستماع" إلى إشارات الرنا الرسول قصيرة الأمد من جينين طفيليين رئيسيين، يمكن لاختبار gra1–bag1 RT-qPCR أن يعمل كفحص قبلي: يحدد الأنسجة التي تحتوي بوضوح على مستويات خطرة من الطفيليات الحية، ويطمئن إلى أن عينات أخرى آمنة من منظور الطفيلي. ومع أن هناك حاجة لمزيد من العمل على الحيوانات المصابة طبيعياً ومنتجات اللحوم المعالجة، قد تقلل هذه المقاربة في نهاية المطاف من عدد الفئران المستخدمة في اختبار سلامة الغذاء وتساعد الجهات المنظمة والصناعة على تقييم أي اللحوم تشكل خطراً حقيقياً بداء المقوسات للمستهلكين.
الاستشهاد: Largo-de la Torre, A., Velasco-Jiménez, N., Ortega-Mora, L.M. et al. Development and validation of a gra1–bag1 RT-qPCR assay as an alternative to the mouse bioassay for assessing Toxoplasma gondii viability. Sci Rep 16, 14370 (2026). https://doi.org/10.1038/s41598-026-43786-0
الكلمات المفتاحية: داء المقوسات, طفيليات منقولة عن طريق الغذاء, اختبارات PCR, سلامة اللحوم, اختبارات خالية من الحيوانات