Clear Sky Science · zh
与4-1BB相比,CD28共刺激结构域在卵巢癌小鼠模型中提高了CER T细胞疗法的疗效
这项研究对患者的重要性
卵巢癌常在腹腔广泛转移后才被发现,许多晚期患者即便经过手术和化疗仍然死亡。利用机体自身免疫细胞对抗癌症的免疫疗法已经改变了一些血液系统肿瘤的治疗,但在卵巢癌等实质性肿瘤中效果有限。本研究探索了一种针对常见于卵巢癌细胞受体的T细胞新改造方法,并提出了一个实际设计问题:哪种内在的“发动机”能让这些T细胞更有效地杀死癌细胞?
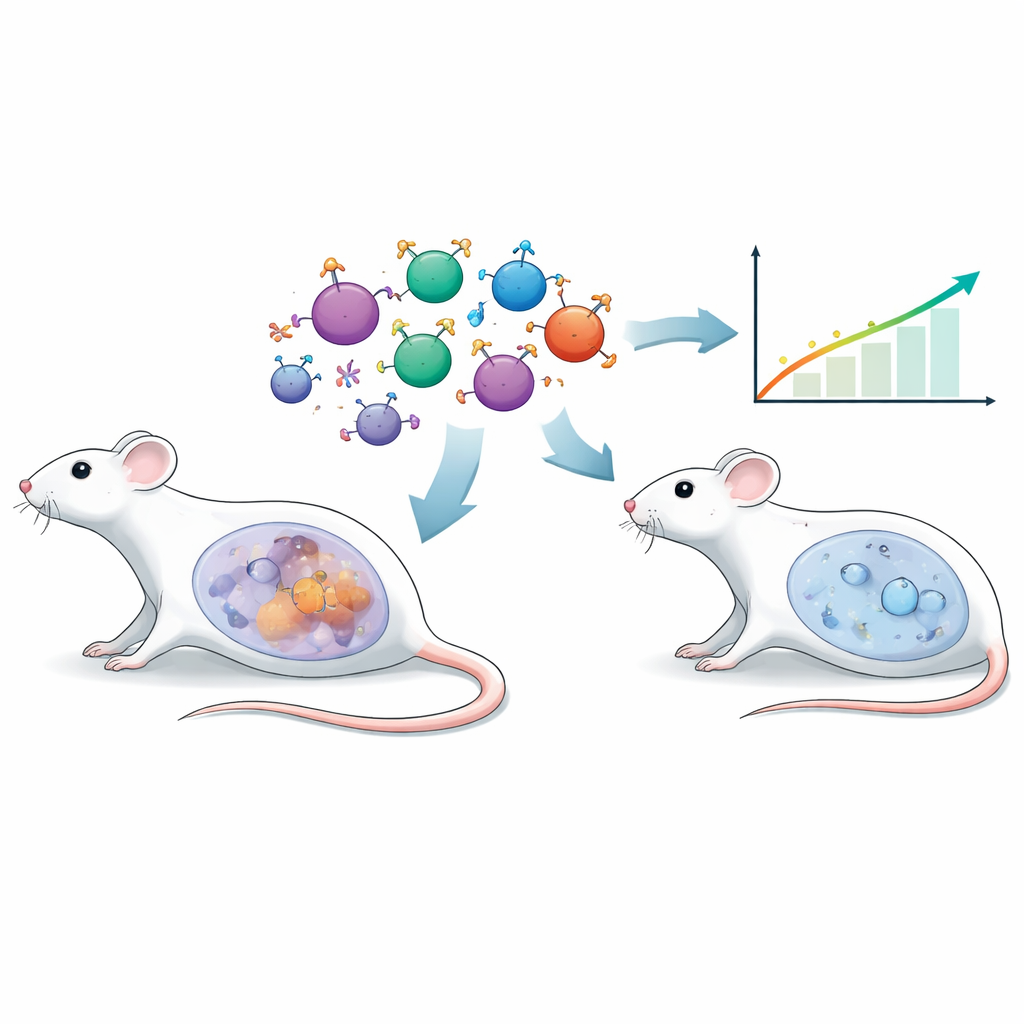
引导免疫细胞的新方法
传统的工程化T细胞疗法通常依赖人工抗体片段识别肿瘤。此处研究者采用了不同策略,称为嵌合内分泌受体(CER)。这些T细胞表面不是装抗体,而是携带促卵泡刺激素(FSH)——一种以生殖功能著称的天然激素。许多卵巢癌细胞在其表面表达相配的促卵泡刺激素受体(FSHR)。通过为小鼠T细胞装上基于FSH的受体,团队将其定向至FSHR阳性的卵巢肿瘤细胞,旨在实现精确靶向并尽量减少对正常组织的损伤。
构建更具挑战性的卵巢癌模型
为在更真实的环境中测试该方法,科学家使用了名为ID8的小鼠卵巢癌系,并构建了过表达FSHR的版本(ID8‑FSHR)。当将其植入小鼠腹腔时,这些富含FSHR的肿瘤比原始细胞系生长更具侵袭性。动物因腹水而体重更快增加,影像学显示更高的肿瘤信号,生存期更短。肿瘤中的基因表达转向促进癌症的程序,腹腔液中的蛋白质和代谢物也发生广泛变化,提示更加抑制免疫的敌对环境。重要的是,来自八位上皮性卵巢癌女性患者的腹水细胞也显示FSHR表达,支持该靶点的临床相关性。
比较T细胞内的两种“发动机”
每个工程化受体内部都包含一个信号模块,决定T细胞响应的强度和持续时间。团队在相同的FSH‑CER T细胞框架下比较了两种常用的共刺激设计——CD28ζ和4‑1BBζ,并设置了一个最小控制版本。在体外培养中,携带CD28ζ模块的FSH‑CER T细胞(称为FSH‑28ζ)持续优于4‑1BBζ的版本。它们更有效地杀伤FSHR阳性肿瘤细胞、增殖更强、向与长效免疫相关的记忆样状态转变,并释放更多炎性介质如干扰素‑γ和肿瘤坏死因子。信号强度的分子读出和活化标志位也证实,基于CD28的设计在早期提供了更强的冲击力。
在活体小鼠中测试疗法
当携带ID8‑FSHR肿瘤的小鼠接受一次FSH‑CER T细胞输注时,装备CD28的细胞再次表现突出。接受FSH‑28ζ T细胞治疗的动物肿瘤信号更低、腹水更少、存活显著长于接受4‑1BBζ或无活性对照细胞的组。在进行详细免疫取样时,CD28处理组小鼠的腹腔冲洗液中几乎检测不到肿瘤细胞。然而,研究也暴露出一个缺点:在输注后一周内,大多数肿瘤区域的工程化T细胞出现多种“耗竭”标志物,且CER T细胞总体数量较低,表明尽管它们起初活性更强,但恶劣的肿瘤环境仍然使其功能衰竭。
当肿瘤腹水反击时
研究者进一步探究为何FSHR阳性肿瘤的腹水具有强烈的抑制性。当他们将这些小鼠的腹水加入体外培养时,显著降低了FSH‑CER T细胞的杀伤能力、增殖和信号传导,4‑1BBζ版本受抑制尤甚,而针对不同靶点的常规CD19 CAR T细胞影响甚微。细致的蛋白质分析未发现肿瘤细胞将FSHR剪切释放到液体中以阻断受体。相反,在不能产生抗体的免疫缺陷小鼠的实验指向了另一类元凶:由动物自身B细胞或T细胞对FSHR过表达肿瘤产生的因子,可能包括抗‑FSHR抗体,这些因子特异性干扰了这种基于激素的靶向策略。
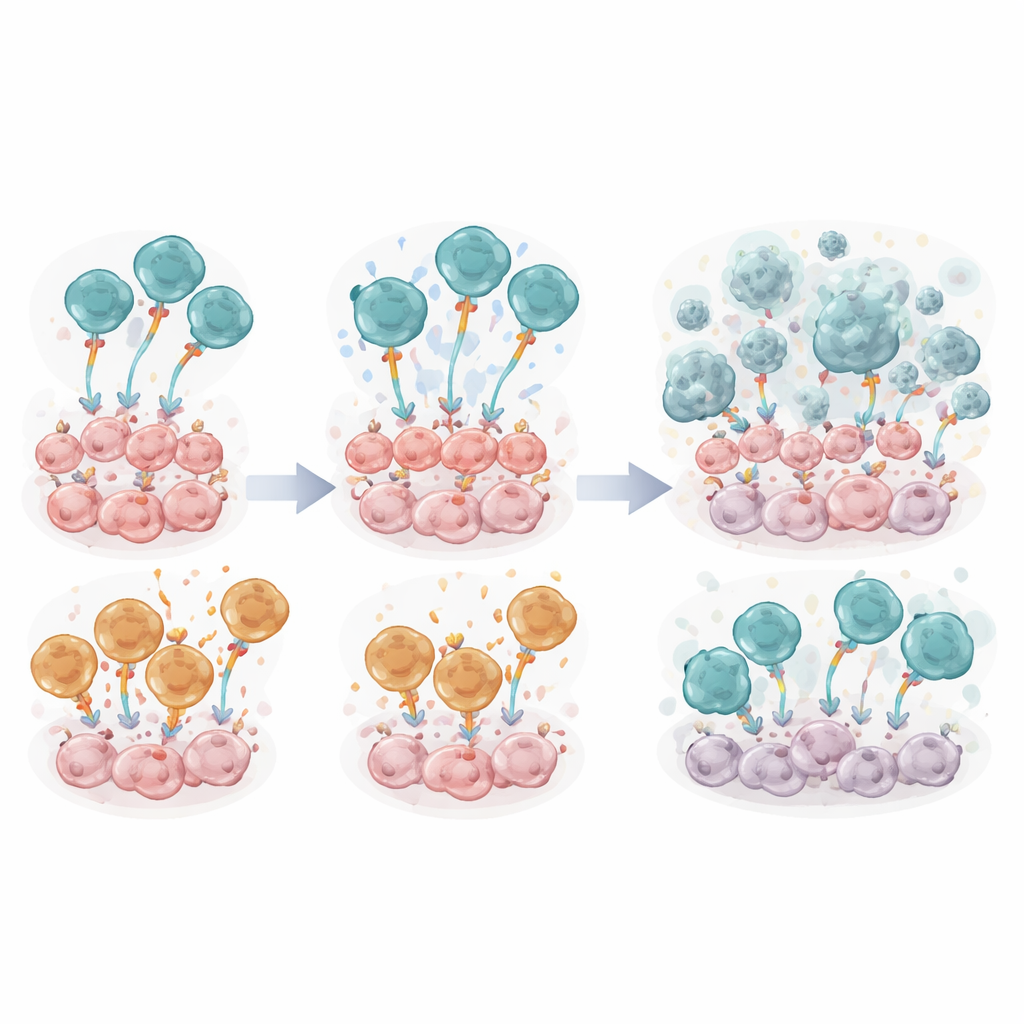
对未来治疗的意义
对非专业读者来说,主要结论是:并非所有工程化T细胞都一样,内部线路的细节很重要。在这个卵巢癌小鼠模型中,携带FSH受体且采用CD28ζ信号核心的T细胞比采用4‑1BBζ核心的细胞更强劲地杀伤肿瘤并更能延长生存。同时,这项工作也揭示了卵巢肿瘤周围的液体环境如何削弱这些免疫细胞的力量,可能通过针对它们所识别受体的抗体来实现。该研究支持基于CD28的FSH‑CER T细胞作为卵巢癌免疫疗法的有前景蓝图,但也强调任何临床策略都需将此类细胞与防止或逆转免疫耗竭和对抗肿瘤抑制性环境的措施配套使用。
引用: Beatty, N.J., Ma, M., Goala, P. et al. CD28 co-stimulatory domain enhances efficacy of CER T cell therapy compared to 4-1BB in an ovarian cancer mouse model. Sci Rep 16, 13068 (2026). https://doi.org/10.1038/s41598-026-43225-0
关键词: 卵巢癌, T细胞疗法, 免疫疗法, 促卵泡刺激素受体, 肿瘤微环境