Clear Sky Science · he
תחום הקושרים המשלים CD28 משפר את היעילות של טיפול תאי CER בהשוואה ל‑4‑1BB במודל עכבר לסרטן השחלה
מדוע מחקר זה חשוב למטופלות
סרטן השחלה מאובחן לעתים רק לאחר שכבר התפשט בשקט ברחם הבטן, ורבות מהנשים עם מחלה מתקדמת עדיין נפטרות למרות ניתוח וכימותרפיה. אימונותרפיה — שימוש בתאי מערכת החיסון של הגוף להלחם בסרטן — שינתה את הטיפול בחלק מהסרטןי הדם אך התקשתה בגידולים מוצקים כמו סרטן השחלה. המחקר הזה חוקר פיתוח חדש בטיפול בתאי T שמטרתו לכוון לקולטן שנפוץ בתאי סרטן השחלה, ושואל שאלה עיצובית מעשית: איזו "מנוע" פנימי בתוך תאי ה‑T האלה הופך אותם ליותר קטלניים נגד סרטן?
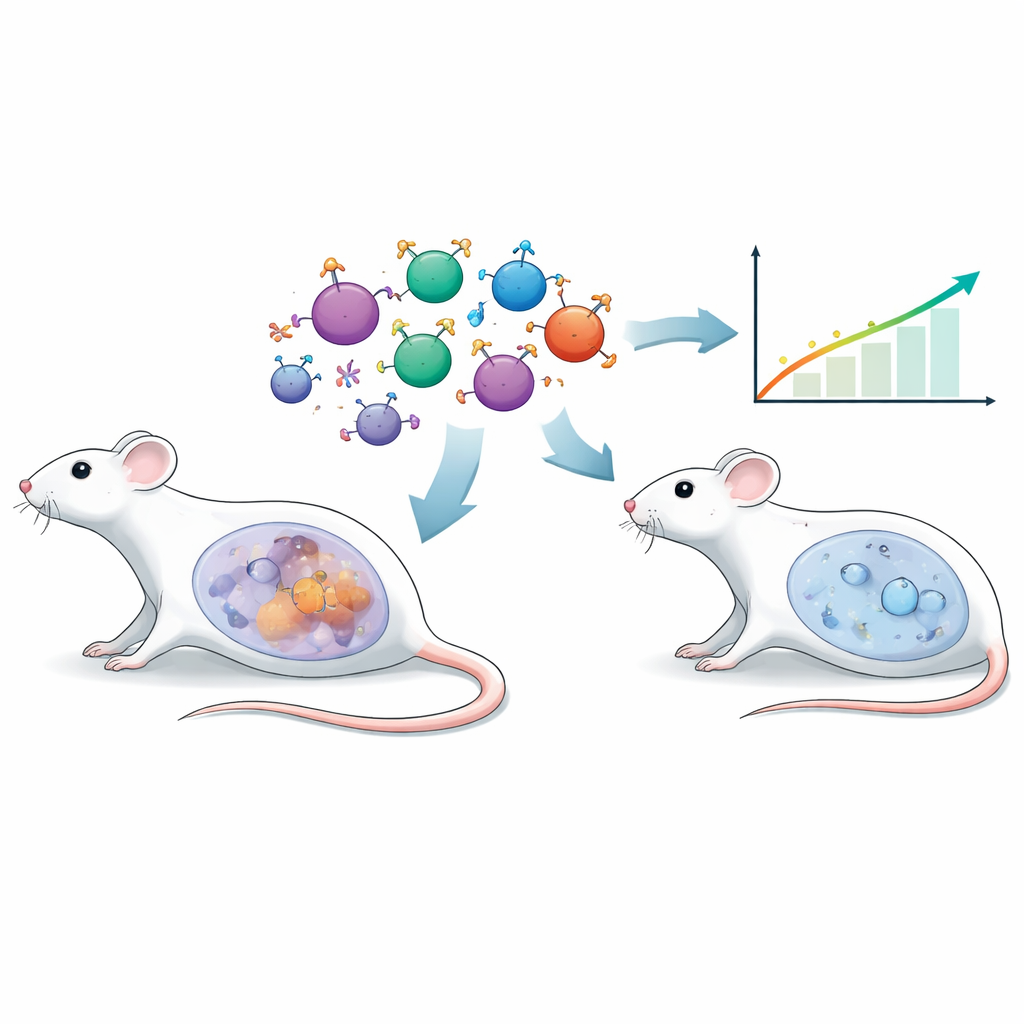
דרך חדשה לנווט תאי חיסון
טיפולי תאי T מהונדסים מסורתיים מסתמכים לעתים קרובות על קטעי נוגדן מלאכותיים לזיהוי גידולים. כאן השתמשו החוקרים באסטרטגיה שונה שנקראת קולטן אנדוקריני כימרי (CER). במקום נוגדן, החלק החיצוני של תאי ה‑T הללו נושא את ההורמון מגרה הזקיק (FSH), הורמון טבעי הידוע בעיקר בתפקידו בפוריות. תאי סרטן שחלה רבים מבטאים על המשטח שלהם את הקולטן המתאים להורמון זה (FSHR). על ידי הענקת קולטן מבוסס FSH לתאי T של העכברים, הקבוצה כיוונה אותם באופן ספציפי כלפי תאי גידול שחלתיים חיוביים ל‑FSHR, במטרה לדיוק מכוון עם נזק מינימלי לרקמות בריאות.
בניית מודל סרטן שחלה קשה יותר
כדי לבחון את הגישה בסביבה מציאותית, השתמשו המדענים בקו סרטן שחלה של עכברים בשם ID8 ומהנדסים גרסה שמבטאת FSHR ברמות גבוהות (ID8‑FSHR). כאשר הושתלו בבטן העכברים, הגידולים העשירים ב‑FSHR גדלו באגרסיביות רבה יותר מהקו המקורי. החיות עלו במשקל במהירות יותר עקב הצטברות נוזלים, הראו אותות גידול גבוהים יותר בהדמיה ונפטרו מוקדם יותר. פעילות גנטית בתוך הגידולים הוסטה לתוכניות התומכות בסרטן, והנוזל הסובב הראה שינויים רחבים בחלבונים ובמטבוליטים אשר איתרו סביבה עוינת יותר המדכאת את החיסון. בדגש על הרלוונטיות הקלינית, תאים מנוזל האסקיטס של שמונה נשים עם סרטן אפיתלי של השחלה הראו גם הם ביטוי FSHR.
השוואת שני "מנועים" פנימיים בתאי T
בכל רצפטור מהונדס יש יחידת איתות שמורותת לתא ה‑T כמה חזק וכמה זמן להגיב. הצוות השווה שני עיצובים קושרי‑תוספת (co‑stimulatory) בשימוש נרחב — CD28ζ ו‑4‑1BBζ — בתוך תאי FSH‑CER זהים מלבד זאת, לצד גרסה בקרה מינימלית. בצלחות מעבדה, תאי FSH‑CER עם מודול CD28ζ (שנקראו FSH‑28ζ) עקפו בקביעות את אלה עם 4‑1BBζ. הם הרגו תאי גידול חיוביים ל‑FSHR ביעילות גבוהה יותר, התחלקו בעוצמה רבה יותר, עברו למצבי זיכרון הקשורים לחיסון מתמשך ושחררו רמות גבוהות יותר של שליחים דלקתיים כמו אינטרפרון‑גמא ו‑TNF. מדדי מולקולות של עוצמת איתות וסמנים של הפעלה אישרו שעיצוב מבוסס CD28 סיפק מכה מוקדמת חזקה יותר.
בדיקת הטיפול בעכברים חיים
כאשר עכברים המושתלים עם גידולי ID8‑FSHR קיבלו עירוי יחיד של תאי FSH‑CER, התאים המצוידים ב‑CD28 שוב בלטו. חיות שטופלו בתאי FSH‑28ζ הראו אותות גידול נמוכים יותר, פחות הצטברות נוזלים וחיו זמן משמעותית ארוך יותר מאשר אלה שקיבלו 4‑1BBζ או את תאי הבקרה הבלתי פעילים. בזמן דגימות חיסוניות מפורטות, תאי הגידול היו כמעט לא ניתנים לזיהוי בשטיפת הבטן של עכברים שטופלו ב‑CD28. עם זאת, המחקר חשף גם חסרון: כשבוע לאחר העירוי, רוב תאי ה‑CER מהונדסים באזור הגידול נשאו מספר סמני "התשה" (exhaustion), ומספרם הכולל היה נמוך, מה שמעיד שסביבת הגידול הקשה שחקה אותם למרות הפעילות ההתחלתית הגבוהה שלהם.
כשנוזל הגידול מתנגד
החוקרים שאלו מדוע נוזל הבטן של גידולים חיוביים ל‑FSHR מדכא כל כך. כאשר ערבבו אסקיטס של עכברים אלה לתרביות מעבדה, הוא הפחית בצורה חדה את יכולת ההרג, את הגידול ואת האיתות של תאי FSH‑CER, במיוחד של גרסת 4‑1BBζ, בעוד שלא השפיע הרבה על תאי CAR‑T סטנדרטיים נגד CD19 המיועדים למטרה אחרת. ניתוח חלבוני קפדני לא הראה עדויות לכך שתאי הגידול משילים FSHR אל הנוזל כדי לחסום את הרצפטורים. במקום זאת, ניסויים בעכברים חסרי מערכת חיסון נורמלית אשר אינם מייצרים נוגדנים הצביעו על אשמה אחרת: גורמים המיוצרים על‑ידי תאי B או T של החיה בתגובה לגידולים המבטאים FSHR, ובכלל זה סביר שכוללים נוגדנים נגד FSHR, שמפריעים באופן ספציפי לאסטרטגיית המטרה המבוססת‑הורמון הזו.
מה המשמעות לטיפולים עתידיים
לקריאה כללית, המסר המרכזי הוא שלא כל תאי ה‑T המהונדסים שווים, ופרטי החיווט הפנימי שלהם חשובים. במודל עכבר של סרטן השחלה הזה, תאים המזוינים בקולטן מבוסס FSH ובגרעין איתות CD28ζ היו קטלניים יותר כלפי הגידול והאריכו את ההישרדות יותר מאשר אלה שבנו עם גרעין 4‑1BBζ. יחד עם זאת, המחקר חושף כיצד סביבה הנוזלית סביב גידולי השחלה יכולה להחליש את כוחם של תאי החיסון הללו, ייתכן באמצעות נוגדנים נגד הקולטן שהם ממקדים. הממצאים תומכים בתאי FSH‑CER מבוססי CD28 כתבנית מבטיחה לאימונותרפיות עתידיות לסרטן השחלה, ובו‑בזמן מדגישים שכל אסטרטגיה קלינית תצטרך לזווג תאים כאלה בצעדים המונעים או הופכים את התשישות החיסונית ומנטרלים את המרחב המדכא של הגידול.
ציטוט: Beatty, N.J., Ma, M., Goala, P. et al. CD28 co-stimulatory domain enhances efficacy of CER T cell therapy compared to 4-1BB in an ovarian cancer mouse model. Sci Rep 16, 13068 (2026). https://doi.org/10.1038/s41598-026-43225-0
מילות מפתח: סרטן השחלה, טיפול בתאי T, אימונותרפיה, קולטן להורמון מגרה זקיק, מיקרו‑סביבת הגידול