Clear Sky Science · ar
مجال التحفيز المرافق CD28 يعزز فعالية علاج الخلايا التائية CER مقارنةً بـ 4-1BB في نموذج فأري لسرطان المبيض
لماذا تهم هذه الدراسة المرضى
غالباً ما يُكتشف سرطان المبيض بعد أن يكون قد انتشر بهدوء في البطن، ولا تزال العديد من النساء المصابات بمرض متقدم يمتن رغم الجراحة والعلاج الكيميائي. لقد غيّر العلاج المناعي — باستخدام خلايا الجهاز المناعي نفسها لمكافحة السرطان — نتائج بعض سرطانات الدم، لكنه ظل يواجِه صعوبات في الأورام الصلبة مثل سرطان المبيض. تستكشف هذه الدراسة نهجاً جديداً للعلاج بالخلايا التائية يهدف إلى استهداف مستقبل موجود شائعاً على خلايا سرطان المبيض وتسأل سؤال تصميم عملي: أي «محرك» داخلي داخل هذه الخلايا يجعلها أكثر فتكاً بالسرطان؟
طريقة جديدة لتوجيه الخلايا المناعية
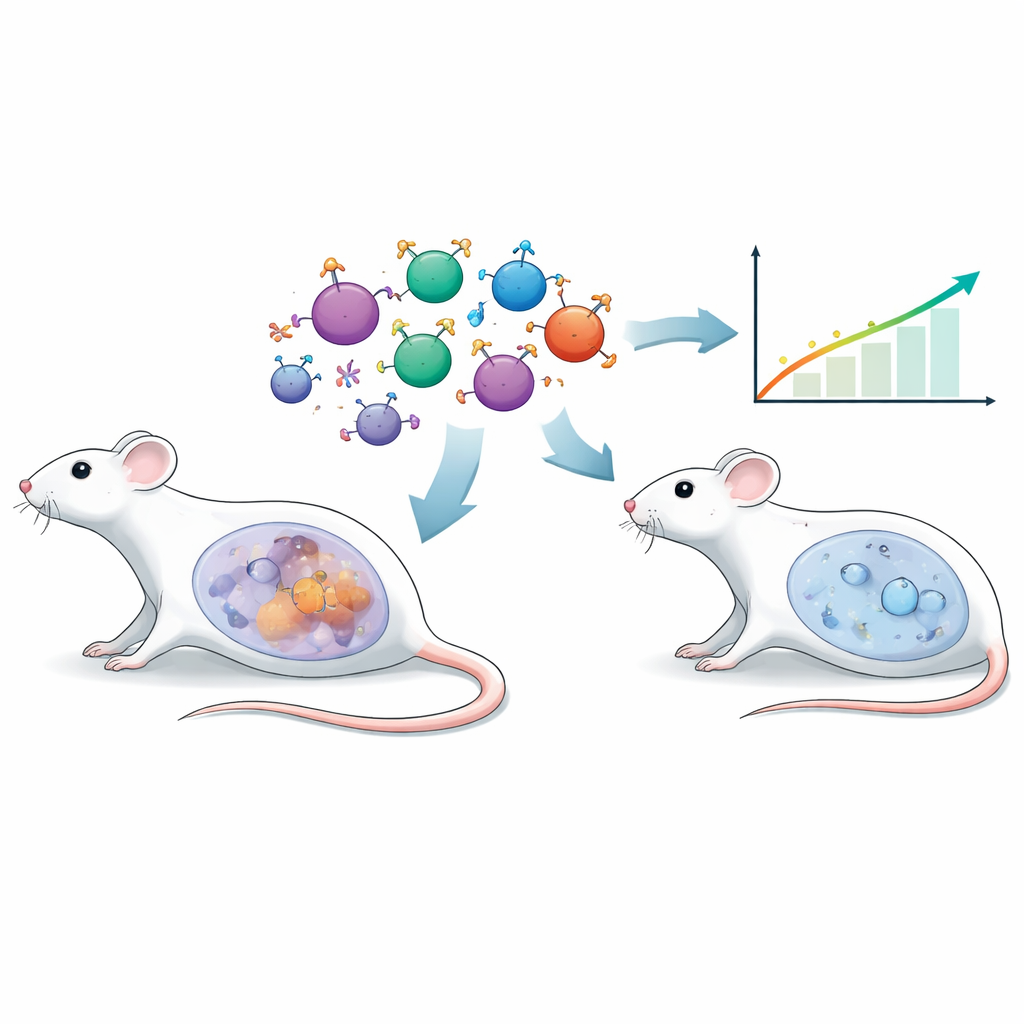
تعتمد علاجات الخلايا التائية الهندسية التقليدية في الغالب على شظايا مضادات أجسام مصنعة للتعرف على الأورام. هنا استخدم الباحثون استراتيجية مختلفة تسمى المستقبل الغشائي الهرموني الهجين، أو CER. بدلاً من مضاد الجسم، يحمل سطح هذه الخلايا التائية هرموناً طبيعياً هو الهرمون المحفز للجريب (FSH)، وهو هرمون معروف بدوره في الخصوبة. تُظهر العديد من سرطانات المبيض وجود مستقبل الهرمون المحفز للجريب (FSHR) على سطحها. من خلال تزويد خلايا تائية فأرية بمستقبل قائم على FSH، وجه الفريق هذه الخلايا تحديداً نحو خلايا الورم الموجبة لـ FSHR، ساعين لتحقيق استهداف دقيق مع إحداث أقل ضرر ممكن للأنسجة الطبيعية.
بناء نموذج أقسى لسرطان المبيض
لاختبار هذا الأسلوب في إعداد واقعي، استخدم العلماء سلالة فأرية لسرطان المبيض تسمى ID8 وهدَفوا إلى هندسة نسخة تعبر عن مستويات عالية من FSHR (ID8‑FSHR). عندما زُرِعَت هذه الأورام الغنية بـ FSHR في تجويف البطن للفئران، نمت هذه الأورام بسرعة أكبر من السلالة الأصلية. كسبت الحيوانات الوزن بشكل أسرع بسبب تراكم السوائل، وظهرت إشارات ورمية أعلى في التصوير، وماتت في وقت أبكر. تحولت برامج نشاط الجينات في الأورام نحو برامج تعزز السرطان، وأظهرت السوائل المحيطة تغيّرات واسعة في البروتينات والمواد الأيضية تشير إلى بيئة أكثر عدائية وكبحاً للمناعة. ومن المهم أن خلايا من سائل الاستسقاء (ascites) لثماني نساء مصابات بسرطان بطانية المبيض أظهرت أيضاً FSHR، مما يدعم الأهمية السريرية لهذا الهدف.
مقارنة محركين داخليين في الخلايا التائية
داخل كل مستقبل مهجن هناك وحدة إشارية تخبر الخلية التائية بمدى قوة ومدة الاستجابة. قارن الفريق تصميمين تحفيزيين داخليين مستخدمين على نطاق واسع — CD28ζ و4‑1BBζ — ضمن خلايا FSH‑CER التائية المتطابقة خلاف ذلك، إلى جانب نسخة مراقبة بسيطة. في الأطباق المخبرية، تفوقت خلايا FSH‑CER التائية المزودة بوحدة CD28ζ (المسماة FSH‑28ζ) باستمرار على تلك المزودة ب4‑1BBζ. قتلت خلايا الورم الموجبة لـ FSHR بكفاءة أكبر، وانقسمت بشكل أقوى، ومالت نحو حالات شبيهة بالذاكرة المرتبطة بالمناعة المستمرة، وأفرجت عن مستويات أعلى من الرسل الالتهابية مثل الإنترفيرون‑غاما وعامل نخر الورم. وقراءات الجزيئات المتعلقة بقوة الإشارة ومؤشرات التنشيط أكدت أن التصميم المبني على CD28 قدّم ضربة مبكرة أقوى.
اختبار العلاج في فئران حية
عندما تلقت الفئران الحاملة لأورام ID8‑FSHR تسريباً واحداً من خلايا FSH‑CER التائية، تميّزت مرة أخرى الخلايا المزودة بـ CD28. كانت الحيوانات المعالجة بخلايا FSH‑28ζ تمتلك إشارات ورمية أقل، وتراكم سائل أقل، وعاشت لفترة أطول بكثير مقارنة بتلك التي أعطيت إما 4‑1BBζ أو الخلايا الضابطة غير النشطة. عند وقت أخذ عينات مناعية مفصّلة، كانت خلايا الورم بالكاد قابلة للكشف في غسل البطن للفئران المعالجة بـ CD28. ومع ذلك، كشفت الدراسة أيضاً عن جانب سلبي: بعد أسبوع واحد من التسريب، حملت معظم الخلايا التائية المهندسة في منطقة الورم مؤشرات متعددة لـ «الإجهاد» (exhaustion)، وكانت الأعداد الإجمالية لخلايا CER التائية منخفضة، مما يشير إلى أن بيئة الورم القاسية أرهقت هذه الخلايا رغم نشاطها الأولي المتفوق.
عندما يقاوم سائل الورم
بعد ذلك سأل الباحثون لماذا كان سائل البطن من الأورام الموجبة لـ FSHR مثبطاً إلى هذا الحد. عندما أضافوا استسقاء من هذه الفئران إلى مزروعات مخبرية، قلّل بشدة من قدرة القتل والنمو والإشارة لخلايا FSH‑CER التائية، لا سيما نسخة 4‑1BBζ، بينما كان له تأثير طفيف على خلايا CAR T المعيارية الموجهة ضد CD19 لمستهدف مختلف. أظهر تحليل بروتيني دقيق عدم وجود دليل على أن خلايا الورم كانت تطرَح FSHR في السائل لتسد المستقبلات. وبدلاً من ذلك، أشارت تجارب في فئران ناقصة المناعة قادرة على عدم إنتاج الأجسام المضادة إلى سبب آخر: عوامل تنتجها خلايا B أو T الخاصة بالحيوان استجابةً للأورام ذات التعبير العالي لـ FSHR، وربما تشمل أجساماً مضادة ضد FSHR، تتداخل بشكل خاص مع استراتيجية الاستهداف القائمة على هذا الهرمون.
ماذا يعني هذا للعلاجات المستقبلية
بالنسبة للقارئ العام، الرسالة الأساسية هي أن ليس كل الخلايا التائية المهندسة متساوية، وتفاصيل توصيلها الداخلي مهمة. في نموذج فأري لسرطان المبيض هذا، كانت الخلايا التائية المزودة بمستقبل قائم على FSH ونواة إشارية CD28ζ قادرة على قتل الأورام بشكل أقوى ومددت البقاء بشكل أفضل من تلك المبنية بنواة 4‑1BBζ. في الوقت نفسه، تكشف الدراسة كيف يمكن أن تستنزف بيئة السائل المحيطة بأورام المبيض قوة هذه الخلايا المناعية، ربما عبر أجسام مضادة ضد المستقبل ذاته. تدعم الدراسة خلايا FSH‑CER ذات أساس CD28 كخريطة طريق واعدة لعلاجات مناعية مستقبلية لسرطان المبيض، مع التأكيد على أن أي استراتيجيّة سريرية ستحتاج إلى إقران مثل هذه الخلايا بإجراءات تمنع أو تعكس إجهاد المناعة وتصدّ البيئة المكبِّحة للورم.
الاستشهاد: Beatty, N.J., Ma, M., Goala, P. et al. CD28 co-stimulatory domain enhances efficacy of CER T cell therapy compared to 4-1BB in an ovarian cancer mouse model. Sci Rep 16, 13068 (2026). https://doi.org/10.1038/s41598-026-43225-0
الكلمات المفتاحية: سرطان المبيض, علاج بالخلايا التائية, العلاج المناعي, مستقبل الهرمون الملوتن, البيئة الدقيقة للورم