Clear Sky Science · fr
Le domaine co‑stimulatoire CD28 améliore l’efficacité de la thérapie par cellules T CER par rapport à 4‑1BB dans un modèle murin du cancer de l’ovaire
Pourquoi cette recherche importe pour les patientes
Le cancer de l’ovaire est souvent découvert seulement après s’être discrètement étendu dans l’abdomen, et de nombreuses femmes atteintes d’une maladie avancée décèdent malgré la chirurgie et la chimiothérapie. L’immunothérapie — utiliser les propres cellules immunitaires du corps pour combattre le cancer — a transformé certains cancers du sang mais a peiné dans les tumeurs solides comme le cancer de l’ovaire. Cette étude explore une nouvelle variante de la thérapie par cellules T visant un récepteur fréquemment présent sur les cellules ovariennes et pose une question de conception pratique : quel « moteur » interne de ces cellules T les rend meilleures pour tuer le cancer ?
Une nouvelle façon d’orienter les cellules immunitaires
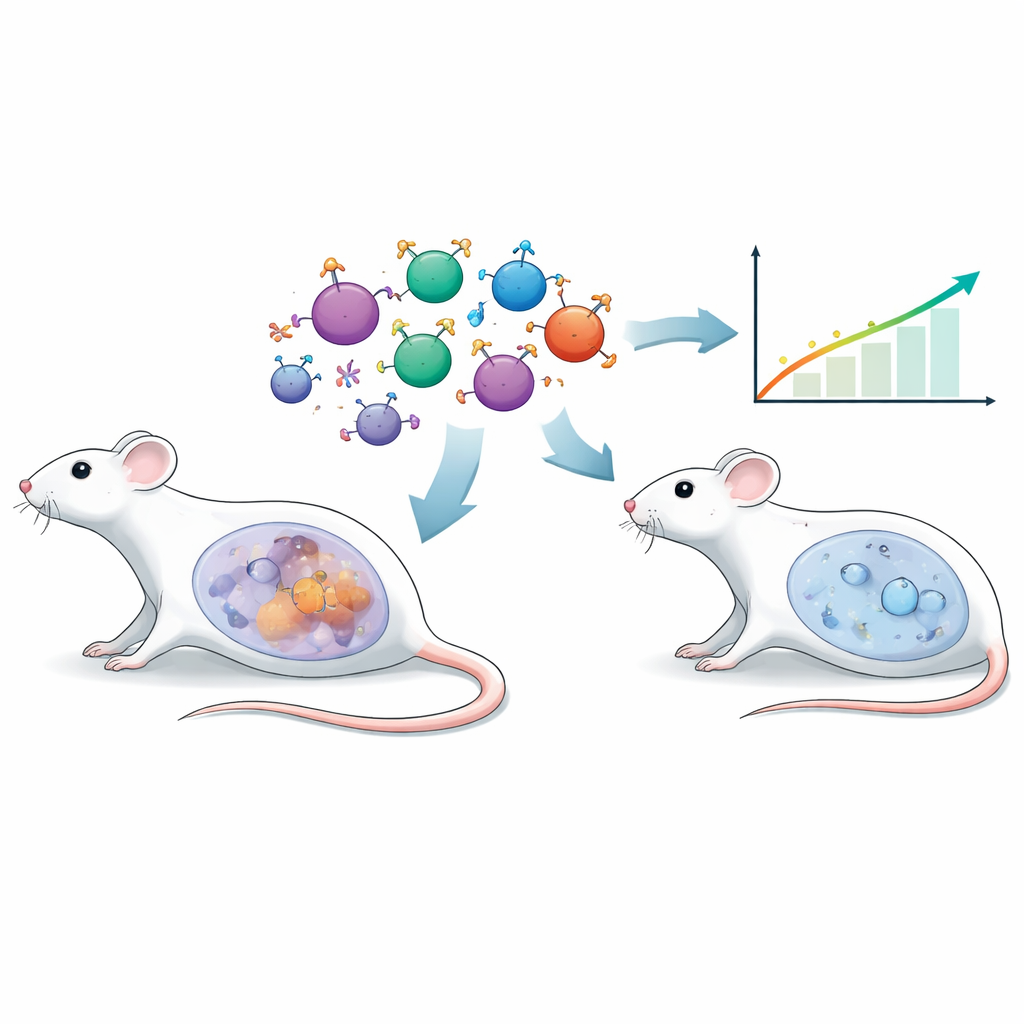
Les thérapies classiques de cellules T génétiquement modifiées reposent souvent sur des fragments d’anticorps artificiels pour reconnaître les tumeurs. Ici, les chercheurs ont utilisé une stratégie différente appelée récepteur endocrinien chimérique, ou CER. Au lieu d’un anticorps, l’extérieur de ces cellules T porte l’hormone folliculo‑stimulante (FSH), une hormone naturelle surtout connue pour son rôle dans la fertilité. De nombreux cancers de l’ovaire expriment à leur surface le récepteur correspondant, le récepteur de la FSH (FSHR). En équipant des cellules T de souris d’un récepteur basé sur la FSH, l’équipe les a dirigées spécifiquement vers les cellules tumorales ovariennes positives pour FSHR, visant un ciblage précis avec un minimum de dommages aux tissus normaux.
Construire un modèle du cancer de l’ovaire plus robuste
Pour tester cette approche dans un contexte réaliste, les scientifiques ont utilisé une lignée murine de cancer de l’ovaire appelée ID8 et ont conçu une version surexprimant FSHR (ID8‑FSHR). Lorsqu’elles sont implantées dans l’abdomen des souris, ces tumeurs riches en FSHR croissent plus agressivement que la lignée originale. Les animaux ont pris du poids plus rapidement en raison d’un épaississement liquidien, ont présenté des signaux tumoraux plus élevés à l’imagerie et sont morts plus tôt. L’activité génétique dans les tumeurs a basculé vers des programmes favorisant le cancer, et le liquide environnant a montré de larges changements protéiques et métaboliques indiquant un milieu plus hostile et immunosuppresseur. Fait important, des cellules provenant de l’ascite de huit femmes atteintes d’un cancer épithélial de l’ovaire ont également exprimé FSHR, soutenant la pertinence clinique de cette cible.
Comparer deux « moteurs » internes dans les cellules T
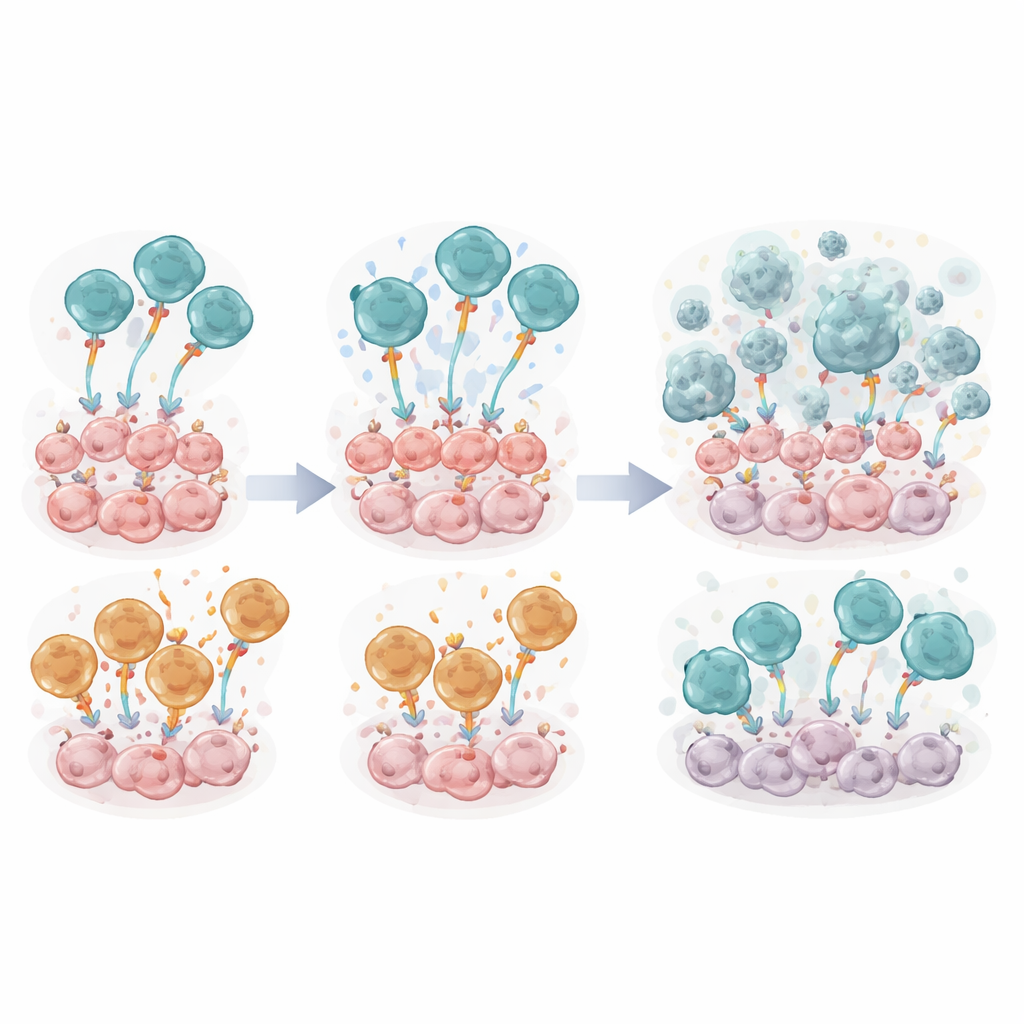
À l’intérieur de chaque récepteur artificiel se trouve un module de signalisation qui indique à la cellule T l’intensité et la durée de sa réponse. L’équipe a comparé deux conceptions co‑stimulatoires largement utilisées — CD28ζ et 4‑1BBζ — au sein de cellules FSH‑CER identiques par ailleurs, en parallèle d’une version témoin minimale. En culture, les cellules FSH‑CER munies du module CD28ζ (appelées FSH‑28ζ) ont systématiquement surpassé celles à 4‑1BBζ. Elles tuaient les cellules tumorales positives pour FSHR plus efficacement, se divisaient de façon plus robuste, évoluaient vers des états proches de cellules mémoires associés à une immunité durable, et libéraient des niveaux plus élevés de médiateurs inflammatoires tels que l’interféron‑gamma et le facteur de nécrose tumorale. Les mesures moléculaires de la force de signalisation et des marqueurs d’activation ont confirmé que la conception basée sur CD28 fournissait un coup d’envoi plus puissant.
Tester la thérapie chez des souris vivantes
Lorsque des souris portant des tumeurs ID8‑FSHR ont reçu une unique perfusion de cellules T FSH‑CER, les cellules équipées de CD28 se sont à nouveau distinguées. Les animaux traités avec des cellules FSH‑28ζ présentaient des signaux tumoraux plus faibles, moins d’accumulation de liquide, et une survie significativement prolongée comparée à ceux ayant reçu soit 4‑1BBζ soit les cellules témoins inactives. Au moment des prélèvements immunitaires détaillés, les cellules tumorales étaient presque indétectables dans le lavage abdominal des souris traitées par CD28. Toutefois, l’étude a aussi révélé un inconvénient : une semaine après la perfusion, la plupart des cellules T génétiquement modifiées dans la région tumorale portaient plusieurs marqueurs d’« épuisement », et le nombre total de cellules CER était faible, indiquant que le milieu tumoral hostile les épuisaient malgré leur activité initiale supérieure.
Quand le liquide tumoral riposte
Les chercheurs ont ensuite interrogé pourquoi l’ascite des tumeurs FSHR‑positives était si suppressive. Lorsqu’ils ont ajouté ce liquide à des cultures en laboratoire, il réduisait fortement la capacité de destruction, la prolifération et la signalisation des cellules FSH‑CER, en particulier la version 4‑1BBζ, alors qu’il n’affectait guère des cellules CAR T standard ciblant CD19 conçues pour une autre cible. Une analyse protéique minutieuse n’a pas montré de preuve que les cellules tumorales libéraient FSHR dans le liquide pour bloquer les récepteurs. À la place, des expériences chez des souris déficientes en cellules immunitaires capables de produire des anticorps ont pointé un autre coupable : des facteurs produits par les propres cellules B ou T de l’animal en réponse aux tumeurs surexprimant FSHR, probablement y compris des anticorps anti‑FSHR, qui interfèrent spécifiquement avec cette stratégie de ciblage basée sur une hormone.
Ce que cela implique pour les traitements futurs
Pour un lecteur non spécialiste, le message principal est que toutes les cellules T génétiquement modifiées ne se valent pas, et que les détails de leur câblage interne comptent. Dans ce modèle murin de cancer de l’ovaire, les cellules T équipées d’un récepteur à base de FSH et d’un noyau de signalisation CD28ζ étaient des tueuses de tumeurs plus puissantes et prolongeaient la survie mieux que celles construites avec un noyau 4‑1BBζ. En même temps, le travail met en lumière la manière dont le liquide entourant les tumeurs ovariennes peut affaiblir ces cellules immunitaires, possiblement via des anticorps dirigés contre le récepteur qu’elles ciblent. L’étude soutient les cellules FSH‑CER à base de CD28ζ comme une feuille de route prometteuse pour de futures immunothérapies du cancer de l’ovaire, tout en soulignant que toute stratégie clinique devra associer ces cellules à des mesures pour prévenir ou inverser l’épuisement immunitaire et contrer le milieu suppressif tumoral.
Citation: Beatty, N.J., Ma, M., Goala, P. et al. CD28 co-stimulatory domain enhances efficacy of CER T cell therapy compared to 4-1BB in an ovarian cancer mouse model. Sci Rep 16, 13068 (2026). https://doi.org/10.1038/s41598-026-43225-0
Mots-clés: cancer de l’ovaire, thérapie par cellules T, immunothérapie, récepteur de l’hormone folliculo‑stimulante, microenvironnement tumoral