Clear Sky Science · sv
CD28 co‑stimulerande domän ökar effekten av CER‑T‑cellsterapi jämfört med 4‑1BB i en ovarialcancer‑musmodell
Varför denna forskning är viktig för patienter
Äggstockscancer upptäcks ofta först efter att den tyst spridit sig i buken, och många kvinnor med avancerad sjukdom dör fortfarande trots operation och cytostatika. Immunterapi — att använda kroppens egna immunceller för att bekämpa cancer — har revolutionerat vissa blodcancerformer men har haft svårare att lyckas i solida tumörer som äggstockscancer. Denna studie undersöker en ny variant av T‑cellsterapi som riktar in sig mot en receptor som ofta finns på äggstockscellernas yta och ställer en praktisk konstruktionsfråga: vilken intern ”motor” i dessa T‑celler gör dem bättre på att döda cancer?
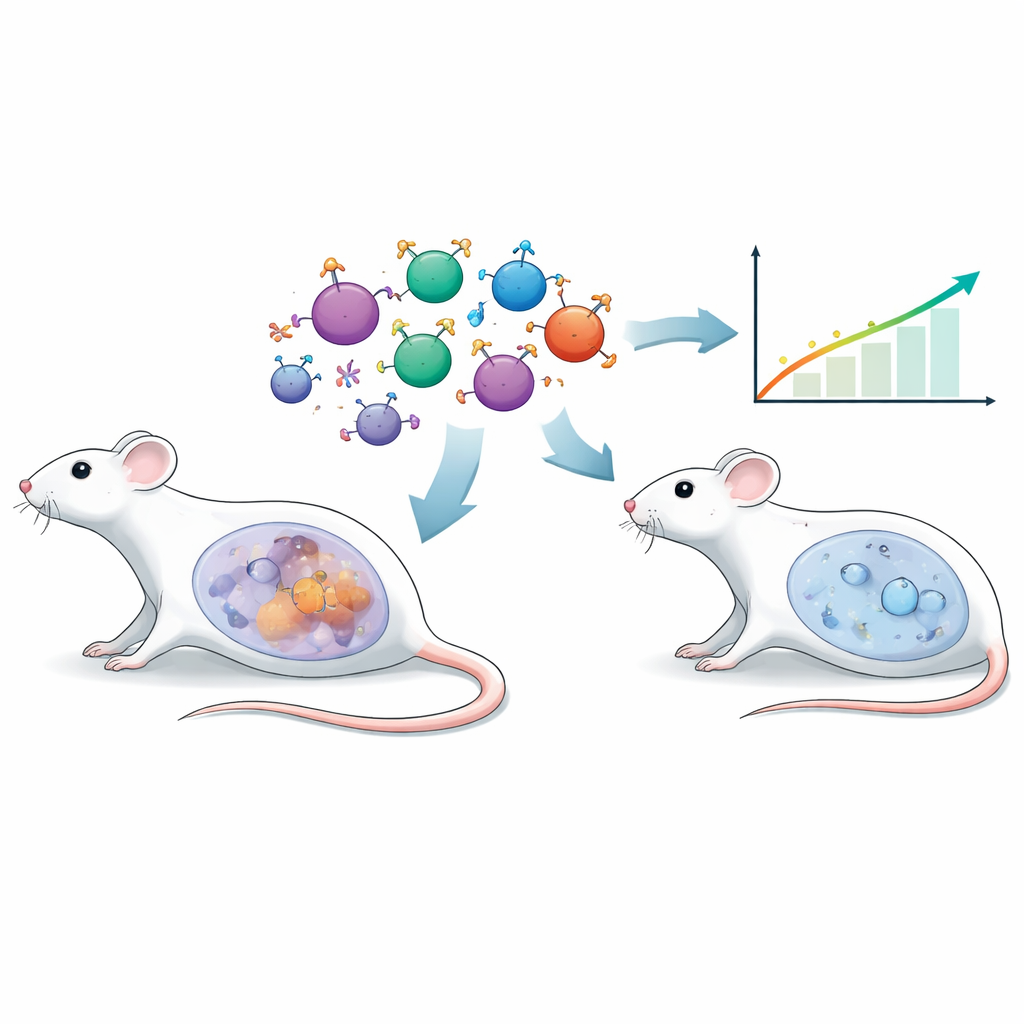
Ett nytt sätt att styra immunceller
Traditionella konstruerade T‑cellsterapier förlitar sig ofta på konstgjorda antikroppsfragment för att känna igen tumörer. Här använde forskarna en annan strategi kallad kimerisk endokrin receptor, eller CER. Istället för en antikropp bär dessa T‑cellers utsida follikelstimulerande hormon (FSH), ett naturligt hormon mest känt för sin roll i fertilitet. Många äggstockscancerformer uttrycker den matchande follikelstimulerande hormonreceptorn (FSHR) på sin yta. Genom att ge mus‑T‑celler en FSH‑baserad receptor riktade teamet dem specifikt mot FSHR‑positiva ovarialtumörceller, med målet att uppnå precis targeting med minimal skada på friska vävnader.
Bygga en tuffare modell för äggstockscancer
För att testa metoden i en mer realistisk miljö använde forskarna en musäggstockscancercellinje kallad ID8 och konstruerade en version som överuttrycker FSHR (ID8‑FSHR). När dessa FSHR‑rika tumörer implanterades i musornas buk växte de aggressivare än den ursprungliga linjen. Djuren lade på sig snabbare på grund av vätskeansamling, hade högre tumörsignal vid avbildning och avled tidigare. Genuttryck i tumörerna skiftade mot program som gynnar cancer, och den omgivande vätskan uppvisade omfattande förändringar i proteiner och metaboliter som signalerade en mer fientlig, immundämpande miljö. Viktigt är att celler från ascitesvätska hos åtta kvinnor med epitelial äggstockscancer också visade FSHR, vilket stöder den kliniska relevansen av detta mål.
Jämförelse av två interna motorer i T‑celler
Inuti varje konstruerad receptor finns en signalmodul som talar om för T‑cellen hur starkt och hur länge den ska svara. Teamet jämförde två vida använda co‑stimulära konstruktioner — CD28ζ och 4‑1BBζ — i annars identiska FSH‑CER T‑celler, tillsammans med en minimal kontrollversion. I laboratorieodlingar presterade FSH‑CER T‑celler med CD28ζ‑modulen (kallad FSH‑28ζ) konsekvent bättre än de med 4‑1BBζ. De dödade FSHR‑positiva tumörceller mer effektivt, delade sig mer robust, skiftade mot minnesliknande tillstånd kopplade till bestående immunitet och frisatte högre nivåer av inflammatoriska budbärare som interferon‑gamma och tumörnekrosfaktor. Molekylära mätningar av signalstyrka och aktiveringsmarkörer bekräftade att CD28‑basen gav ett kraftfullare tidigt genomslag.
Test av terapin i levande möss
När möss med ID8‑FSHR‑tumörer fick en enda infusion av FSH‑CER T‑celler stod CD28‑utrustade celler återigen ut. Djur behandlade med FSH‑28ζ‑celler hade lägre tumörsignal, mindre vätskeansamling och levde signifikant längre än de som fick antingen 4‑1BBζ eller de inaktiva kontrollcellerna. Vid tidpunkten för detaljerad immunsampling var tumörceller nästan omätbara i bukspolningen hos CD28‑behandlade möss. Studien visade dock också en nackdel: redan en vecka efter infusion hade de flesta av de konstruerade T‑cellerna i tumörområdet flera ”utmattnings”‑markörer, och det totala antalet CER‑T‑celler var lågt, vilket indikerar att den hårda tumörmiljön tröttade ut dem trots deras överlägsna initiala aktivitet.
När tumörvätskan slår tillbaka
Forskarna undrade vidare varför bukvätskan från FSHR‑positiva tumörer var så hämmande. När de blandade ascites från dessa möss i odlingskulturer minskade det kraftigt FSH‑CER T‑cellernas dödande förmåga, tillväxt och signalering, särskilt för 4‑1BBζ‑varianten, medan det hade liten effekt på standard CD19 CAR‑celler designade för ett annat mål. Noggranna proteinanalyser visade inget tecken på att tumörcellerna lossnade FSHR i vätskan för att blockera receptorerna. Istället pekade experiment i immundefekta möss som inte kan bilda antikroppar mot en annan syndabock: faktorer producerade av djurets egna B‑ eller T‑celler som svar på FSHR‑överuttryckande tumörer — sannolikt inkluderande anti‑FSHR‑antikroppar — som stör just denna hormonbaserade riktstrategi.
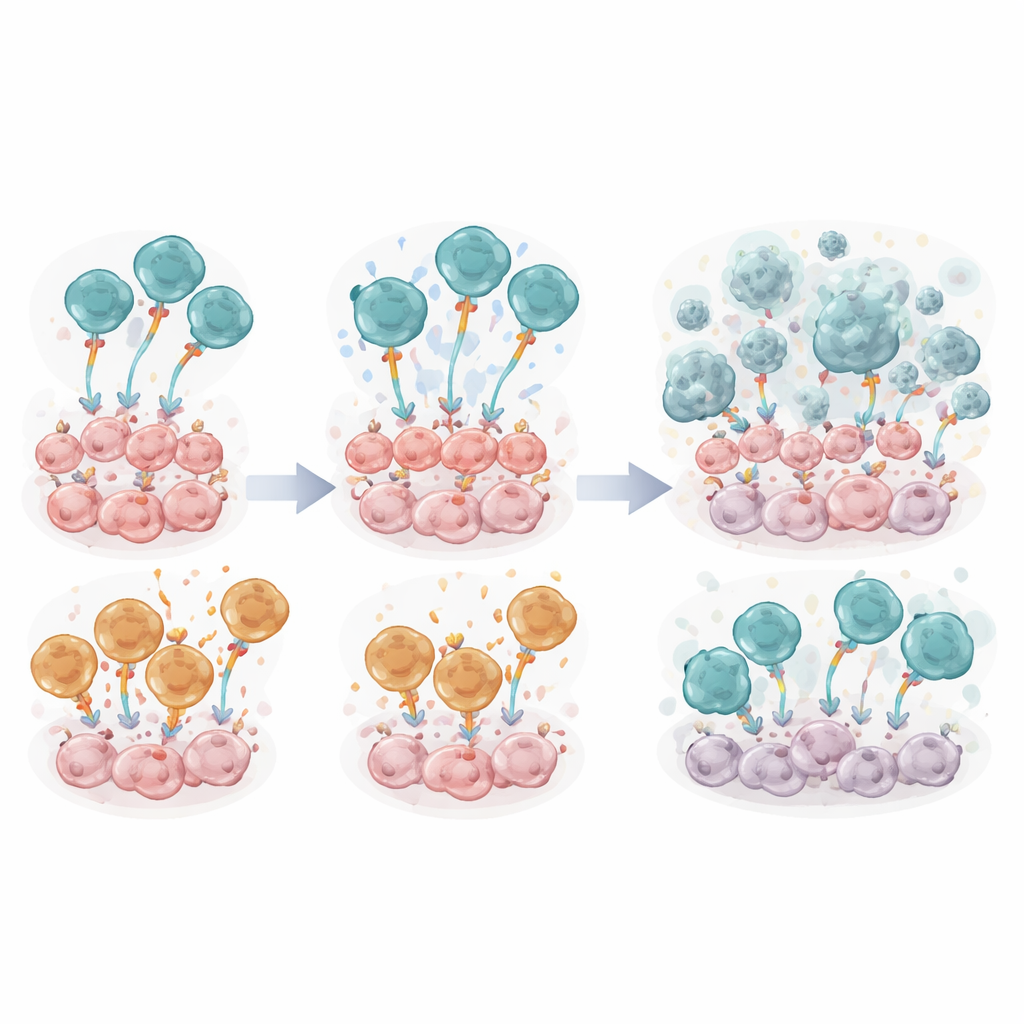
Vad detta betyder för framtida behandlingar
För en lekmäns läsare är huvudbudskapet att inte alla konstruerade T‑celler är likadana, och detaljerna i deras interna koppling är viktiga. I denna ovarialcancer‑musmodell var T‑celler utrustade med en FSH‑baserad receptor och en CD28ζ‑signalstomme mer potenta tumördödare och förlängde överlevnad bättre än de byggda med en 4‑1BBζ‑stomme. Samtidigt visar arbetet hur vätskemiljön runt äggstockstumörer kan urholka styrkan hos dessa immunceller, möjligen genom antikroppar mot just den receptor de riktar sig mot. Studien stöder CD28‑baserade FSH‑CER‑T‑celler som en lovande mall för framtida immunterapier mot äggstockscancer, samtidigt som den understryker att varje klinisk strategi behöver kombineras med åtgärder för att förebygga eller vända immunutmattning och motverka tumörens undertryckande miljö.
Citering: Beatty, N.J., Ma, M., Goala, P. et al. CD28 co-stimulatory domain enhances efficacy of CER T cell therapy compared to 4-1BB in an ovarian cancer mouse model. Sci Rep 16, 13068 (2026). https://doi.org/10.1038/s41598-026-43225-0
Nyckelord: äggstockscancer, T‑cellsterapi, immunterapi, follikelstimulerande hormonreceptor, tumörmikromiljö