Clear Sky Science · it
Il dominio co‑stimolatorio CD28 migliora l’efficacia della terapia con cellule T CER rispetto a 4‑1BB in un modello murino di carcinoma ovarico
Perché questa ricerca conta per i pazienti
Il carcinoma ovarico viene spesso scoperto solo dopo essersi diffuso silenziosamente nella cavità addominale, e molte donne con malattia avanzata muoiono ancora nonostante interventi chirurgici e chemioterapia. L’immunoterapia — l’uso delle cellule immunitarie dell’organismo per combattere il cancro — ha trasformato alcuni tumori ematologici ma ha incontrato difficoltà nei tumori solidi come il carcinoma ovarico. Questo studio esplora una nuova variante della terapia con cellule T che mira a riconoscere un recettore comunemente espresso sulle cellule ovariane e pone una domanda pratica di progettazione: quale “motore” interno dentro queste cellule T le rende migliori nell’eliminare il cancro?
Un nuovo modo di indirizzare le cellule immunitarie
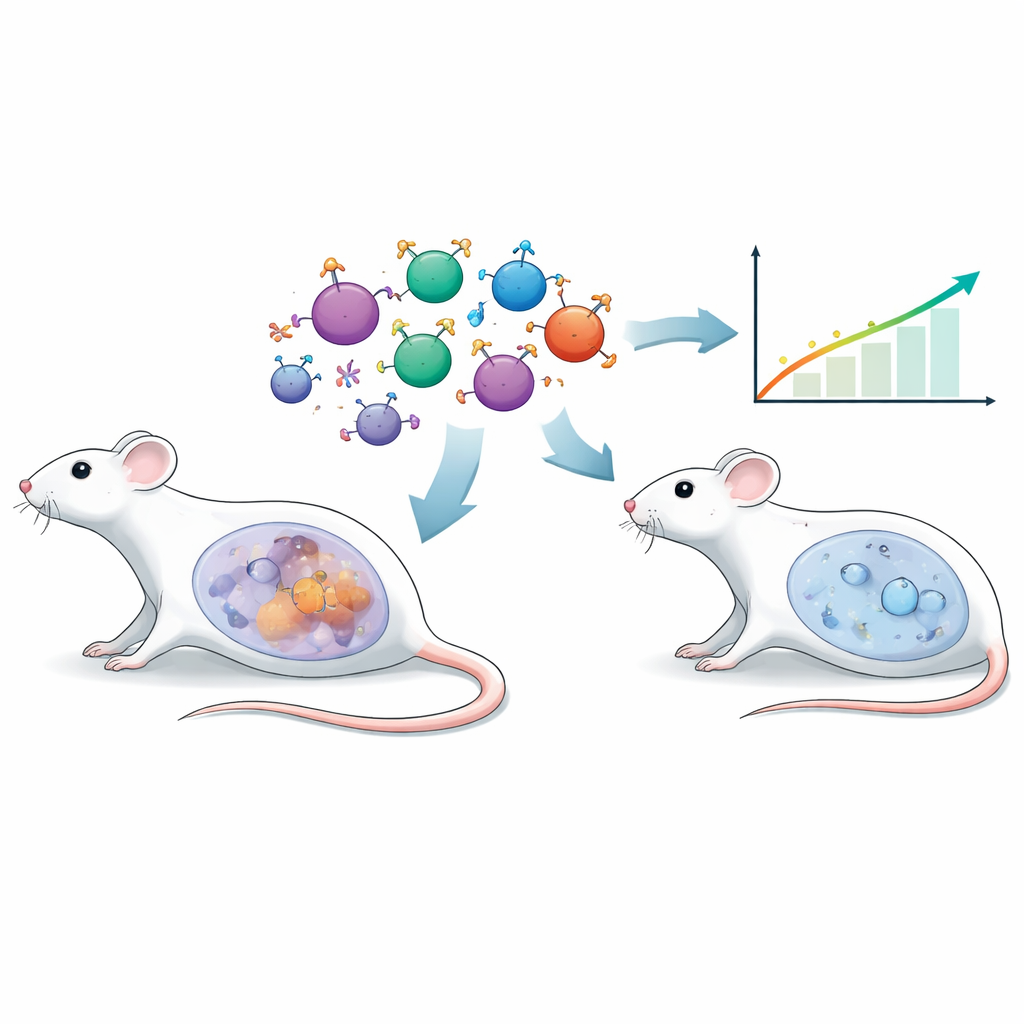
Le terapie tradizionali con cellule T ingegnerizzate spesso si basano su frammenti di anticorpi sintetici per riconoscere i tumori. Qui, i ricercatori hanno usato una strategia diversa chiamata recettore endocrino chimerico, o CER. Invece di un anticorpo, la parte esterna di queste cellule T porta l’ormone follicolo‑stimolante (FSH), un ormone naturale noto soprattutto per il suo ruolo nella fertilità. Molti carcinomi ovarici esprimono sulla superficie il corrispondente recettore per l’FSH (FSHR). Dotando le cellule T dei topi di un recettore basato su FSH, il gruppo le ha dirette specificamente verso le cellule tumorali ovariche FSHR‑positive, puntando a un targeting preciso con danni minimi ai tessuti normali.
Costruire un modello più aggressivo di carcinoma ovarico
Per testare questo approccio in un contesto realistico, gli scienziati hanno usato una linea murina di carcinoma ovarico chiamata ID8 e ne hanno ingegnerizzato una versione che sovra‑esprime FSHR (ID8‑FSHR). Quando impiantati nella cavità addominale dei topi, questi tumori ricchi di FSHR crescevano più aggressivamente rispetto alla linea originale. Gli animali aumentavano di peso più rapidamente a causa dell’accumulo di liquido, mostravano segnali tumorali più elevati nelle immagini e morivano prima. L’attività genica nei tumori si è spostata verso programmi che favoriscono il cancro, e il fluido circostante ha mostrato ampie modifiche in proteine e metaboliti che indicavano un ambiente più ostile e immunosoppressivo. Importante, cellule provenienti dal liquido ascitico di otto donne con carcinoma ovarico epiteliale hanno mostrato espressione di FSHR, a sostegno della rilevanza clinica di questo bersaglio.
Confronto tra due motori interni nelle cellule T
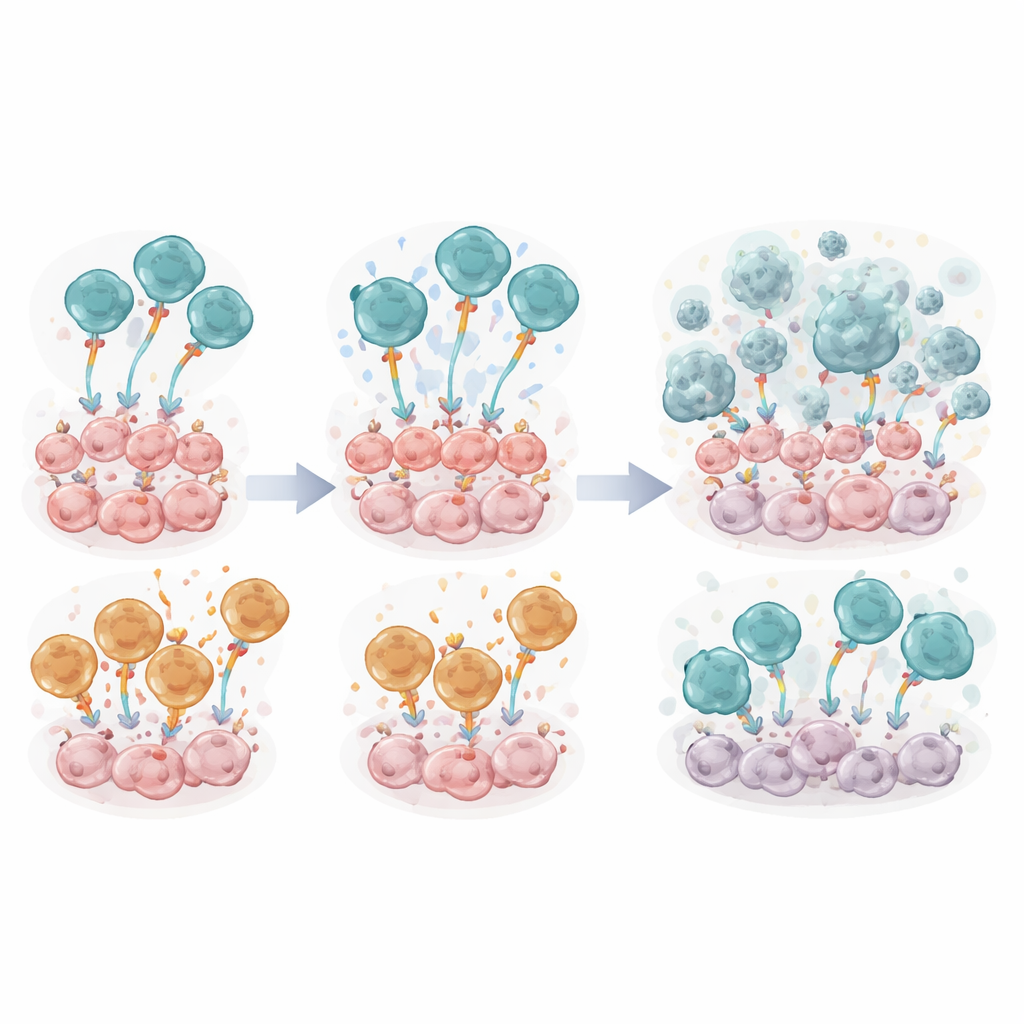
All’interno di ogni recettore ingegnerizzato c’è un modulo di segnalazione che indica alla cellula T quanto intensamente e per quanto tempo rispondere. Il gruppo ha confrontato due design co‑stimolatori ampiamente usati — CD28ζ e 4‑1BBζ — all’interno di cellule T FSH‑CER altrimenti identiche, affiancandoli a una versione di controllo minima. In colture di laboratorio, le cellule FSH‑CER con il modulo CD28ζ (chiamate FSH‑28ζ) hanno costantemente superato quelle con 4‑1BBζ. Hanno ucciso le cellule tumorali FSHR‑positive in modo più efficiente, si sono divise più robustamente, hanno assunto stati simili alla memoria associati a immunità duratura e hanno rilasciato livelli più alti di messaggeri infiammatori come interferone‑gamma e fattore di necrosi tumorale. Letture molecolari della forza di segnalazione e dei marcatori di attivazione hanno confermato che il design basato su CD28 forniva un colpo iniziale più potente.
Testare la terapia nei topi vivi
Quando i topi portatori di tumori ID8‑FSHR hanno ricevuto una singola infusione di cellule T FSH‑CER, le cellule dotate di CD28 si sono nuovamente distinte. Gli animali trattati con cellule FSH‑28ζ hanno mostrato segnali tumorali più bassi, meno accumulo di liquido e una sopravvivenza significativamente più lunga rispetto a quelli a cui sono state date cellule con 4‑1BBζ o le cellule di controllo inattive. Al momento dei prelievi immunologici dettagliati, le cellule tumorali erano quasi assenti nel lavaggio addominale dei topi trattati con CD28. Tuttavia, lo studio ha anche rivelato un aspetto negativo: entro una settimana dall’infusione, la maggior parte delle cellule T ingegnerizzate nella zona tumorale presentava molti marcatori di “esaurimento” e il numero complessivo di cellule CER era basso, indicando che l’ambiente tumorale ostile le stava affaticando nonostante la loro superiore attività iniziale.
Quando il fluido tumorale contrattacca
I ricercatori hanno quindi chiesto perché il liquido addominale dei tumori FSHR‑positivi fosse così soppressivo. Quando hanno aggiunto ascite di questi topi nelle colture di laboratorio, questa ha ridotto drasticamente la capacità di uccidere, la crescita e la segnalazione delle cellule FSH‑CER, in particolare della versione 4‑1BBζ, mentre ha avuto poco effetto sulle convenzionali cellule CAR T contro CD19 progettate per un bersaglio diverso. Un’analisi proteica accurata non ha mostrato evidenza che le cellule tumorali stessero rilasciando FSHR nel fluido per bloccare i recettori. Invece, esperimenti in topi immunodeficienti incapaci di produrre anticorpi hanno indicato un altro colpevole: fattori prodotti dalle stesse cellule B o T dell’animale in risposta ai tumori che sovra‑esprimono FSHR, probabilmente inclusi anticorpi anti‑FSHR, che interferiscono specificamente con questa strategia di targeting basata sull’ormone.
Cosa significa per i trattamenti futuri
Per un lettore non specialista, il messaggio principale è che tutte le cellule T ingegnerizzate non sono uguali e i dettagli della loro circuiteria interna sono importanti. In questo modello murino di carcinoma ovarico, le cellule T armate con un recettore basato su FSH e un nucleo di segnalazione CD28ζ sono state killer tumorali più potenti e hanno prolungato la sopravvivenza meglio rispetto a quelle costruite con un nucleo 4‑1BBζ. Allo stesso tempo, il lavoro mette in luce come il fluido che circonda i tumori ovarici possa indebolire queste cellule immunitarie, forse tramite anticorpi contro lo stesso recettore che esse mirano. Lo studio supporta le cellule FSH‑CER basate su CD28 come un progetto promettente per future immunoterapie del carcinoma ovarico, sottolineando però che qualsiasi strategia clinica dovrà associare tali cellule a misure per prevenire o invertire l’esaurimento immunitario e contrastare il milieu soppressivo tumorale.
Citazione: Beatty, N.J., Ma, M., Goala, P. et al. CD28 co-stimulatory domain enhances efficacy of CER T cell therapy compared to 4-1BB in an ovarian cancer mouse model. Sci Rep 16, 13068 (2026). https://doi.org/10.1038/s41598-026-43225-0
Parole chiave: carcinoma ovarico, terapia con cellule T, immunoterapia, recettore dell’ormone follicolo‑stimolante, microambiente tumorale