Clear Sky Science · es
El dominio coestimulador CD28 mejora la eficacia de la terapia con células T CER frente a 4-1BB en un modelo murino de cáncer de ovario
Por qué esta investigación importa para las pacientes
El cáncer de ovario suele detectarse solo después de haberse diseminado silenciosamente por el abdomen, y muchas mujeres con enfermedad avanzada siguen falleciendo pese a la cirugía y la quimioterapia. La inmunoterapia —usar las propias células inmunitarias del cuerpo para combatir el cáncer— ha transformado algunos cánceres hematológicos, pero ha tenido dificultades en tumores sólidos como el de ovario. Este estudio explora una variante de la terapia con células T que busca dirigirse a un receptor común en las células de cáncer de ovario y plantea una pregunta práctica de diseño: ¿qué “motor” interno dentro de estas células T las hace mejores para matar el cáncer?
Una nueva forma de dirigir las células inmunitarias
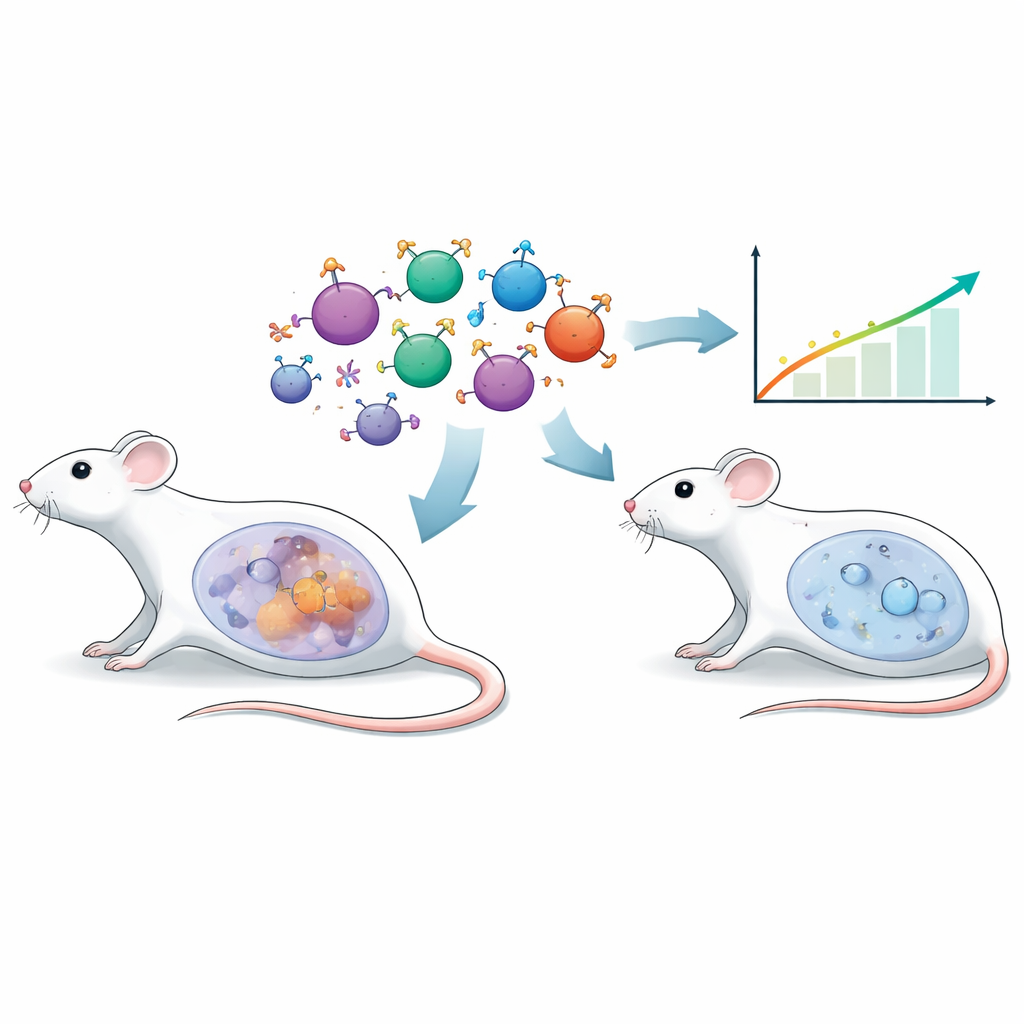
Las terapias tradicionales de células T diseñadas suelen basarse en fragmentos de anticuerpos artificiales para reconocer tumores. Aquí, los investigadores usaron una estrategia diferente llamada receptor endocrino quimérico, o CER. En lugar de un anticuerpo, la superficie de estas células T porta hormona foliculoestimulante (FSH), una hormona natural conocida por su papel en la fertilidad. Muchos cánceres de ovario presentan en su superficie el receptor correspondiente, FSHR. Al dotar a las células T de ratón de un receptor basado en FSH, el equipo las dirigió específicamente hacia las células tumorales ováricas FSHR-positivas, buscando un objetivo preciso con daño mínimo a tejidos normales.
Construyendo un modelo de cáncer de ovario más exigente
Para probar este enfoque en un escenario realista, los científicos usaron una línea murina de cáncer de ovario llamada ID8 y diseñaron una versión que sobreexpresa FSHR (ID8-FSHR). Cuando se implantaron en el abdomen de los ratones, estos tumores ricos en FSHR crecieron con más agresividad que la línea original. Los animales aumentaron de peso más rápido por acumulación de líquido, mostraron señales tumorales más altas en imágenes y murieron antes. La actividad génica en los tumores se desplazó hacia programas que favorecen el cáncer, y el fluido circundante mostró cambios amplios en proteínas y metabolitos que señalaron un entorno más hostil y supresor de la respuesta inmune. De forma importante, células del ascitis de ocho mujeres con cáncer epitelial de ovario también mostraron FSHR, lo que respalda la relevancia clínica de este objetivo.
Comparando dos motores internos en las células T
Dentro de cada receptor diseñado hay un módulo de señalización que indica a la célula T con qué intensidad y durante cuánto tiempo responder. El equipo comparó dos diseños coestimuladores de uso generalizado —CD28ζ y 4-1BBζ— dentro de células T FSH-CER idénticas por lo demás, junto a una versión de control mínima. En cultivos de laboratorio, las células T FSH-CER con el módulo CD28ζ (llamadas FSH-28ζ) superaron de forma consistente a las que tenían 4-1BBζ. Mataron las células tumorales FSHR-positivas con mayor eficiencia, se dividieron con más robustez, evolucionaron hacia estados similares a células de memoria asociados a inmunidad duradera y liberaron niveles más altos de mensajeros inflamatorios como interferón gamma y factor de necrosis tumoral. Lecturas moleculares de la fuerza de señalización y marcadores de activación confirmaron que el diseño basado en CD28 proporcionó un golpe inicial más potente.
Probando la terapia en ratones vivos
Cuando ratones con tumores ID8-FSHR recibieron una única infusión de células T FSH-CER, las células equipadas con CD28 volvieron a destacar. Los animales tratados con células FSH-28ζ presentaron señales tumorales más bajas, menor acumulación de líquido y vivieron significativamente más que aquellos que recibieron 4-1BBζ o las células inactivas de control. En el momento del muestreo inmunitario detallado, las células tumorales eran casi indetectables en el lavado abdominal de los ratones tratados con CD28. Sin embargo, el estudio también reveló un inconveniente: a la semana tras la infusión, la mayoría de las células T diseñadas en la región tumoral mostraban múltiples marcadores de “agotamiento”, y el número total de células CER T era bajo, lo que indica que el duro microambiente tumoral las estaba debilitando pese a su superior actividad inicial.
Cuando el líquido tumoral contraataca
Los investigadores se preguntaron por qué el líquido abdominal de los tumores FSHR-positivos era tan supresor. Al mezclar ascitis de estos ratones en cultivos, se redujo drásticamente la capacidad de lisis, el crecimiento y la señalización de las células T FSH-CER, especialmente la versión 4-1BBζ, mientras que tuvo poco efecto sobre células CAR T CD19 estándar diseñadas para otro objetivo. Un análisis proteico cuidadoso no mostró evidencia de que las células tumorales desprendieran FSHR al fluido para bloquear los receptores. En su lugar, experimentos en ratones inmunodeficientes incapaces de producir anticuerpos apuntaron a otro culpable: factores producidos por las propias células B o T del animal en respuesta a los tumores que sobreexpresan FSHR, probablemente incluidos anticuerpos anti-FSHR, que interfieren específicamente con esta estrategia de orientación basada en la hormona.
Qué significa esto para tratamientos futuros
Para el lector general, el mensaje principal es que no todas las células T diseñadas son iguales y que los detalles de su cableado interno importan. En este modelo murino de cáncer de ovario, las células T armadas con un receptor basado en FSH y un núcleo de señalización CD28ζ fueron más potentes en la eliminación tumoral y prolongaron mejor la supervivencia que las construidas con un núcleo 4-1BBζ. Al mismo tiempo, el trabajo pone de manifiesto cómo el entorno líquido alrededor de los tumores ováricos puede agotar la fuerza de estas células inmunitarias, posiblemente mediante anticuerpos contra el propio receptor que se pretende atacar. El estudio respalda a las células T FSH-CER basadas en CD28 como un diseño prometedor para futuras inmunoterapias del cáncer de ovario, a la vez que subraya que cualquier estrategia clínica deberá combinar estas células con medidas que prevengan o reviertan el agotamiento inmune y contrarresten el entorno supresor del tumor.
Cita: Beatty, N.J., Ma, M., Goala, P. et al. CD28 co-stimulatory domain enhances efficacy of CER T cell therapy compared to 4-1BB in an ovarian cancer mouse model. Sci Rep 16, 13068 (2026). https://doi.org/10.1038/s41598-026-43225-0
Palabras clave: cáncer de ovario, terapia con células T, inmunoterapia, receptor de la hormona foliculoestimulante, microambiente tumoral