Clear Sky Science · pl
Domena kostymulacyjna CD28 zwiększa skuteczność terapii CER komórek T w porównaniu z 4-1BB w modelu mysiego raka jajnika
Dlaczego te badania mają znaczenie dla pacjentek
Rak jajnika bywa często wykrywany dopiero po cichym rozsianiu w jamie brzusznej, a wiele kobiet z zaawansowaną chorobą nadal umiera pomimo operacji i chemioterapii. Immunoterapia — wykorzystanie własnych komórek odpornościowych do walki z rakiem — zrewolucjonizowała niektóre nowotwory krwi, lecz napotyka trudności w guzach litych, takich jak rak jajnika. W tym badaniu zaproponowano nowe podejście do terapii komórkami T, które ma tropić receptor powszechnie występujący na komórkach raka jajnika, i zadano praktyczne pytanie projektowe: który wewnętrzny „silnik” w tych komórkach T czyni je lepszymi zabójcami nowotworu?
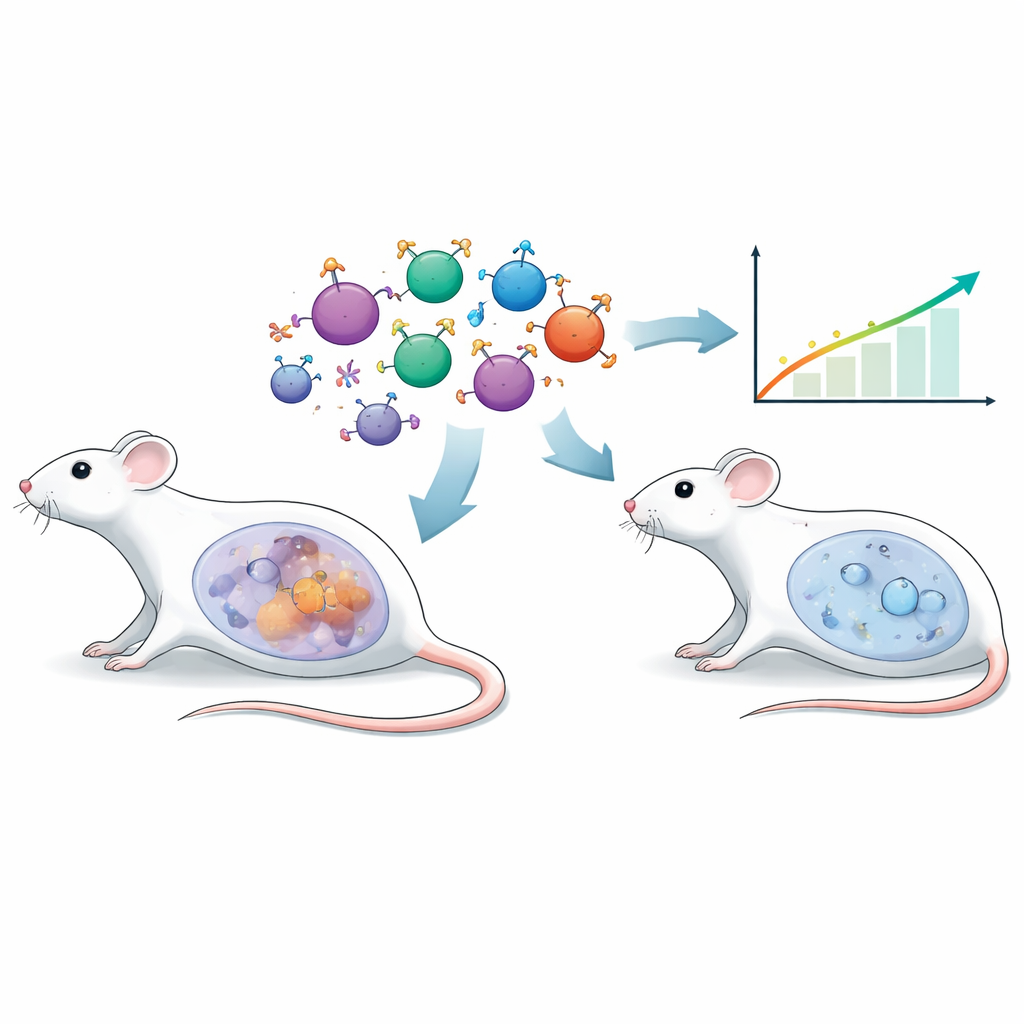
Nowy sposób kierowania komórkami odpornościowymi
Tradycyjne terapie inżynierowanych komórek T często opierają się na fragmentach przeciwciał do rozpoznawania nowotworów. Tutaj badacze zastosowali inną strategię zwaną chimerycznym receptorem endokrynnym (CER). Zamiast przeciwciała, na zewnątrz tych komórek T umieszczono hormon folikulotropowy (FSH), naturalny hormon znany głównie z roli w płodności. Wiele raków jajnika eksponuje na powierzchni odpowiadający mu receptor dla FSH (FSHR). Wyposażając mysie komórki T w receptor oparty na FSH, zespół ukierunkował je specyficznie na komórki guza pozytywne na FSHR, dążąc do precyzyjnego celowania przy minimalnym uszkodzeniu tkanek zdrowych.
Budowanie bardziej wymagającego modelu raka jajnika
Aby przetestować podejście w realistycznym kontekście, naukowcy użyli linii mysiego raka jajnika zwanej ID8 i zaprojektowali wersję nadekspresjonującą FSHR (ID8-FSHR). Po wszczepieniu do jamy brzusznej myszy, guzy bogate w FSHR rosły bardziej agresywnie niż linia macierzysta. Zwierzęta szybciej przybierały na wadze z powodu gromadzenia się płynu, miały silniejsze sygnały nowotworowe w obrazowaniu i umierały wcześniej. Aktywność genów w guzach przesunęła się w kierunku programów sprzyjających nowotworowi, a płyn otaczający guzy wykazywał szerokie zmiany białek i metabolitów wskazujące na bardziej wrogie, tłumiące odpornie środowisko. Co istotne, komórki z płynu otrzewnowego (ascites) ośmiu kobiet z rakiem nabłonkowym jajnika również wykazywały FSHR, co potwierdza kliniczne znaczenie tego celu.
Porównanie dwóch wewnętrznych „silników” w komórkach T
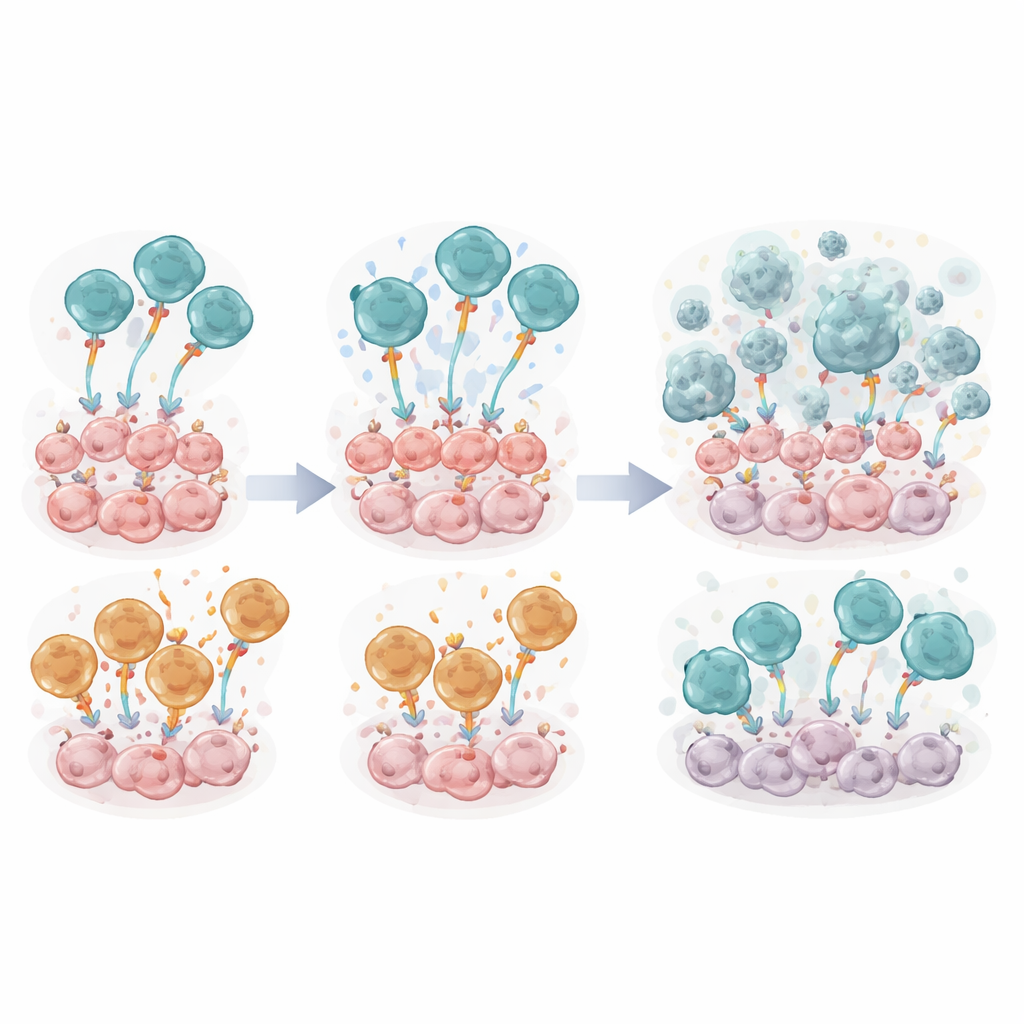
W każdej inżynierowanej cząsteczce receptora znajduje się moduł sygnałowy, który mówi komórce T, jak mocno i jak długo reagować. Zespół porównał dwa powszechnie stosowane projekty kostymulacyjne — CD28ζ i 4-1BBζ — w ramach otherwise identycznych FSH-CER komórek T, wraz z minimalną wersją kontrolną. W hodowlach laboratoryjnych FSH-CER komórki T z modułem CD28ζ (nazwane FSH-28ζ) konsekwentnie przewyższały te z 4-1BBζ. Skuteczniej zabijały komórki nowotworowe pozytywne na FSHR, dzieliły się bardziej intensywnie, przemieszczały się w kierunku stanów pamięciowych związanych z długotrwałą odpornością i wydzielały wyższe poziomy prozapalnych mediatorów, takich jak interferon gamma i czynnik martwicy nowotworów. Odczyty molekularne siły sygnalizacji i markerów aktywacji potwierdziły, że konstrukcja oparta na CD28 dostarczała silniejszego początkowego uderzenia.
Testowanie terapii in vivo w myszach
Gdy myszy z guzami ID8-FSHR otrzymały pojedynczą infuzję FSH-CER komórek T, ponownie to komórki wyposażone w CD28 wyróżniały się. Zwierzęta leczone komórkami FSH-28ζ miały niższe sygnały nowotworowe, mniejsze gromadzenie się płynu i żyły znacząco dłużej niż te otrzymujące 4-1BBζ lub nieaktywną kontrolę. W czasie szczegółowych badań immunologicznych komórki nowotworowe były niemal nieuchwytne w płukance jamy brzusznej myszy leczonych CD28. Jednak badanie ujawniło także wadę: tydzień po infuzji większość inżynierowanych komórek T w rejonie guza nosiła liczne markery „wyczerpania”, a ogólna liczba CER komórek T była niska, co wskazuje, że surowe środowisko guza osłabiało je mimo ich początkowo wyższej aktywności.
Kiedy płyn nowotworowy kontratakuje
Naukowcy zastanawiali się następnie, dlaczego płyn jamy brzusznej z guzów pozytywnych na FSHR był tak tłumiący. Gdy dodawali ascites z tych myszy do kultur komórkowych, znacznie zmniejszał on zdolność zabijania, wzrost i sygnalizację FSH-CER komórek T, szczególnie wersji 4-1BBζ, podczas gdy miał niewielki wpływ na standardowe CD19 CAR T komórki zaprojektowane dla innego celu. Dokładna analiza białek nie wykazała dowodów, że komórki nowotworowe uwalniają FSHR do płynu, aby blokować receptory. Zamiast tego eksperymenty na myszach immunodeficiencyjnych, które nie wytwarzają przeciwciał, wskazały na innego winowajcę: czynniki produkowane przez własne komórki B lub T zwierzęcia w odpowiedzi na guzy nadekspresjonujące FSHR, prawdopodobnie w tym przeciwciała przeciw FSHR, które specyficznie zakłócają tę strategię celowania opartą na hormonie.
Co to oznacza dla przyszłych terapii
Dla czytelnika niebędącego specjalistą główne przesłanie jest takie, że nie wszystkie inżynierowane komórki T są sobie równe i szczegóły ich wewnętrznego okablowania mają znaczenie. W tym mysim modelu raka jajnika komórki T uzbrojone w receptor oparty na FSH i rdzeń sygnałowy CD28ζ były silniejszymi zabójcami guza i lepiej wydłużały przeżycie niż te z rdzeniem 4-1BBζ. Jednocześnie praca ujawnia, jak środowisko płynne wokół guzów jajnika może osłabiać te komórki odpornościowe, prawdopodobnie poprzez przeciwciała skierowane przeciw samemu receptorowi. Badanie popiera CD28-oparte FSH-CER komórki T jako obiecujący schemat dla przyszłych immunoterapii raka jajnika, podkreślając jednocześnie, że każda strategia kliniczna będzie musiała łączyć takie komórki z działaniami zapobiegającymi lub odwracającymi wyczerpanie odporności oraz przeciwdziałającymi tłumiącemu mikrośrodowisku guza.
Cytowanie: Beatty, N.J., Ma, M., Goala, P. et al. CD28 co-stimulatory domain enhances efficacy of CER T cell therapy compared to 4-1BB in an ovarian cancer mouse model. Sci Rep 16, 13068 (2026). https://doi.org/10.1038/s41598-026-43225-0
Słowa kluczowe: rak jajnika, terapia komórkami T, immunoterapia, receptor dla hormonu folikulotropowego, mikrośrodowisko guza