Clear Sky Science · zh
腹膜来源MSC外泌体通过传递miR-320d抑制CCL24合成,有助于改善腹膜透析相关纤维化
为何保护透析膜很重要
对于肾功能衰竭的人来说,腹膜透析提供了在家用自身腹膜作为天然滤过层清洁血液的自由。但多年下来,这层脆弱的膜可能会发生瘢痕化和增厚,最终迫使患者放弃该治疗。该研究探讨了这种瘢痕化发生的原因,并测试了一种前沿的基于细胞的策略,利用微小的生物囊泡来抑制有害的免疫信号,从而帮助维持腹膜的健康。
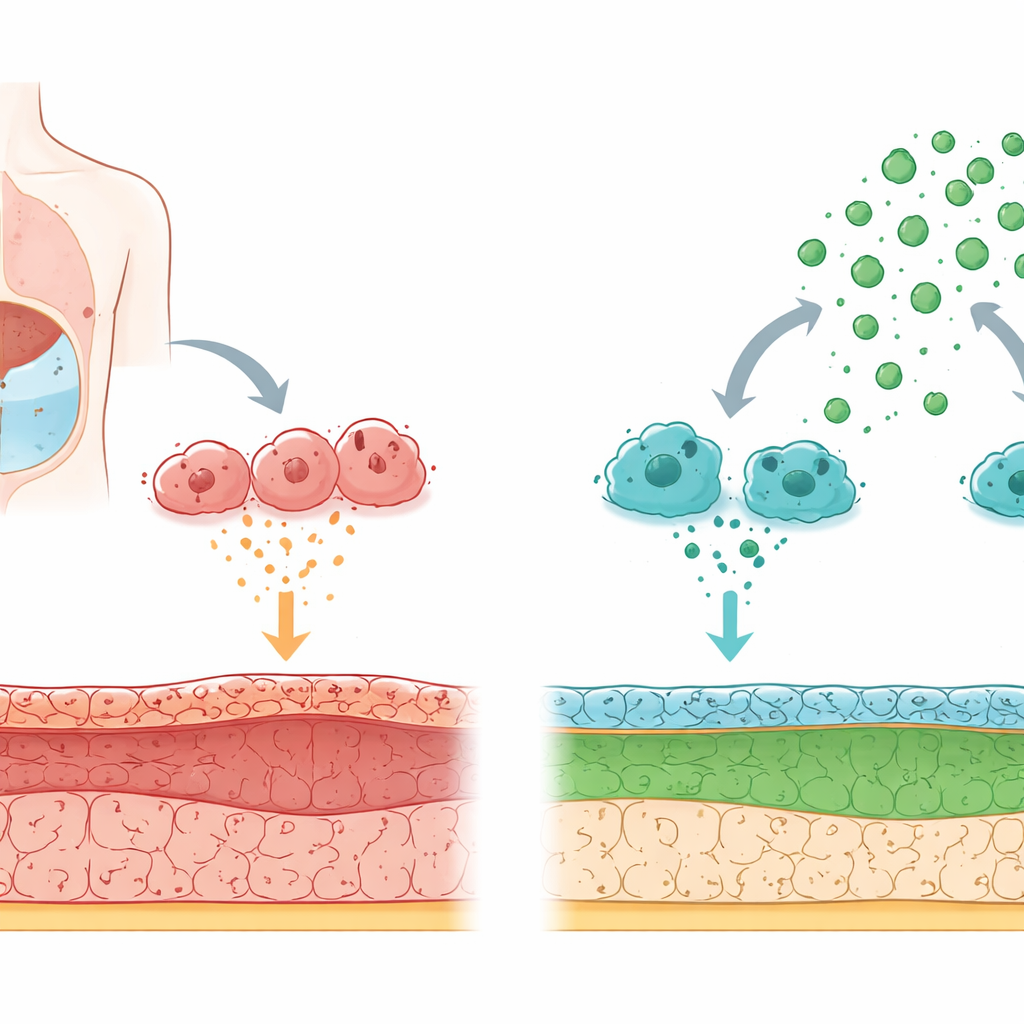
身体过滤层随时间受损的机制
腹膜透析的工作原理是向腹腔注入特殊液体,使废物可以通过腹膜从血液中转移。长期暴露于高葡萄糖的透析液和反复的炎症会逐步损伤这层上皮。直接接触液体的细胞会发生表型改变:它们不再像平滑、保护性的“瓷砖”那样工作,而开始表现成类似瘢痕形成的细胞,沉积刚性的纤维。这种从上皮细胞向瘢痕样细胞的转变推动了膜的增厚和功能丧失。
促使细胞走向瘢痕的免疫信使
研究人员关注的是巨噬细胞——在腹腔巡逻的免疫细胞。在大鼠透析损伤模型中,他们发现在这些巨噬细胞中主要存在高水平的信号蛋白CCL24。当巨噬细胞产生更多CCL24时,邻近的腹膜上皮丧失了有序结构并开始产生纤维蛋白,这是瘢痕形成的标志。阻断巨噬细胞中的CCL24,或阻断其表面受体(称为CCR3)或其下游化学开关(涉及p38蛋白的通路),可阻止上皮细胞向瘢痕细胞转变。这表明巨噬细胞来源的CCL24在瘢痕化过程中处于核心地位。
能抑制有害信号的干细胞囊泡
研究团队随后转向从透析患者废液中分离的间充质干细胞。这些细胞天然释放外泌体——携带小RNA等分子信息的纳米级囊泡。当巨噬细胞暴露于这些干细胞的培养液或纯化的外泌体时,其CCL24的产生和释放显著下降。因此,巨噬细胞分泌物对腹膜的有害影响被减弱,上皮细胞保留了更多保护性特征。将外泌体从干细胞培养液中去除会大幅消除这种益处,表明这些微小囊泡是主要的治疗性信使。
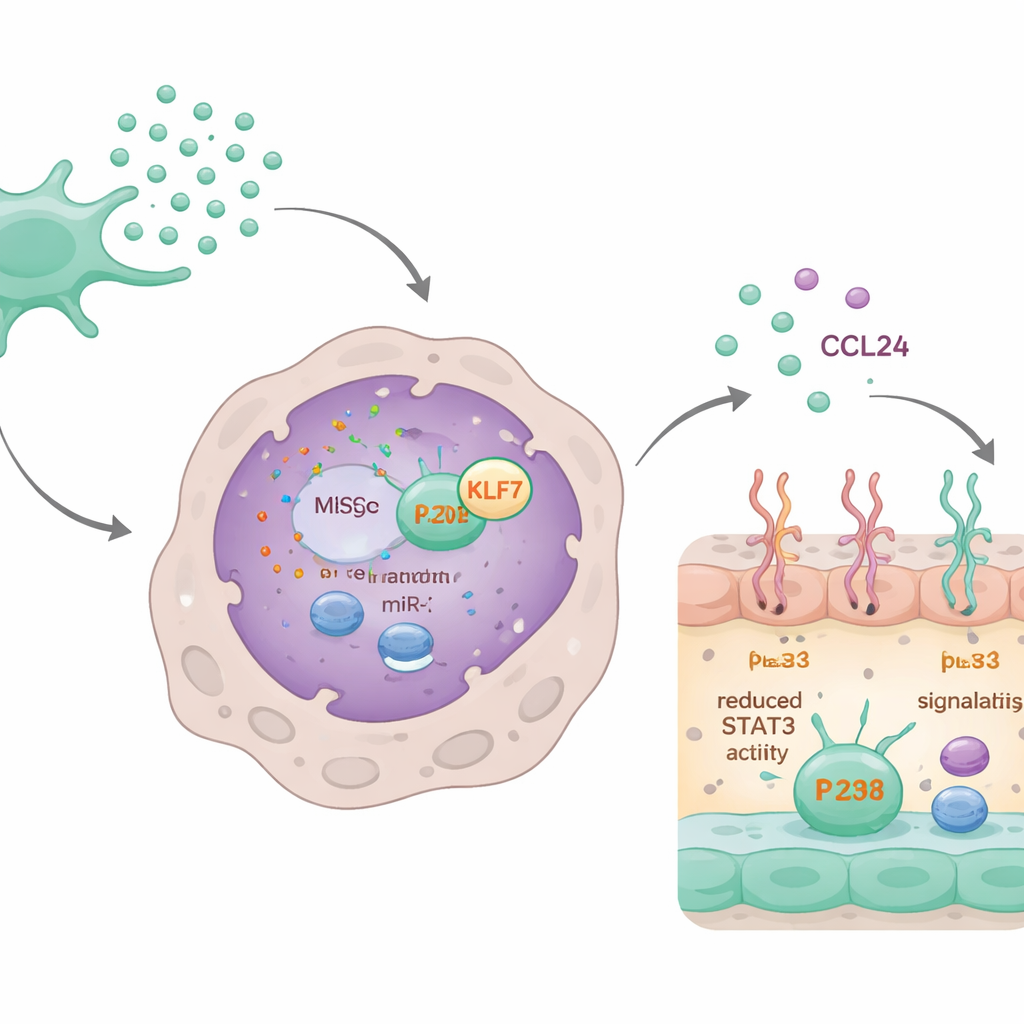
关闭瘢痕化的microRNA回路
进一步研究发现,外泌体内携带的一种特定microRNA——miR-320d,起到了关键作用。巨噬细胞容易摄取富含该microRNA的外泌体。进入细胞后,miR-320d与并降低一种称为KLF7的蛋白水平结合,KLF7通常有助于激活另一种蛋白STAT3。被激活的STAT3会结合CCL24基因并促进其表达。通过降低KLF7,miR-320d减少了STAT3的激活,进而降低了CCL24的合成与分泌。当阻断miR-320d或人为增加KLF7时,外泌体对CCL24及巨噬细胞行为的抑制效果大部分消失。
从细胞培养到活体实验
研究者改造了干细胞,使其释放富含额外miR-320d的外泌体,并将其与未改造的外泌体进行了比较。增强型外泌体被巨噬细胞摄取得更高效,并在降低KLF7水平、STAT3活性和CCL24释放方面产生更强的效果。在接受类透析处理的大鼠中,每周注射标准或富含miR-320d的外泌体均可减少腹膜增厚和胶原沉积。增强型外泌体提供了最大的保护,使组织外观更接近正常,并抑制了从巨噬细胞活化到上皮细胞转化和瘢痕形成的关键信号步骤。
这对透析患者可能意味着什么
这项工作描述了一个链式过程:巨噬细胞释放CCL24,推动透析膜走向瘢痕化和功能下降。来自腹膜干细胞的外泌体,尤其是携带miR-320d的外泌体,通过沉默决定CCL24表达的KLF7–STAT3开关打断了这条链。通俗地说,该研究提示患者自身来源的干细胞外泌体未来或可作为个性化、无细胞的治疗手段,用于减缓或预防腹膜损伤,帮助患者更长时间、安全地维持腹膜透析并减少并发症。
引用: Zhao, X., Xi, M., Qi, H. et al. Peritoneal MSCs-derived exosomes suppress CCL24 synthesis through miR-320d delivery contributing to the improvement of peritoneal dialysis-associated fibrosis. Sci Rep 16, 11998 (2026). https://doi.org/10.1038/s41598-026-42489-w
关键词: 腹膜透析, 腹膜纤维化, 巨噬细胞, 外泌体, 微小RNA疗法