Clear Sky Science · fr
Les exosomes dérivés des CSM péritonéales suppriment la synthèse de CCL24 via le transport de miR-320d contribuant à l’amélioration de la fibrose associée à la dialyse péritonéale
Pourquoi protéger la membrane de dialyse est important
Pour les personnes dont les reins ont cessé de fonctionner, la dialyse péritonéale offre la liberté de purifier leur sang à domicile en utilisant la paroi abdominale comme filtre naturel. Mais au fil des années, cette membrane délicate peut se cicatriser et s’épaissir, contraignant finalement les patients à abandonner ce traitement. Cette étude examine les causes de cette cicatrisation et évalue une stratégie cellulaire de pointe qui utilise de minuscules paquets biologiques pour apaiser les signaux immunitaires nocifs et aider à préserver la membrane.
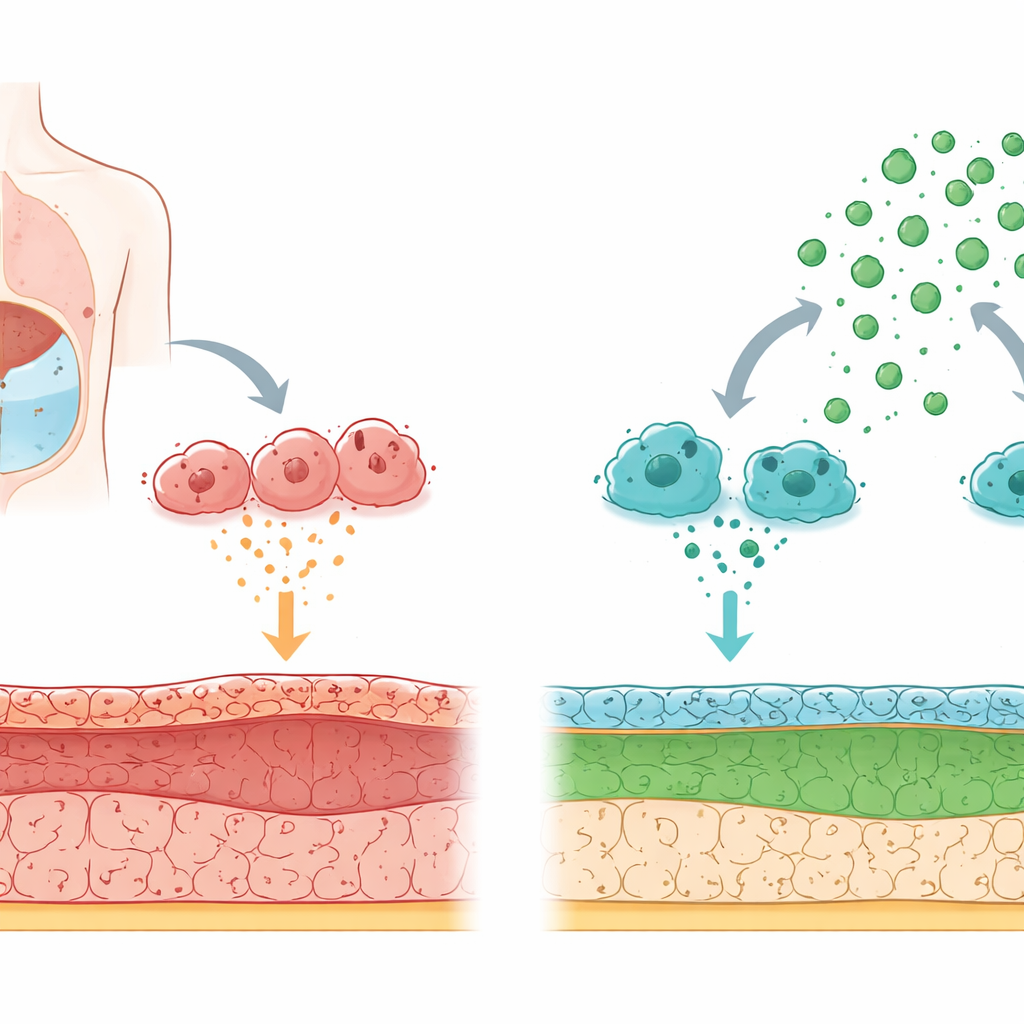
Comment le filtre du corps se détériore avec le temps
La dialyse péritonéale fonctionne en remplissant l’abdomen d’un liquide spécial afin que les déchets puissent passer du sang à travers la membrane péritonéale. Une exposition prolongée à un liquide de dialyse riche en glucose et des épisodes inflammatoires répétés endommagent progressivement cette paroi. Les cellules exposées au liquide peuvent changer de caractère : au lieu de se comporter comme des revêtements lisses et protecteurs, elles commencent à agir comme des cellules productrices de cicatrice qui déposent des fibres rigides. Ce changement, appelé transition des cellules de revêtement vers des cellules de type cicatriciel, entraîne l’épaississement et la perte de fonction de la membrane.
Les messagers immunitaires qui poussent à la cicatrisation
Les chercheurs se sont concentrés sur les macrophages, des cellules immunitaires qui patrouillent la cavité péritonéale. Dans un modèle de rat de lésion induite par la dialyse, ils ont trouvé des niveaux élevés d’une protéine de signalisation appelée CCL24 principalement dans ces macrophages. Lorsque les macrophages produisaient davantage de CCL24, les cellules du revêtement à proximité perdaient leur structure ordonnée et commençaient à produire des protéines fibreuses, un marqueur de la cicatrisation. Bloquer CCL24 dans les macrophages, ou bloquer son récepteur de surface (connu sous le nom de CCR3) ou son interrupteur chimique en aval (une voie impliquant la protéine p38), empêchait les cellules de revêtement de se transformer en cellules productrices de cicatrice. Cela place le CCL24 d’origine macrophagique au centre du processus de cicatrisation.
Des paquets de cellules souches qui calment les signaux nocifs
L’équipe s’est ensuite intéressée aux cellules souches mésenchymateuses collectées à partir du liquide d’évacuation des patients en dialyse. Ces cellules libèrent naturellement des exosomes—des vésicules nanométriques qui transportent des messages moléculaires tels que de petits ARN. Lorsque des macrophages ont été exposés au liquide de ces cellules souches, ou à des exosomes purifiés, leur production et libération de CCL24 ont fortement diminué. En conséquence, l’influence néfaste des sécrétions macrophagiques sur la paroi péritonéale a été réduite, et les cellules de revêtement ont conservé davantage de leurs caractéristiques protectrices. L’élimination des exosomes du liquide des cellules souches a en grande partie annulé cet avantage, montrant que ces minuscules paquets sont les principaux messagers thérapeutiques.
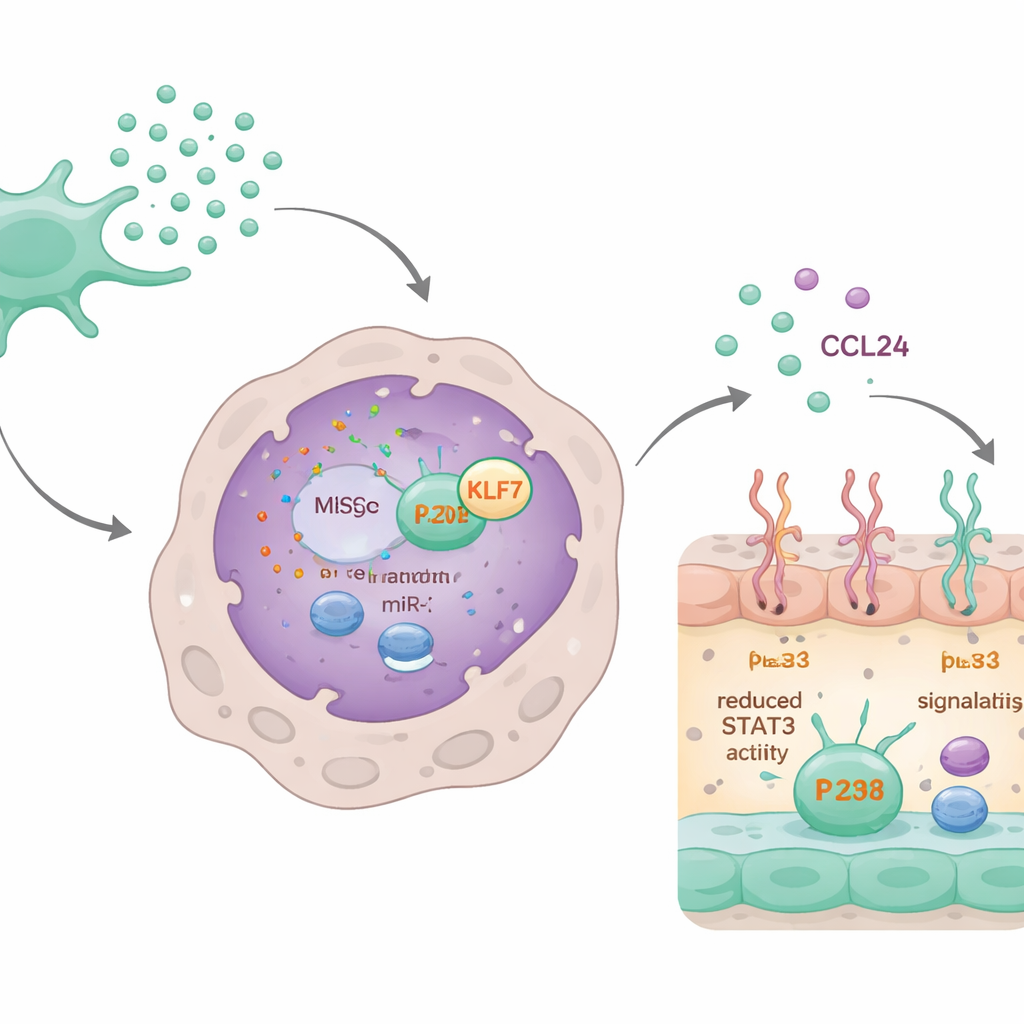
Le circuit microARN qui éteint la cicatrisation
En approfondissant, les scientifiques ont découvert qu’un microARN spécifique, miR-320d, contenu dans les exosomes était déterminant. Les macrophages absorbaient facilement les exosomes chargés de ce microARN. Une fois à l’intérieur, miR-320d se liait et réduisait les niveaux d’une protéine appelée KLF7, qui aide normalement à activer une autre protéine, STAT3. STAT3 activé se fixe au gène CCL24 et augmente sa production. En diminuant KLF7, miR-320d réduisait l’activation de STAT3, ce qui à son tour abaissait la synthèse et la sécrétion de CCL24. Lorsque miR-320d était bloqué ou que KLF7 était artificiellement augmenté, l’effet apaisant des exosomes sur la production de CCL24 et sur le comportement des macrophages disparaissait en grande partie.
De la culture cellulaire aux animaux vivants
Les chercheurs ont modifié des cellules souches pour libérer des exosomes enrichis en miR-320d supplémentaire et les ont comparés à des exosomes non modifiés. Les exosomes renforcés étaient mieux absorbés par les macrophages et provoquaient des diminutions plus marquées des niveaux de KLF7, de l’activité de STAT3 et de la libération de CCL24. Chez des rats soumis à un traitement de type dialyse, des injections hebdomadaires d’exosomes standards ou riches en miR-320d ont réduit l’épaississement et l’accumulation de collagène dans la membrane péritonéale. Les exosomes enrichis ont offert la meilleure protection, préservant une apparence tissulaire plus normale et atténuant les étapes clés du signal menant de l’activation des macrophages à la transformation des cellules de revêtement et à la cicatrisation.
Ce que cela pourrait signifier pour les personnes sous dialyse
Ce travail décrit une chaîne d’événements dans laquelle les macrophages libèrent CCL24, poussant la membrane de dialyse vers un état cicatriciel et moins fonctionnel. Les exosomes issus des cellules souches péritonéales, en particulier lorsqu’ils sont chargés de miR-320d, interrompent cette chaîne en silencant l’interrupteur KLF7–STAT3 qui active CCL24. En termes concrets, l’étude suggère que les exosomes dérivés des cellules souches du patient pourraient un jour être utilisés comme thérapie personnalisée sans cellules pour ralentir ou prévenir les lésions de la membrane péritonéale, aidant ainsi les patients à rester plus longtemps sous dialyse péritonéale avec moins de complications.
Citation: Zhao, X., Xi, M., Qi, H. et al. Peritoneal MSCs-derived exosomes suppress CCL24 synthesis through miR-320d delivery contributing to the improvement of peritoneal dialysis-associated fibrosis. Sci Rep 16, 11998 (2026). https://doi.org/10.1038/s41598-026-42489-w
Mots-clés: dialyse péritonéale, fibrose péritonéale, macrophages, exosomes, thérapie par microARN